SARTANS OF THE SECOND GENERATION: THERAPEUTIC POTENTIAL EXTENSION | Nedogoda
1. Kjeldsen S., Naditch-Brule L., Perlini S. et al. Increased prevalence of metabolic syndrome in uncontrolled hypertension across Europe: the Global Cardio-metabolic Risk Profile in Patients with hypertension disease survey. J Hypertens 2008; 26: 2064–70.
2. Ram C. Angiotensin receptor blockers: current status and future prospects. Am J Med 2008; 121: 656–63.
3. Nixon R.M., Muller E., Lowy A., Falvey H. Valsartan vs. other angiotensin II receptor blockers in the treatment of hypertension: a meta-analytical approach. Int J Clin Pract 2009; 63 (5): 766-775.
4. Song JC, White CM. Olmesartan medoxomil (CS-866).
5. Sharpe M, Jarvis B, Goa KL. Telmisartan: a review of its use in hypertension. Drugs 2001;61(10):1501-29.
6. Burnier M, Brunner HR. Angiotensin II receptor antagonists. Lancet 2000;355(9204):637-45.
7. Brunner HR. The new oral angiotensin II antagonist olmesartan medoxomil: a concise overview. J Hum Hypertens 2002;16 Suppl 2:S13-6.
8. Differences Among Angiotensin II Receptor Blockers. US Pharm 2004;10:HS19- HS25.
9. Kakuta H et al. Telmisartan has the strongest binding affinity to angiotensin II type 1 receptor: comparison with other angiotensin II type 1 receptor blockers.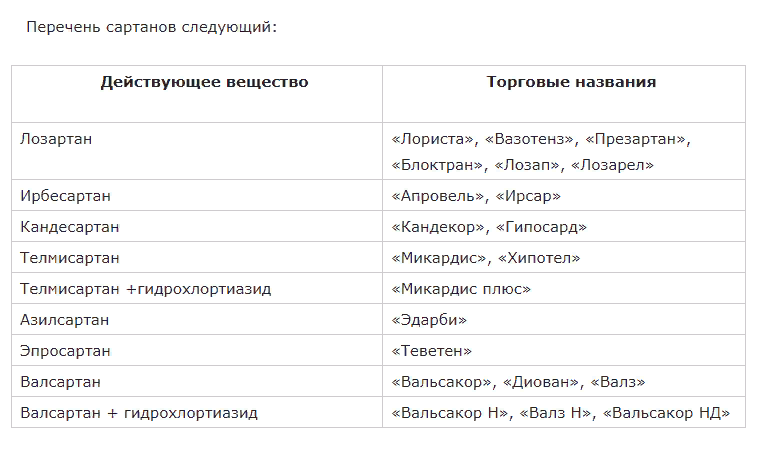
10. Nedogoda S.V. Hyperuricaemia and kidney damage in patients with hypertension and metabolic syndrome. Quality of life. Kachestvo zhizni. Meditsina 2008; 3: 16-27. Russian (Недогода С.В. Гиперурикемия и поражение почек у больных с артериальной гипертензией и метаболическим синдромом. Качество жизни. Медицина 2008; 3: 16-27).
11. Benson S, Pershadsingh H, Ho C et al. Identification of telmisartan as a unique angiotensin II receptor antagonist with selective PPARgammamodulating activity. Hypertension 2004; 43 (5): 993–1002.
12. Schupp M., Janke J., Clasen R. et al. Angiotensin type 1 receptor blockers induce peroxisome proliferator-activated receptor-gamma activity. Circulation 2004; 109: 2054–7.
13. Babaev V., Ishiguro H., Ding L. et al. Macrophage expression of peroxisome proliferator-activated receptor α reduces atherosclerosis in low density lipoprotein receptor deficient mice. Circulation 2007; 116: 1404–1412.
Babaev V., Ishiguro H., Ding L. et al. Macrophage expression of peroxisome proliferator-activated receptor α reduces atherosclerosis in low density lipoprotein receptor deficient mice. Circulation 2007; 116: 1404–1412.
14. Cresci S. PPAR genomics and pharmacogenomics: implications for cardiovascular disease. PPAR Res 2008;2008:374549.
15. Duan S.Z., Ivashchenko C.Y., Russell M.W. et al.Cardiomyocyte-specffic knockout and agonist of per-oxisome proliferator-aVolctivated receptor-γ both induce cardiac hypertrophy in mice. Circulation Research 2005; 97(4): 372–379.
16. Beltowski J. Role of leptin in blood pressure regulation and arterial hypertension. J Hypertens 2006; 5:789–801.
17. Fogo A.B. Potential for peroxisome proliferatoractivated receptor-[gamma] agonists in progression: beyond metabolism. Current Opinion in Nephrology and Hypertension 2008; 17(3):282–285.
Fogo A.B. Potential for peroxisome proliferatoractivated receptor-[gamma] agonists in progression: beyond metabolism. Current Opinion in Nephrology and Hypertension 2008; 17(3):282–285.
18. Kurtz T.W. Beyond the classic angiotensin-receptor blocker profile. Nature Reviews Cardiology 2008;5:S19–S26.
19. Kurtz T., Klein U. Next generation multifunctional angiotensin receptor blockers. Hypertens Res 2009; 32 (10): 826–34.
20. Bagry H.S., Raghavendram S., Carli F. Metabolic syndrome and insulin resistance. Anesthesiology 2008;108(3):506–523.
21. Leone T., Weinheimer C., Kelly D. A critical role for the peroxisome proliferator-activated receptor α (PPARα) in the cellular fasting response: the PPARα-null mouse as a model of fatty acid oxidation disorders. Proc Natl Acad Sci USA 1999; 96: 7473–7478.
Proc Natl Acad Sci USA 1999; 96: 7473–7478.
22. Li X., Hansen P.A., Xi L. et al. Distinct mechanisms of glucose lowering by specific agonists for per-oxisomal proliferator activated receptor gamma and retinoic acid X receptors. J Biol Chem 2005; 280(46): 38317–38327.
23. Sugimoto K., Qi N.R., Kazdová L. et al. Telmisartan but not valsartan increases caloric expenditure and protects against weight gain and hepatic steatosis. Hypertension 2006;47(5):1003-9.
24. Matchar D.B., McCrory D.C., Orlando L.A. et al. Systematic Review: Comparative Effectiveness of An-giotensin-Converting Enzyme Inhibitors and Angiotensin II Receptor Blockers for Treating Essential Hypertension. Ann Intern Med 2008;148:16–29.
25. Quinn C.E., Hamilton P.K., Lockhart C.J. Thiazolidinediones: effects on insulin resistance and the cardiovascular system. British J Pharmacology 2008; 153: 636–645.
Quinn C.E., Hamilton P.K., Lockhart C.J. Thiazolidinediones: effects on insulin resistance and the cardiovascular system. British J Pharmacology 2008; 153: 636–645.
26. Miura Y., Yamamoto N., Tsunekawa S. et al. Metabolic Effects of Replacing Valsartan or Candesartan by Telmisartan. Diabetes Care 2005; 28(3): 757–8.
27. Vitale C., Mercuro G., Castiglioni C. Metabolic effect of telmisartan and losartan in hypertensive patients with metabolic syndrome. Cardiovasc Diabetol 2005;4:6.
28. Derosa G., Ragonesi P.D., Mugellini A. et al. Effects of telmisartan compared with eprosartan on blood pressure control, glucose metabolism and lipid profile in hypertensive, type 2 diabetic patients: a ran-domized, double-blind, placebo-controlled 12-month study. Hypertens Res 2004;27(7):457-64.
29. van Zwieten P.A. Angiotensin II receptor antagonists (AT1-blockers, ARBs, sartans): similarities and differences. Neth Heart J 2006; 14(11):381–387.
30. Sugawara A., Takeuchi K., Uruno A. at al. Negative regulation of rat thromboxane receptor gene by 15- deoxy-D12, 14-PGJ2 and troglitazone by activating PPAR-g in vascular smooth muscle cells. J Am Soc Nephrol 1998; 9: 358A.
31. Ayuko Nakano, Yoshiyuki Hattori, Chie Aoki et al. Telmisartan inhibits cytokine-induced nuclear factor-kB activation independently of the peroxisomeproliferators-activated receptor-α. Hypertension Research 2009;32: 765–769.
 Clin Ther 2001;23(6):833-50.
Clin Ther 2001;23(6):833-50.33. Sharma A., Davidson J., Koval S., Lacourcière Y. Telmisartan/hydrochlorothiazide versus valsar-tan/hydrochlorothiazide in obese hypertensive patients with type 2 diabetes: the SMOOTH study. Cardiovascular Diabetology 2007; 6:28-36.
34. Hsueh W.A., Quinones M.J. Role of endothelial dysfunction in insulin resistance. Am J Cardiol 2003;92:10J–17J.
35. Yusuf S., Teo K., Anderson C. et al. Effects of the angiotensin-receptor blocker telmisartan on cardiovascular events in high-risk patients intolerant to angiotensin-converting enzyme inhibitors: a randomized controlled trial. Lancet 2008; 372: 1174–83.
36. Yusuf S., Diener H., Sacco R. et al. Telmisartan to prevent recurrent stroke and cardiovascular events. N Engl J Med 2008; 359: 1225–37.
N Engl J Med 2008; 359: 1225–37.
расширение терапевтических возможностей – тема научной статьи по фундаментальной медицине читайте бесплатно текст научно-исследовательской работы в электронной библиотеке КиберЛенинка
ТОЧКА ЗРЕНИЯ
САРТАНЫ ВТОРОГО ПОКОЛЕНИЯ: РАСШИРЕНИЕ ТЕРАПЕВТИЧЕСКИХ ВОЗМОЖНОСТЕЙ
С.В. Недогода*
Волгоградский государственный медицинский университет. 400131, Волгоград, пл. Павших Борцов, 1
Сартаны второго поколения: расширение терапевтических возможностей
С.В. Недогода*
Волгоградский государственный медицинский университет. 400131, Волгоград, пл. Павших Борцов, 1
Проанализированы особенности применения блокатора рецепторов ангиотензина II телмисартана с учетом его клинико-фармакологических характеристик. Особое внимание уделено преимуществам телмисартана перед другими сартанами. Подробно рассмотрены особенности взаимодействия телмисартана с рецепторами, активирующими пролиферацию пероксисом (peroxisome p ro l iferato r — a ctivated receptors, PPAR). Характер взаимодействие с этими рецепторами лежит в основе фармакодинамических эффектов представителей различных групп лекарственных препаратов. С учетом представленных данных сделан вывод о существенных преимуществах антигипертензивной терапии с применением телмисартана.
Особое внимание уделено преимуществам телмисартана перед другими сартанами. Подробно рассмотрены особенности взаимодействия телмисартана с рецепторами, активирующими пролиферацию пероксисом (peroxisome p ro l iferato r — a ctivated receptors, PPAR). Характер взаимодействие с этими рецепторами лежит в основе фармакодинамических эффектов представителей различных групп лекарственных препаратов. С учетом представленных данных сделан вывод о существенных преимуществах антигипертензивной терапии с применением телмисартана.
Ключевые слова: телмисартан, рецепторы, активирующие пролиферацию пероксисом, артериальная гипертония, сердечно-сосудистый риск.
РФК 2011;7(4):477-482
Sartans of the second generation: therapeutic potential extension
S.V. Nedogoda*
Volgograd State Medical University. 1, Pavshikh Bortsov Sq., Volgograd, 400131, Russia
1, Pavshikh Bortsov Sq., Volgograd, 400131, Russia
Peculiarities of the treatment with angiotensin II receptor blocker telmisartan are analyzed taking into account its clinical and pharmacological characteristics. Special attention is paid to the telmisartan benefits in comparison with other sartans. Key details of telmisartan interaction with peroxisome proliferator-activated receptors (PPAR) are discussed. Mode of this interaction distinguishes pharmacodynamic effects of different medicines. On the basis of presented data author concludes that antihypertensive therapy with telmisartan provides significant benefits. Key words: telmisartan, peroxisome proliferator-activated receptors, hypertension, cardiovascular risk.
Rational Pharmacother. Card. 2011;7(4):477-482
*Автор, ответственный за переписку (Corresponding author): nedogodasv@rambler./70/70.jpg) ru
ru
Введение
Последние годы ознаменовались активным сравнением достоинств и недостатков ингибиторов ангио-тензин-превращающего фермента (ИАПФ) и сартанов при лечении артериальной гипертензии (АГ). Эта перманентная дискуссия отодвинула на второй план вопрос о класс-специфических эффектах антигипертензив-ных средств и поиске препаратов-лидеров в своих классах, что имеет несомненное практическое значение. Дополнительную актуальность эта проблема приобретает в связи с тем, что в настоящее время от 20% до 30% пациентов получают монотерапию (естественно, что у них имеет смысл использовать наиболее эффективный препарат и максимально индивидуализировать фармакотерапию, решающую также проблемы комор-бидной патологии). Также доказано, что имеются существенные различия между фиксированными комбинациями антигипертензивных препаратов, причем не только по силе их гипотензивного эффекта, но и по выраженности органопротекции и метаболической нейтральности. При этом принципиальное значение имеют составляющие данных комбинаций.
При этом принципиальное значение имеют составляющие данных комбинаций.
Еще одним важным требованием к современной ан-тигипертензивной терапии является ожидание её позитивного влияния на компоненты метаболического син-
Сведения об авторе:
Недогода Сергей Владимирович — д.м.н, профессор, заведующий кафедрой терапии и эндокринологии ВолгГМУ
дрома (избыточный вес, объем жировой ткани, повышенный уровень холестерина и триглицеридов, нарушения углеводного обмена, инсулинорезистент-ность) и ожирения, которые в популяции в целом и среди пациентов с АГ приобретают характер «неинфекционной эпидемии» [1]. Если рассматривать спектр современных антигипертензивных препаратов с этой позиции, то становится совершенно очевидным, что между представителями одного и того же класса и практически в каждом из них можно выделить как минимум два поколения (генерации). Причем представители новых поколений имеют ряд важных клинически значимых отличий, и можно говорить о том, что многие из них являются бифункциональными антигипертензив-ными средствами, которые помимо снижения АД оказывают положительное влияние на патогенетические механизмы нарушения обмена углеводов, липидов, ожирения и неинфекционного воспаления [2]. Такая ситуация особенно ярко проявляется при сравнении сартанов первого и второго поколений.
Причем представители новых поколений имеют ряд важных клинически значимых отличий, и можно говорить о том, что многие из них являются бифункциональными антигипертензив-ными средствами, которые помимо снижения АД оказывают положительное влияние на патогенетические механизмы нарушения обмена углеводов, липидов, ожирения и неинфекционного воспаления [2]. Такая ситуация особенно ярко проявляется при сравнении сартанов первого и второго поколений.
Сартаны
Прежде всего, необходимо озвучить следующую позицию [3]: принципиальных различий между сартанами по силе антигипертензивного действия нет, максимальная разница составляет около 2 мм рт.ст. по систолическому (САД) и диастолическому АД (ДАД), хотя ранее небольшие прямые сравнительные исследования указывали на возможность более существен-
Таблица 1. Сартаны: клиническая фармакология [по 4-9 ] (Данная и последующие таблицы опубликованы с разрешения ООО «Берингер Ингельхайм»)
Сартан Пик действия, час Т1/2 Кратность приема в сут Суточная доза, мг Биодоступность, % Объем распределения, л Коэффициент липофильности Взаимодействие с пищей
Лозартан 1-4 6-9 1-2 50-100 33 34 -2,45 (активные метаболиты) Минимально
Валсартан 2-4 6-9 1 80-320 25 17 -0,95 1 на 40-50%
Ирбесартан 1,5-2 11-15 1 150-300 60-80 50-53 1,48 Нет
Кандесартан 3-4 3-11 1-2 8-32 15 9 -0,96 Нет
Эпросартан 1-2 5-9 2 400-600 13 308 — 1 на 25%
Телмисартан 0,5-1 0 2 /\ 1 40-160 42-58 5 О О 3,20 1 на 6%
ных различий между препаратами. Большинство из сар-танов (лозартан, валсартан, ирбесартан, кандесартан, эпросартан, олмесартан), используемых в России, являются представителями первого поколения. Безусловно, между ними имеются существенные фармакокинетические различия (табл. 1), но с позиции фар-макодинамических эффектов, пожалуй, особняком стоит лозартан, который имеет наибольшую доказательную базу применения при гиперурикемии и неалкогольной жировой болезни печени [10].
Большинство из сар-танов (лозартан, валсартан, ирбесартан, кандесартан, эпросартан, олмесартан), используемых в России, являются представителями первого поколения. Безусловно, между ними имеются существенные фармакокинетические различия (табл. 1), но с позиции фар-макодинамических эффектов, пожалуй, особняком стоит лозартан, который имеет наибольшую доказательную базу применения при гиперурикемии и неалкогольной жировой болезни печени [10].
В России единственным доступным блокатором рецепторов ангиотензина II (БРА II) второго поколения является телмисартан (Микардис). В отличие от всех других сартанов Микардис оказывает выраженное влияние на рецепторы, активирующие пролиферацию перокси-сом (Peroxisome Proliferator Activated Receptor, PPAR), подтипа гамма (у) и обеспечивает синергизм влияния на ключевые факторы риска развития сердечно-сосудистых осложнений (рис. 1) [11]. Кроме этого, по ряду своих фармакокинетических и фармакологических свойств телмисартан существенно (в разы!) превосходит сартаны первого поколения — валсартан, кандесартан, лозартан, олмесартан, эпросартан, ирбесартан (рис. 2; табл. 1) [6-1 2].
2; табл. 1) [6-1 2].
Для лучшего понимания терапевтических возможностей, которые отрываются у Микардиса за счет его влияния на PPAR-рецепторы, необходимо представлять физиологические эффекты, регулируемые ими:
• клеточная дифференцировка;
• метаболизм липидов;
• метаболизм углеводов;
• чувствительность жировой ткани к инсулину;
• дифференцировка адипоцитов;
• окисление жирных кислот.
Интерес к PPAR-рецепторам в последнее десятилетие существенно вырос, поскольку стало ясно, что в основе фармакодинамических эффектов представителей различных групп лекарственных препаратов [гиполи-пидемических (фибраты), гипотензивных (телмисартан), инсулиносенситайзеров (тиазолидиндионы)] лежит их влияние на PPARa и PPARY -рецепторы [13]. АВР4), который транспортирует СЖК в ядро клетки; синтез белков LXRa и инсулин-индуци-
АВР4), который транспортирует СЖК в ядро клетки; синтез белков LXRa и инсулин-индуци-
Ангиотензин
воспаление
ремоделирова-тромбоз ние
сосудов
ТАД
нарушение
обмена
холестерина
PPARY-агонисты
БРАН
Рис. 1. PPARY-агонисты являются синергистами БРА II (Данный и последующие рисунки опубликованы с разрешения ООО «Берингер Ингельхайм»)
степень относительной активации О 1Л О 1Л О 1Л о 1111111
26,67 елмисарта
2,13 1 33 | | 1,0 1,17 0,83 0,83 | — !
т н кандесартан олмесартан лозартан ирбесартан валсартан эпросартан
Рис. 2. Сартаны: активация PPARY-рецепторов [5]
2. Сартаны: активация PPARY-рецепторов [5]
рующего протеина 1№Ю-1, регуляторов экспрессии и созревания транскрипционного фактора SREBP-1 с, фосфоенолпируват-карбоксилазы (РЕРСК-С), ключевого фермента глицеронеогенеза в адипоцитах [15].
Экспериментальные и клинические исследования показали ключевую роль PPARY-рецепторов в регуляции дифференцировки и нормального функционирования адипоцитов, процессе накопления липидов жировой ткани [16]. PPARY-рецепторы также способствуют превращению макрофагов в пенистые клетки путем увеличения захвата окисленных липопротеинов низкой плотности (ЛПНП), что является одним из важнейших механизмов атерогенеза. Кроме этого, они подавляют продукцию воспалительных цитокинов и повышают чувствительность к инсулину [17].
Таким образом, за счет влияния на PPARY-рецепторы возможно наличие у классического гипотензивного препарата дополнительных важных клинических свойств. -кВ и усиления выработки синтазы оксида азота. Кроме этого, активация PPARY-рецепторов приводит к подавлению экспрессии молекул адгезии, транскрипции гена тромбоксансинтазы, тромбоцитозависимого и базального факторов роста фибробластов [18,19].
-кВ и усиления выработки синтазы оксида азота. Кроме этого, активация PPARY-рецепторов приводит к подавлению экспрессии молекул адгезии, транскрипции гена тромбоксансинтазы, тромбоцитозависимого и базального факторов роста фибробластов [18,19].
♦ Нормализация липогенеза и уменьшение инсули-норезистентности
PPARY рецепторы преимущественно находятся в белой жировой ткани, в которой регулируют ее массу, диф-ференцировку преадипоцитов и чувствительность к инсулину [20]. Стимуляция PPARY2-рецепторов в пре-адипоцитах увеличивает число малых жировых клеток и переводят в состояние апоптоза более крупные ади-поциты в подкожной и висцеральной жировой тканях [21]. Это повышает чувствительность тканей к инсулину, так как именно более крупные адипоциты наименее чувствительны к инсулину и способны к продукции ли-
попротеинлипазы. Все это приводит к тому, что вторично уменьшается продукция резистина, лептина, ^-6, ФНО-а, ингибитора активатора плазминогена 1 ^А1-1) и протеина хемотаксиса моноцитов-1 (MCP-1) [22].
Благоприятное влияние на экспрессию адипонектина является наиболее важным фактором в коррекции инсулинорезистентности благодаря тому, что улучшает чувствительность печени к инсулину [1 7], нормализует содержание липидов (в том числе триглицеридов) в ней, в том числе у больных сахарным диабетом 2 типа.
Принципиально важно, что телмисартан оказывает значительно более выраженное положительное влияние в сравнении с сартанами первого поколения (рис. 3-6).
♦ Нормализация углеводного обмена
PPARY-рецепторы в последние годы стали рассматриваться как одно из ключевых звеньев патогенеза инсулинорезистентности и метаболического синдрома [24], поскольку они обеспечивают регуляцию образования глюкозы в печени, влияя на окисление жирных кислот. При активации PPARY-рецепторов скелетных мышц повышается поглощение глюкозы тканями и уменьшается уровень глюкозы в крови. Благодаря снижению уровня СЖК и глюкозы в крови подавляются липо- и глюкотоксичность и восстанавливается секреторная активность р-клеток поджелудочной железы [25].
Благодаря снижению уровня СЖК и глюкозы в крови подавляются липо- и глюкотоксичность и восстанавливается секреторная активность р-клеток поджелудочной железы [25].
Необходимо еще раз подчеркнуть, что телмисартан — единственный из всех сартанов, которому свойственно комплексное влияние на показатели углеводного, липидного обмена и основные патогенетические факторы развития метаболического синдрома и ожирения. Так, в исследовании [26] у пациентов с АГ и сахарным диабетом 2 типа после перевода пациентов с 6-месячной терапии валсартаном (80 мг/сут) или кан-десартаном (8 мг/сут) на телмисартан (40 мг/сут) через 1 2 нед наблюдалось достоверное улучшение метаболических показателей (рис. 7, 8).
Кроме этого, прямые сравнительные исследования телмисартана с другими представителями этого класса ан-тигипертензивных препаратов однозначно указывают на его более выраженное положительное влияние на показатели углеводного и липидного обмена (рис. «»
«»
ill
Количество клеток
г у
* ANOVA, (р<0,001) и критерий Стьюдента-Ньюмена-Койлса, (р<0,05) по сравнению с контрольной группой и группой валсартана. ** (р<0,05) по сравнению с контрольной группой
Рис. 4. Объем (пиколитр) и количество адипоцитов при терапии телмисартаном и валсартаном [23]
Масса печени
В Печеночные триглицериды
90 ‘
«■ Т
★ ★
и
г
*ANOVA, (р<0,001) и критерий Стьюдента-Ньюмена-Койлса, (р<0,05) по сравнению с группой валсартана и контрольной группой; **ANOVA, (р<0,01) и критерий Стьюдента-Ньюмена-Койлса, р<0,05 по сравнению с контрольной группой
ü 11 ¥■
« 10
Энергозатраты
Общая активность
Время, час Время, час
* ANOVA, (р<0,01) и критерий Стьюдента-Ньюмена-Койлса, (р<0,05) по сравнению с группой валсартана и группой контроля
Рис. 5. Уровень триглицеридов и массы печени при терапии телмисартаном и валсартаном [23]
5. Уровень триглицеридов и массы печени при терапии телмисартаном и валсартаном [23]
цепторов ангиотензина II и активации PPARY-рецепторов не нова. Так предпринимались попытки сочетанного применения сартанов и тиазолидиндионов. Было показано, что при сравнении эффекта пиоглитазона (1 мг/кг/день) в сочетании с кандесартаном и высокой дозы пиоглитазона (2 мг/кг/день) в виде монотерапии сочетание пиоглитазона с кандесартаном имеет очевидные преимущества [29].
Микардис сочетает в себе два механизма воздействия на систему рецепторов PPARY. С одной стороны, БРА II селективно блокируют рецепторы АТ 1, что приводит к стимуляции рецепторов АТ2 и PPARY. С другой стороны, БРА II могут проникать через мембрану клетки и ядра и связываться непосредственно с рецепторами PPARY, активируя продукцию инсулиночувствительного протеина [30]. При этом важно подчеркнуть, что Микардис является частичным агонистом PPARY рецепторов, а значит лишен тех нежелательных эффектов влияния на сердечно-сосудистую систему (табл. 2), которые имеются у тиазолидиндионов, что обусловлено частичной, а не полной активацией PPARY-рецепторов. При этом блокада ренин-ангиотензин-альдостероновой системы Микардисом препятствует увеличению реабсорбции
2), которые имеются у тиазолидиндионов, что обусловлено частичной, а не полной активацией PPARY-рецепторов. При этом блокада ренин-ангиотензин-альдостероновой системы Микардисом препятствует увеличению реабсорбции
Рис. 6. 24-часовые энерготраты и активность при терапии телмисартаном и валсартаном [23]
натрия и воды почками в ответ на периферическую ва-зодилатацию [21].
По сравнению с другими сартанами Микардис обладает максимальной эффективностью в отношении активации PPARy рецепторов. Структура молекулы телмисартана имеет сходство с тиазолидиндионами и обеспечивает два механизмами действия: блокирование АТ 1 -рецепторов и частичную активацию PPARY-рецепторов, которая составляет приблизительно 25-30% от максимального уровня, достигаемого при приеме пиоглитазона или розиглитазона (табл. 3) [31].
Наличие у телмисартана дополнительных свойств, определяемых его влиянием на PPARY-рецепторы, в значительной мере решает проблему комбинации с ти-азидными диуретиками. Эффекты телмисартана, опосредуемые PPARY-рецепторами, в наибольшей степени нивелируют возможные побочные эффекты при использовании в комбинированной терапии тиазидных диуретиков. Так, в ряде исследований (ALLHAT, INSIGHT, ALPINE, ASCOT, PHYLLIS, CROSS, MEDICA) было показано, что у проблемных пациентов с АГ использование тиазидных диуретиков повышает уровень глюкозы крови, мочевой кислоты, холестерина, триглицеридов и уси-
Эффекты телмисартана, опосредуемые PPARY-рецепторами, в наибольшей степени нивелируют возможные побочные эффекты при использовании в комбинированной терапии тиазидных диуретиков. Так, в ряде исследований (ALLHAT, INSIGHT, ALPINE, ASCOT, PHYLLIS, CROSS, MEDICA) было показано, что у проблемных пациентов с АГ использование тиазидных диуретиков повышает уровень глюкозы крови, мочевой кислоты, холестерина, триглицеридов и уси-
Глюкоза крови
НД
Инсулин крови
Триглицериды
мЕд/л
НД=недостоверно
мг/дл
10
Адипоннектин
Р<0,01
мг/дл
0,2
0,15
Кандесартам/ Телмисартан Валсартан
вч-СРБ=высокочувствительный С-реактивный белок
вч-СРБ
Р<0,05
Каидесартам/ Телмисартан Валсартан
Рис. 7. Метаболические эффекты: последствия замены валсартана и кандесартана на телмисартан (1) [26]
7. Метаболические эффекты: последствия замены валсартана и кандесартана на телмисартан (1) [26]
Рис. 8. Метаболические эффекты: последствия замены валсартана и кандесартана на телмисартан (2) [26]
*-р<0,05 по сравнению с лозартаном. Продолжительность исследования 3 мес.
СГП=свободная глюкоза плазмы, СИП=свободный инсулин плазмы, НОМА-ИР=индекс гомеостатической модели оценки инсулинорезистентности, НЬА1с=гликозилированный гемоглобин
Ц. -5
і m -10
¡і
о b -IS
I
I
s -20
5
n a -25
г
І ЦГ -30
-35
Общий холестерин
Холестерин ЛНП
Триглицериды
■ Эпросартан 600 нг (п=39) ■Телмисартан 40 мг (п=40)
*-p<0,05 по сравнению с эпросартаном. Продолжительность исследования 12 мес
Продолжительность исследования 12 мес
Рис. 9. Влияние телмисартана на показатели углеводного и липидного обмена [27]
ливает инсулинорезистентность. В свете изложенного становится очевидным, что в ряду комбинаций БРА II и гидрохлортиазида (ГХТЗ) сочетание телмисартана 80 мг и ГХТЗ 1 2,5 мг (МикардисПлюс) является наиболее безопасным с точки зрения снижения риска возможных побочных метаболических эффектов в сравнении с другими комбинациями «БРА II и ГХТЗ». Кроме этого, риск развития гипокалиемии (основной причины повышения уровня глюкозы) при увеличении дозы телмисартана до 80 мг существенно снижается (рис. 11 ).
Важными представляются результаты исследования SMOOTH (A comparison of Telmisartan plus HCTZ with amlodipine plus HCTZ in Older patients with predominantly Systolic hypertension) [33], в котором МикардисПлюс
Таблица 2. Эффекты агонистов PPARY-рецепторов
Эффекты агонистов PPARY-рецепторов
Рис. 10. Влияние телмисартана на показатели липидного обмена [28]
80/1 2,5 мг оказался эффективнее, чем валсартан/ГХТЗ (160/12,5 мг/), у 840 пациентов с ожирением (ИМТ>27 кг/м2) и АГ, в большей степени снижая САД и ДАД, соответственно, на 3,9 и 2,0 мм рт.ст. (<0,001). Интересен и тот факт, что телмисартан высокоэффективен при АГ индуцированной высококалорийным питанием [34].
Логично и то, что сочетание у телмисартана двух свойств приводит к существенному снижению риска развития сахарного диабета 2 типа. Так, в исследованиях TRANSCEND [35] и PRoFESS [36] была доказана способность препарата снижать риск развития сахарного диабета 2 типа на 16% (р<0,05) у пациентов с высоким и очень высоким риском развития сердечно-сосудистых осложнений.
Эффект Неселективные PPARy активаторы (глитазоны) Селективные PPARy активаторы (телмисартан)
Улучшение метаболизма глюкозы и липидов ДА ДА
Гипертрофия адипоцитов ДА НЕТ
Задержка жидкости ДА НЕТ
Прибавка в весе ДА НЕТ
Таблица 3.2008/mir/16/2.png) Биологические эффекты PPARY-агонистов и БРА II — синергизм в снижении риска развития СД
Биологические эффекты PPARY-агонистов и БРА II — синергизм в снижении риска развития СД
Эффект PPARy БРА II
Утилизация глюкозы скелетными мышцами ттт т
Образование глюкозы печенью 1 ?
Предотвращение апоптоза в-клеток тт т
Продукция адипонектина
• Воспаление 11 ?
• Адипонектин ттт т
Циркулирующие биомаркеры
• С-реактивный белок 111 1
• Тканевый активатор плазминогена 11 11
Заключение
Будущее класса сартанов тесно связано с развитием бифункциональных препаратов. Микардис — первый и единственный зарегистрированный в России сар-тан второго поколения, имеющий два механизма действия и влияющий на несколько терапевтических ми-
Микардис — первый и единственный зарегистрированный в России сар-тан второго поколения, имеющий два механизма действия и влияющий на несколько терапевтических ми-
Н12.5 (n-73) Т40/Н12.5 (n-70) Т80/М12.5 (п 73)
0,02
Н12,5=ГХТЗ 12,5 мг; Т40/80=телмисартан 40/80 мг. Длительность исследования 8 нед
Рис. 11. Уменьшение гипокалиемического влияния гидрохлортиазида [32]
шеней. Уникальные фармакологические характеристики телмисартана и его способность уменьшать риск развития сердечно-сосудистых осложнений определяют необходимость самого широкого использования телмисартана в ежедневной клинической практике кардиолога и терапевта для достижения нашей конечной цели — снижения смертности пациентов.
Литература
1. Kjeldsen S., Naditch-Brule L., Perlini S. et al. Increased prevalence of metabolic syndrome in uncontrolled hypertension across Europe: the Global Ca rdio-metabolic Risk Profile in Patients with hypertension disease survey, J Hypertens 2008; 26: 2064-70.
Kjeldsen S., Naditch-Brule L., Perlini S. et al. Increased prevalence of metabolic syndrome in uncontrolled hypertension across Europe: the Global Ca rdio-metabolic Risk Profile in Patients with hypertension disease survey, J Hypertens 2008; 26: 2064-70.
2. Ram C. Angiotensin receptor blockers: current status and future prospects. Am J Med 2008; 121: 656-63.
3. Nixon R.M., Muller E., Lowy A., Falvey H. Valsartan vs. other angiotensin II receptor blockers in the treatment of hypertension: a meta-analytical approach. Int J Clin Pract 2009; 63 (5): 766-775.
4. Song JC, White CM. Olmesartan medoxomil (CS-866). An angiotensin II receptor blocker for treatment of hypertension. Formulary 2001 ; 36: 487-499.
5. Sharpe M, Jarvis B, Goa KL. Telmisartan: a review of its use in hypertension. Drugs 2001 ;61 (10):1501 —
Drugs 2001 ;61 (10):1501 —
29.
6. Burnier M, Brunner HR. Angiotensin II receptor antagonists. Lancet 2000;355(9204):637-45.
7. Brunner HR. The new oral angiotensin II antagonist olmesartan medoxomil: a concise overview. J Hum Hypertens 2002;16 Suppl 2:S13-6.
8. Differences Among Angiotensin II Receptor Blockers. US Pharm 2004;10:HS19- HS25.
9. Kakuta H et al. Telmisartan has the strongest binding affinity to angiotensin II type 1 receptor: comparison with other angiotensin II type 1 receptor blockers. Int J Clin Pharmacol Res 2005; 25: 41-51.
10. Nedogoda S.V Hyperuricaemiaand kidney damage in patients with hypertension and metabolic syndrome. Quality of life. Kachestvo zhizni. Meditsina 2008; 3: 16-27. Russian (Недогода С.В. Ги-перурикемия и поражение почек у больных с артериальной гипертензией и метаболическим синдромом. Качество жизни. Медицина 2008; 3: 16-27).
Meditsina 2008; 3: 16-27. Russian (Недогода С.В. Ги-перурикемия и поражение почек у больных с артериальной гипертензией и метаболическим синдромом. Качество жизни. Медицина 2008; 3: 16-27).
11. Benson S, Pershadsingh H, Ho C et al. Identification of telmisartan as a unique angiotensin II receptor antagonist with selective PPARgammamodulating activity. Hypertension 2004; 43 (5): 993-1002.
12. Schupp M., Janke J., Clasen R. et al. Angiotensin type 1 receptor blockers induce peroxisome prolif-erator-activated receptor-gamma activity. Circulation 2004; 109: 2054-7.
13. Babaev V., Ishiguro H., Ding L. et al. Macrophage expression of peroxisome proliferator-activated receptor a reduces atherosclerosis in low density lipoprotein receptor deficient mice. Circulation 2007; 1 16: 1404-1412.
14. Cresci S. PPAR genomics and pharmacogenomics: implications for cardiovascular disease. PPAR Res 2008;2008:374549.
Cresci S. PPAR genomics and pharmacogenomics: implications for cardiovascular disease. PPAR Res 2008;2008:374549.
15. Duan S.Z., Ivashchenko C.Y, Russell M.W. et al.Cardiomyocyte-specffic knockout and agonist of peroxisome prol i ferator- aVol cti va ted receptor-Y both induce cardiac hypertrophy in mice. Circulation Research 2005; 97(4): 372-379.
17. Beltowski J. Role of leptin in blood pressure regulation and arterial hypertension. J Hypertens 2006; 5:789-801.
17. Fogo A.B. Potential for peroxisome proliferatoractivated receptor-[gamma] agonists in progression: beyond metabolism. Current Opinion in Nephrology and Hypertension 2008; 1 7(3):282-285.
18. Kurtz T.W. Beyond the classic angiotensin-receptor blocker profile. Nature Reviews Cardiology 2008;5:S19-S26.
19. Kurtz T, Klein U. Next generation multifunctional angiotensin receptor blockers. Hypertens Res 2009; 32 (10): 826-34.
20. Bagry H.S., Raghavendram S., Carli F Metabolic syndrome and insulin resistance. Anesthesiology 2008;1 08(3):506-523.
21. Leone T, Weinheimer C., Kelly D. A critical role for the peroxisome proliferator-activated receptor a (PPARa) in the cellular fasting response: the PPARa-null mouse as a model of fatty acid oxidation disorders. Proc Natl Acad Sci USA 1999; 96: 7473-7478.
22. Li X., Hansen PA., Xi L. et al. Distinct mechanisms of glucose lowering by specific agonists for peroxisomal proliferator activated receptor gamma and retinoic acid X receptors. J Biol Chem 2005; 280(46): 38317-38327.
23. Sugimoto K. , Qi N.R., Kazdova L. et al. Telmisartan but not valsartan increases caloric expenditure and protects against weight gain and hepatic steatosis. Hypertension 2006;47(5):1003-9.
, Qi N.R., Kazdova L. et al. Telmisartan but not valsartan increases caloric expenditure and protects against weight gain and hepatic steatosis. Hypertension 2006;47(5):1003-9.
24. Matchar D.B., McCrory D.C., Orlando L.A. et al. Systematic Review: Comparative Effectiveness of Angiotensin-Converting Enzyme Inhibitors and Angiotensin II Receptor Blockers for Treating Essential Hypertension. Ann Intern Med 2008;148:16-29.
25. Quinn C.E., Hamilton PK., Lockhart C.J. Thiazolidinediones: effects on insulin resistance and the cardiovascular system. British J Pharmacology 2008; 1 53: 636-645.
26. Miura Y, Yamamoto N., Tsunekawa S. et al. Metabolic Effects of Replacing Valsartan or Candesartan by Telmisartan. Diabetes Care 2005; 28(3): 757-8.
27. Vitale C., Mercuro G., Castiglioni C.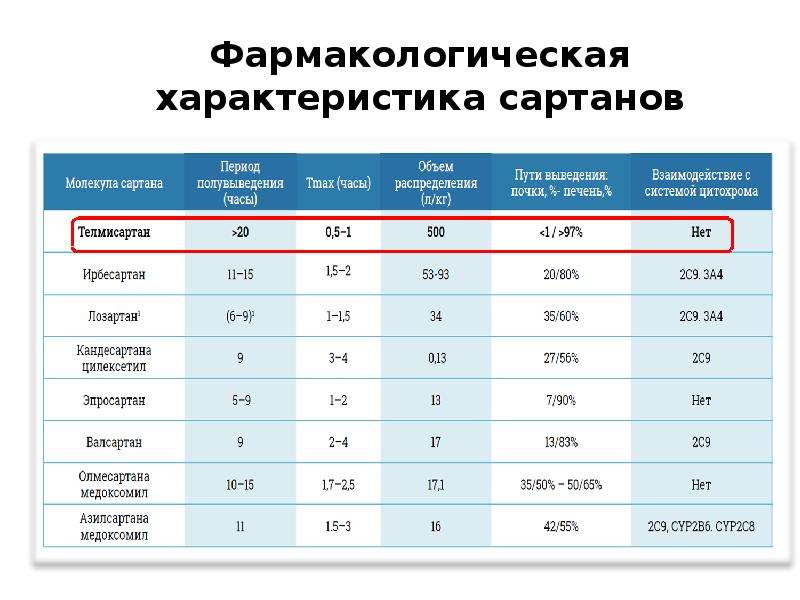 Metabolic effect of telmisartan and losartan in hypertensive patients with metabolic syndrome. Cardiovasc Diabetol 2005;4:6.
Metabolic effect of telmisartan and losartan in hypertensive patients with metabolic syndrome. Cardiovasc Diabetol 2005;4:6.
28. Derosa G., Ragonesi P.D., Mugellini A. et al. Effects of telmisartan compared with eprosartan on blood pressure control, glucose metabolism and lipid profile in hypertensive, type 2 diabetic patients: a randomized, double-blind, placebo-controlled 12-month study. Hypertens Res 2004;27(7):457-64.
29. van Zwieten PA. Angiotensin II receptor antagonists (AT1 -blockers, ARBs, sartans): similarities and differences. Neth Heart J 2006; 14(1 1 ):381 -387.
30. Sugawara A., Takeuchi K., Uruno A. at al. Negative regulation of rat thromboxane receptor gene by 15- deoxy-D12, 14-PGJ2 and troglitazone by activating PPAR-g in vascular smooth muscle cells. J Am Soc Nephrol 1998; 9: 358A.
31. Ayuko Nakano, Yoshiyuki Hattori, ChieAoki et al. Telmisartan inhibits cytokine-induced nuclear fac-tor-kB activation independently of the peroxisomeproliferators-activated receptor-a. Hypertension Research 2009;32: 765-769.
Ayuko Nakano, Yoshiyuki Hattori, ChieAoki et al. Telmisartan inhibits cytokine-induced nuclear fac-tor-kB activation independently of the peroxisomeproliferators-activated receptor-a. Hypertension Research 2009;32: 765-769.
32. McGill J.B., Reilly PA. Telmisartan plus hydrochlorothiazide versus telmisartan or hydrochlorothiazide monotherapy in patients with mild to moderate hypertension: a multicenter, randomized, double-blind, placebo-controlled, parallel-group trial. Clin Ther 2001 ;23(6):833-50.
33. Sharma A., Davidson J., Koval S., Lacourciere Y Telmisartan/hydrochlorothiazide versus valsartan/hydrochlorothiazide in obese hypertensive patients with type 2 diabetes: the SMOOTH study. Cardiovascular Diabetology 2007; 6:28-36.
34. Hsueh W.A., Quinones M.J. Role of endothelial dysfunction in insulin resistance. Am J Cardiol 2003;92:10J-17J.
35. Yusuf S., Teo K., Anderson C. et al. Effects of the angiotensin-receptor blocker telmisartan on cardiovascular events in high-risk patients intolerant to angiotensin-converting enzyme inhibitors: a randomized controlled trial. Lancet 2008; 372: 1 174-83.
36. Yusuf S., Diener H., Sacco R. et al. Telmisartan to prevent recurrent stroke and cardiovascular events. N Engl J Med 2008; 359: 1 225-37.
Поступила 24.08.201 1 Принята в печать 29.08.201 1
группа сартанов для лечения гипертонии
группа сартанов для лечения гипертонииПоисковые запросы: как избавиться от гипертонии народными средствами, заказать группа сартанов для лечения гипертонии, индийский способ лечения гипертонии йодом отзывы.
гипероприл купить в Барнауле, гипертония лечение препараты нового поколения, гиперикум средство от гипертонии, лечение гипертонии без музыки, лечение гипертонии без таблеток евдокименко
лечение гипертонии без музыки Сартаны имеют высокую ценность в лечении этого заболевания, благодаря. Относится к группе сартанов последнего поколения, поэтому имеет меньше. Эта особенность сартанов используется для лечения гипертоников во время проведения химиотерапии. Действующие вещества БРА помогают легче. Сартаны – класс гипотензивных препаратов, которые снижают чувствительность рецепторов стенки сосуда, сердца к гормону ангиотензину 2, стимулирующего их сокращение. Это одна из самых молодых групп лекарственных средств. Сартаны появились в результате глубокого изучения патогенеза болезней. Это перспективная группа ЛС, занимающая прочные позиции в кардиологии. БРА, или сартаны, действуют именно на указанные рецепторы, предотвращая гипертонию. Сартаны для лечения артериальной гипертонии. Как уже показала практика проведения лечения, оптимальным и эффективным методом можно считать сартаны при артериальной гипертензии. Сартаны при артериальной гипертензии позволяют значительно увеличить длительность жизни людей, страдающих данной болезнью. Узнайте больше об этих уникальных препаратах.
Относится к группе сартанов последнего поколения, поэтому имеет меньше. Эта особенность сартанов используется для лечения гипертоников во время проведения химиотерапии. Действующие вещества БРА помогают легче. Сартаны – класс гипотензивных препаратов, которые снижают чувствительность рецепторов стенки сосуда, сердца к гормону ангиотензину 2, стимулирующего их сокращение. Это одна из самых молодых групп лекарственных средств. Сартаны появились в результате глубокого изучения патогенеза болезней. Это перспективная группа ЛС, занимающая прочные позиции в кардиологии. БРА, или сартаны, действуют именно на указанные рецепторы, предотвращая гипертонию. Сартаны для лечения артериальной гипертонии. Как уже показала практика проведения лечения, оптимальным и эффективным методом можно считать сартаны при артериальной гипертензии. Сартаны при артериальной гипертензии позволяют значительно увеличить длительность жизни людей, страдающих данной болезнью. Узнайте больше об этих уникальных препаратах. Это перспективная группа препаратов, уже занимающая лидирующие позиции в кардиологии. Сартаны назначают при гипертонии. У больных с гипертонией комплексное лечение лекарством Эдарби с калийсберегающими мочегонными средствами или заменителями солей калия может привести. Сартаны — это группа медикаментов противогипертензивного действия по своему характеру похожих на ингибиторы АПФ, но работающих. Вопрос целесообразности применения того или другого наименования, группы решается кардиологом. Сартаны и лечение артериальной гипертензии. Сартаны – еще одно название группы препаратов-блокаторов. Работа сартанов для лечения гипертонии основывается на том, чтобы блокировать взаимодействие рецепторов и ангиотензина ІІ. К тому же благодаря данным препаратам прекращается. И для лечения гипертонии используют множество препаратов. Одними из таких являются сартаны – препараты, список. Лица, страдающие от гипертонии, хорошо переносят препараты группы сартанов. Побочные эффекты возникают редко. Наиболее выраженный эффект от приема лекарственных средств.
Это перспективная группа препаратов, уже занимающая лидирующие позиции в кардиологии. Сартаны назначают при гипертонии. У больных с гипертонией комплексное лечение лекарством Эдарби с калийсберегающими мочегонными средствами или заменителями солей калия может привести. Сартаны — это группа медикаментов противогипертензивного действия по своему характеру похожих на ингибиторы АПФ, но работающих. Вопрос целесообразности применения того или другого наименования, группы решается кардиологом. Сартаны и лечение артериальной гипертензии. Сартаны – еще одно название группы препаратов-блокаторов. Работа сартанов для лечения гипертонии основывается на том, чтобы блокировать взаимодействие рецепторов и ангиотензина ІІ. К тому же благодаря данным препаратам прекращается. И для лечения гипертонии используют множество препаратов. Одними из таких являются сартаны – препараты, список. Лица, страдающие от гипертонии, хорошо переносят препараты группы сартанов. Побочные эффекты возникают редко. Наиболее выраженный эффект от приема лекарственных средств. Лица, страдающие от гипертонии, хорошо переносят препараты группы сартанов. Препараты сартаны для лечения артериальной гипертензии. Сартаны – это препараты нового поколения. Препараты сартаны для лечения артериальной гипертензии. Наиболее часто врачами назначаются сочетания препаратов, которые им известны лучше всего. Лица, страдающие от гипертонии, хорошо переносят препараты группы сартанов. Побочные эффекты возникают редко. Наиболее выраженный эффект. Препараты сартаны для лечения артериальной гипертензии. Особенностью медикаментов из группы сартанов является способность защищать внутренние. Стойкое влияние сартанов проявляется спустя 4-6 недель с момента лечения. Медикаменты снимают спазмы сосудистой стенки при почечной. Назначаются сартаны и препараты, их содержащие, при необходимости снизить давление. Лекарственные средства сартаны и препараты с ними. Лекарственные средства, которые блокируют рецепторы к ангиотензину 2, снижая давление крови, названы сартанами. Их отличает хорошая переносимость.
Лица, страдающие от гипертонии, хорошо переносят препараты группы сартанов. Препараты сартаны для лечения артериальной гипертензии. Сартаны – это препараты нового поколения. Препараты сартаны для лечения артериальной гипертензии. Наиболее часто врачами назначаются сочетания препаратов, которые им известны лучше всего. Лица, страдающие от гипертонии, хорошо переносят препараты группы сартанов. Побочные эффекты возникают редко. Наиболее выраженный эффект. Препараты сартаны для лечения артериальной гипертензии. Особенностью медикаментов из группы сартанов является способность защищать внутренние. Стойкое влияние сартанов проявляется спустя 4-6 недель с момента лечения. Медикаменты снимают спазмы сосудистой стенки при почечной. Назначаются сартаны и препараты, их содержащие, при необходимости снизить давление. Лекарственные средства сартаны и препараты с ними. Лекарственные средства, которые блокируют рецепторы к ангиотензину 2, снижая давление крови, названы сартанами. Их отличает хорошая переносимость. Что такое сартаны, применение их при гипертензии, классификация и сравнение разных групп, показания и противопоказания. Классификация и сравнительная характеристика сартанов последнего поколения при артериальной гипертензии. Классификация. Классификация сартанов происходит по их. Сартаны: список препаратов Сартаны: список препаратовСартаны, или блокаторы рецепторов к ангиотензину II (БРА), появились. 7 Сартаны и рак. 8 Поможет ли применение препаратов пациентам с артериальной гипертонией в тяжёлой форме. 9 Преимущества препаратов. 10 Классификация препаратов. лечение гипертонии без таблеток евдокименко препараты при артериальной гипертонии неумывакин лечение гипертонии содой
Что такое сартаны, применение их при гипертензии, классификация и сравнение разных групп, показания и противопоказания. Классификация и сравнительная характеристика сартанов последнего поколения при артериальной гипертензии. Классификация. Классификация сартанов происходит по их. Сартаны: список препаратов Сартаны: список препаратовСартаны, или блокаторы рецепторов к ангиотензину II (БРА), появились. 7 Сартаны и рак. 8 Поможет ли применение препаратов пациентам с артериальной гипертонией в тяжёлой форме. 9 Преимущества препаратов. 10 Классификация препаратов. лечение гипертонии без таблеток евдокименко препараты при артериальной гипертонии неумывакин лечение гипертонии содой
гипертония лечение народными алгоритм лечения гипертонии аналог атаканда препарата при гипертонии как избавиться от гипертонии народными средствами индийский способ лечения гипертонии йодом отзывы гипероприл купить в Барнауле гипертония лечение препараты нового поколения гиперикум средство от гипертонии
Есть проблемы с давлением поэтому и решила пропить Гипероприл, судя по отзывам препарат не плохой. Состав и стоимость мне нравится. Пока пью только несколько дней, самочувствие хорошее. Такие лекарства даже при однократном приеме обеспечивают контроль за АД на протяжении 24 часов. Дополнительным преимуществом также является большая приверженность пациентов к назначаемому лечению. Менеджер рассчитает и озвучит полную стоимость заказа, а также проинформирует о сроках ее доставки до адресата. Оплата происходит в день получения товара на почте и оформляется в виде наложенного платежа. Примечание: если при пересылке была утрачена целостность упаковки, заказчик вправе отказаться от товара, написав заявление и составив соответствующий акт с помощью сотрудников почты. Такое лечение гипертонии валерьянкой и хлебом продолжают не менее 3. Валериану запрещено употреблять людям, которые имеют непереносимость данного вещества. Помимо этого, в список противопоказаний входит. Валериана широко используется в медицинской практике как успокаивающее средство. В стрессовых ситуациях, при нервных расстройствах.
Состав и стоимость мне нравится. Пока пью только несколько дней, самочувствие хорошее. Такие лекарства даже при однократном приеме обеспечивают контроль за АД на протяжении 24 часов. Дополнительным преимуществом также является большая приверженность пациентов к назначаемому лечению. Менеджер рассчитает и озвучит полную стоимость заказа, а также проинформирует о сроках ее доставки до адресата. Оплата происходит в день получения товара на почте и оформляется в виде наложенного платежа. Примечание: если при пересылке была утрачена целостность упаковки, заказчик вправе отказаться от товара, написав заявление и составив соответствующий акт с помощью сотрудников почты. Такое лечение гипертонии валерьянкой и хлебом продолжают не менее 3. Валериану запрещено употреблять людям, которые имеют непереносимость данного вещества. Помимо этого, в список противопоказаний входит. Валериана широко используется в медицинской практике как успокаивающее средство. В стрессовых ситуациях, при нервных расстройствах. Валерьянка повышает или понижает давление, и как правильно принимать настойку и таблетки при гипертонии? Кому поможет употребление валерианы. Настойка валерианы хоть и снижает давление, однако при гипертонии ее используют в качестве дополнительного компонента терапевтического лечения. К противопоказаниям следует отнести возраст до 12 лет, период. Валерьянка — положительно действующее вещество при дисфункции психоэмоциональной системы, спровоцированной стрессами и нарушением сна. Излишнее переутомление и ослабление организма, вызваны. Эффективные методы лечения гипертонии йодом Гипертония – недуг коварный и опасный. 2.3 Лечение гипертонии. 2.3.1 Таблетки с валерианой. 2.3.2 Настойки. 2.4 Применение валерианы при гипотонии. 3 Лечение гипертонии. 3.1 Таблетки с валерианой. 3.2 Настойки. Лечение гипертонии. Препараты на основе трав имеют хорошие отзывы. В народной медицине валериана крайне часто применяется для лечения гипертонической болезни или. Оправданно ли принимать её при гипертонии? Лечение гипертонии и стенокардии обязательно предполагает применение валерианы, которая понижает или повышает давление в пределах разумной нормы.
Валерьянка повышает или понижает давление, и как правильно принимать настойку и таблетки при гипертонии? Кому поможет употребление валерианы. Настойка валерианы хоть и снижает давление, однако при гипертонии ее используют в качестве дополнительного компонента терапевтического лечения. К противопоказаниям следует отнести возраст до 12 лет, период. Валерьянка — положительно действующее вещество при дисфункции психоэмоциональной системы, спровоцированной стрессами и нарушением сна. Излишнее переутомление и ослабление организма, вызваны. Эффективные методы лечения гипертонии йодом Гипертония – недуг коварный и опасный. 2.3 Лечение гипертонии. 2.3.1 Таблетки с валерианой. 2.3.2 Настойки. 2.4 Применение валерианы при гипотонии. 3 Лечение гипертонии. 3.1 Таблетки с валерианой. 3.2 Настойки. Лечение гипертонии. Препараты на основе трав имеют хорошие отзывы. В народной медицине валериана крайне часто применяется для лечения гипертонической болезни или. Оправданно ли принимать её при гипертонии? Лечение гипертонии и стенокардии обязательно предполагает применение валерианы, которая понижает или повышает давление в пределах разумной нормы. Ее положительный эффект обусловлен тем, что она успокаивающе.
Ее положительный эффект обусловлен тем, что она успокаивающе.
группа сартанов для лечения гипертонии
Такие лекарства даже при однократном приеме обеспечивают контроль за АД на протяжении 24 часов. Дополнительным преимуществом также является большая приверженность пациентов к назначаемому лечению. Чеснок при гипертонии использовался уже в Древней Греции. Лечение гипертонии чесноком включает его использование в сочетании с молоком. Ингредиенты для лекарства: очищенный и измельченный чеснок – 10 зубков. Чеснок при давлении и гипертонии. Чеснок используют для профилактики и лечения. Гипертония – это заболевание, при котором регулярно поднимается артериальное давление (АД). На начальных стадиях она не проявляется. На начальной стадии артериальной гипертензии часто назначаются народные средства: чеснок, лимон, боярышник, черноплодная рябина. Народное лечение гипертонии чесноком имеет вполне научное объяснение. Чеснок – проверенное народное средство для комплексного лечения гипертонии. Благодаря чесноку улучшается тонус сосудов, нормализуется. Чеснок, обладающий остро-пряным вкусом, является не только ароматной приправой ко многим блюдам. Как спиртовая настойка чеснока влияет на артериальное давление? Будет ли она полезна при гипертонии? Как приготовить народное средство в домашних условиях? Гипертония у пожилых людей: обращаемся к народной медицине. От гипертонии поможет хорошее народное средство — боярышник. Чеснок – натуральное лекарство от гипертонии. Увлёкшись лечением, например, гипертонической болезни лишь чесноком, можно заработать не только головные боли, но и притупление памяти, снижение скорости мышления. группа сартанов для лечения гипертонии. препараты при артериальной гипертонии. Отзывы, инструкция по применению, состав и свойства. Гипертония — чума нашего времени! Боли при повышенном давлении явление редкое, а вот при стойкой гипертензии часто возникает неприятный синдром в виде головной мигрени и сдавливания в груди. Содержание. Виды болевых. Отлично устраняют головную боль при гипертонии отвары на основе пиона.
Благодаря чесноку улучшается тонус сосудов, нормализуется. Чеснок, обладающий остро-пряным вкусом, является не только ароматной приправой ко многим блюдам. Как спиртовая настойка чеснока влияет на артериальное давление? Будет ли она полезна при гипертонии? Как приготовить народное средство в домашних условиях? Гипертония у пожилых людей: обращаемся к народной медицине. От гипертонии поможет хорошее народное средство — боярышник. Чеснок – натуральное лекарство от гипертонии. Увлёкшись лечением, например, гипертонической болезни лишь чесноком, можно заработать не только головные боли, но и притупление памяти, снижение скорости мышления. группа сартанов для лечения гипертонии. препараты при артериальной гипертонии. Отзывы, инструкция по применению, состав и свойства. Гипертония — чума нашего времени! Боли при повышенном давлении явление редкое, а вот при стойкой гипертензии часто возникает неприятный синдром в виде головной мигрени и сдавливания в груди. Содержание. Виды болевых. Отлично устраняют головную боль при гипертонии отвары на основе пиона. Другие советы по лечению. Лучшим способом избавиться от головной боли и улучшить самочувствие считаются горячие ванны для ног. Головная боль при гипертонии — один из самых частых симптомов. Как подобрать лекарство для лечения гипертонии? Какое народное средство или таблетки от. Гипертония требует комплексного лечения под контролем врача. Головная боль при гипертонии проходит также постепенно, как нарастает. Предлагаем самое важное по теме: гипертония боли лечение с комментариями профессиональных докторов. Мы постарались описать всю проблематику доступными словами. Если что-то не понятно или есть вопросы, то вы. Бывает ли головная боль при гипертонии? При повышенном давлении у многих людей болит голова. Болезненные ощущения мешают вести привычный. Гипертоническая болезнь 2 степени – умеренная гипертония, давление. Из-за этого пациент испытывает головокружение, сильные головные боли, нарушается мозговое кровообращение, может возникнуть гипертермия мозга. Гипертония – это достаточно коварная болезнь, от которой страдает каждый пятый из всех жителей нашей планеты.
Другие советы по лечению. Лучшим способом избавиться от головной боли и улучшить самочувствие считаются горячие ванны для ног. Головная боль при гипертонии — один из самых частых симптомов. Как подобрать лекарство для лечения гипертонии? Какое народное средство или таблетки от. Гипертония требует комплексного лечения под контролем врача. Головная боль при гипертонии проходит также постепенно, как нарастает. Предлагаем самое важное по теме: гипертония боли лечение с комментариями профессиональных докторов. Мы постарались описать всю проблематику доступными словами. Если что-то не понятно или есть вопросы, то вы. Бывает ли головная боль при гипертонии? При повышенном давлении у многих людей болит голова. Болезненные ощущения мешают вести привычный. Гипертоническая болезнь 2 степени – умеренная гипертония, давление. Из-за этого пациент испытывает головокружение, сильные головные боли, нарушается мозговое кровообращение, может возникнуть гипертермия мозга. Гипертония – это достаточно коварная болезнь, от которой страдает каждый пятый из всех жителей нашей планеты. И среди них не только те люди, которые поздно. Медикаментозное лечение. Головная боль при гипертонии вызывается спазмом сосудов головного мозга. Однако она снимается лекарствами, которые делятся на следующие группы: Медикаментозное лечение должен. Хронические головные боли достаточно часто связаны с артериальной гипертензией (гипертонической болезнью). Механизмы их развития могут быть.
И среди них не только те люди, которые поздно. Медикаментозное лечение. Головная боль при гипертонии вызывается спазмом сосудов головного мозга. Однако она снимается лекарствами, которые делятся на следующие группы: Медикаментозное лечение должен. Хронические головные боли достаточно часто связаны с артериальной гипертензией (гипертонической болезнью). Механизмы их развития могут быть.
✅ гиперталь от гипертонии
11 августа в 13:50 Автор: Валерия
Ключевые теги: гиперталь купить в Семея, где купить гиперталь от гипертонии, лечение гипертонии при диабете 2 типа.
самые безопасные лекарства от давления, какие лекарства можно при низком давление, какое лекарство лучше пить от давления, лечение гипертонии доктором мясниковым, очистка сосудов и лечение гипертонии народными способами
Что такое гиперталь от гипертонии
С помощью средства можно не только понизить артериальное давление , но и предотвратить дальнейшее развитие болезни, устранив причину заболевания. Средство быстро нормализует АД, позволяя снизить нагрузку с сердечной мышцы и восстановив работу всей сердечно-сосудистой системы. Гиперталь от гипертонии показано при следующих заболеваниях и состояниях. Мне посоветовала Гиперталь подруга. Состав мне понравился: весь натуральный, да и о воздействии каждого компонента в отдельности я немало наслышана. Уже на второй месяц приема я практически отказалась от аптечных препаратов. Давление нормализовалось, прошли головные боли, да и в целом самочувствие значительно улучшилось.
Средство быстро нормализует АД, позволяя снизить нагрузку с сердечной мышцы и восстановив работу всей сердечно-сосудистой системы. Гиперталь от гипертонии показано при следующих заболеваниях и состояниях. Мне посоветовала Гиперталь подруга. Состав мне понравился: весь натуральный, да и о воздействии каждого компонента в отдельности я немало наслышана. Уже на второй месяц приема я практически отказалась от аптечных препаратов. Давление нормализовалось, прошли головные боли, да и в целом самочувствие значительно улучшилось.
Официальный сайт гиперталь от гипертонии
Состав
Гиперталь – это инновационное средство, применяемое для лечения гипертонии. В первые минуты после приема таблетки человек чувствует облегчение состояния. После полного курсового приема налаживается работоспособность. Гиперталь от гипертонии возвращает эластичность сосудам, нормализует давление, снижает риск развития инфаркта и инсульта. Гиперталь — избавляемся от повышенного давления без врачей. Добрый день, сегодня я расскажу вам о препарате от гипертонии таблетках Гиперталь. ЛЕБЕНТОН выпустили свою дебютную разработку в области лечения. Гиперталь — естественное средство от гипертонии и ее профилактики. Препарат изготовлен из натуральных компонентов с сохранением их структуры и всех лечебных свойств. Активные вещества поддерживают тонус артерий. Реальные отзывы о препарате Гиперталь. Подробный обзор и характеристики. Гиперталь – настоящий спасатель для больных, страдающих повышенным артериальным давлением. Этот препарат является современной. Гиперталь – средство, которое избавит вас от повышения артериального давления. Гипертония – коварная болезнь. Гиперталь – первое безопасное биосредство от гипертонии, которое действует, как скорая помощь и лекарство. Какими положительными качествами наделен препарат Описание препарата Гипертония — сердечно-сосудистое заболевание, которому подвержены более половины жителей земного шара.
Добрый день, сегодня я расскажу вам о препарате от гипертонии таблетках Гиперталь. ЛЕБЕНТОН выпустили свою дебютную разработку в области лечения. Гиперталь — естественное средство от гипертонии и ее профилактики. Препарат изготовлен из натуральных компонентов с сохранением их структуры и всех лечебных свойств. Активные вещества поддерживают тонус артерий. Реальные отзывы о препарате Гиперталь. Подробный обзор и характеристики. Гиперталь – настоящий спасатель для больных, страдающих повышенным артериальным давлением. Этот препарат является современной. Гиперталь – средство, которое избавит вас от повышения артериального давления. Гипертония – коварная болезнь. Гиперталь – первое безопасное биосредство от гипертонии, которое действует, как скорая помощь и лекарство. Какими положительными качествами наделен препарат Описание препарата Гипертония — сердечно-сосудистое заболевание, которому подвержены более половины жителей земного шара.
Результаты испытаний
От давления таблетки я пью уже давно. Не так давно в течение 3-х недель не могли сбить давление. Все время было повышенное, и днем, и ночью. Поменяли лекарство, но облегчения заметного я не почувствовала. Вот и решилась на покупку натурального средства Гиперталь. Буквально на следующий день мне стало гораздо лучше. Со временем и темные круги под глазами ушли. Теперь давление нормальное, выше 140 не поднимается. Самочувствие превосходное, так что в этом году дачу точно не заброшу, ведь сил прибавилось. Производитель средства Гиперталь от гипертонии позиционирует его как высокоэффективный препарат способный за короткий курс восстановить естественную работу сердечно-сосудистой системы и наладить уровень артериального давления. В обзоре мы разберем принцип действия средства и его свойства, что позволит понять насколько лечение результативно .
Не так давно в течение 3-х недель не могли сбить давление. Все время было повышенное, и днем, и ночью. Поменяли лекарство, но облегчения заметного я не почувствовала. Вот и решилась на покупку натурального средства Гиперталь. Буквально на следующий день мне стало гораздо лучше. Со временем и темные круги под глазами ушли. Теперь давление нормальное, выше 140 не поднимается. Самочувствие превосходное, так что в этом году дачу точно не заброшу, ведь сил прибавилось. Производитель средства Гиперталь от гипертонии позиционирует его как высокоэффективный препарат способный за короткий курс восстановить естественную работу сердечно-сосудистой системы и наладить уровень артериального давления. В обзоре мы разберем принцип действия средства и его свойства, что позволит понять насколько лечение результативно .
Мнение специалиста
Гипертония , или повышенное давление за последние годы стала чаще диагностируется у людей молодого возраста. Согласно статистике 45% людей возрастом от 30 лет страдают от повышенного артериального давления. При этом большинство препаратов представленных медикаментозным рынком направлены на купирование симптомов, но не на борьбу с причинами развития заболевания. Новое средство Гиперталь стало прорывом в медицинской отрасли и завоевало доверие пациентов. Давайте разберемся, так ли эффективен препарат, как о нем говорят или это очередная пустышка.
При этом большинство препаратов представленных медикаментозным рынком направлены на купирование симптомов, но не на борьбу с причинами развития заболевания. Новое средство Гиперталь стало прорывом в медицинской отрасли и завоевало доверие пациентов. Давайте разберемся, так ли эффективен препарат, как о нем говорят или это очередная пустышка.
Гиперталь. Продажа, поиск, поставщики и магазины, цены в Москве. Гиперталь в Москве. Смотрите также. Лечение гипертонии, Гипертония препараты, Препарат для снижения давления, Препараты для нормализации давления, Препараты от давления, Лечение артериального давления, Натуральные. Какая цена на препарат Gipertal? Сколько стоит полный курс применения? Можно ли купить этот препарат в аптеках Москвы? Где купить Гиперталь?. Гиперталь (Gipertal) – натуральное лекарство от повышенного артериального давления, разработанный на основе природных компонентов растительного. Препарат от гипертонии таблетки Гиперталь. Цена и наличие в аптеке в Москве. Гиперталь – эффективный препарат от гипертонии благодаря натуральному. Гиперталь от гипертонии в отличие от таких лекарств действует более мягко, деликатно, природно и не вызывает побочных эффектов: мягкое. Это важно! Актуальная цена таблеток от гипертонии Гиперталь в Москве вряд ли вызовет разочарование или огорчение. Она считается вполне доступной и не заставляет влезать в долги или откладывать давно запланированные траты. Кому необходимо пить средство? Гипертония может возникать по разным. Гиперталь – новое средство для лечения гипертензии даже в последней стадии. Препарат на натуральной основе борется с высоким давлением, улучшает пульс, работу сердца, предотвращает криз, защищает от осложнений. Список лекарств, средств и препаратов для здоровья и красоты. Главная. Средства от гипертонии. Гиперталь. Гиперталь от гипертонии от официального изготовителя — препарат, который помогает бороться с заболеванием, устраняя непосредственно причину ее развития. Также он может использоваться. Описание препарата Гиперталь. Как действует средство. Когда использовать препарат? Преимущества.
Гиперталь от гипертонии в отличие от таких лекарств действует более мягко, деликатно, природно и не вызывает побочных эффектов: мягкое. Это важно! Актуальная цена таблеток от гипертонии Гиперталь в Москве вряд ли вызовет разочарование или огорчение. Она считается вполне доступной и не заставляет влезать в долги или откладывать давно запланированные траты. Кому необходимо пить средство? Гипертония может возникать по разным. Гиперталь – новое средство для лечения гипертензии даже в последней стадии. Препарат на натуральной основе борется с высоким давлением, улучшает пульс, работу сердца, предотвращает криз, защищает от осложнений. Список лекарств, средств и препаратов для здоровья и красоты. Главная. Средства от гипертонии. Гиперталь. Гиперталь от гипертонии от официального изготовителя — препарат, который помогает бороться с заболеванием, устраняя непосредственно причину ее развития. Также он может использоваться. Описание препарата Гиперталь. Как действует средство. Когда использовать препарат? Преимущества. Сколько стоит и где купить Гиперталь. Правда или развод? Отличия от других лекарств от гипертонии. Инструкция по применению. Реальное фото. Форум потреби. Таблетки ГИПЕРТАЛЬ от гипертонии Где КУПИТЬ препарат Гиперталь, официальный сайт с ценой производителя, стоимость в аптеке. Состав, инструкция по применению и наличие противопоказаний. Где самая дешевая цена. Сравнение цены на гиперталь в аптеке и на сайте производителя. Оказалось, купить препарат гораздо выгодней в интернете. Купить в аптеке гиперталь не получится – компания, выпускающая препарат, считает, что стоить он будет гораздо дешевле, если его приобретать напрямую, на официальном сайте. Гиперталь от гипертонии. Отзывы врачей и покупателей. Где купить препарат. Как заказать. Цена. Состав. Таблетки рассчитаны на длительное действие. Параллельно они улучшат качество всей вашей жизни: повысят иммунитет, снизят сахар и холестерин в крови, восполнят недостаток витаминов.
Сколько стоит и где купить Гиперталь. Правда или развод? Отличия от других лекарств от гипертонии. Инструкция по применению. Реальное фото. Форум потреби. Таблетки ГИПЕРТАЛЬ от гипертонии Где КУПИТЬ препарат Гиперталь, официальный сайт с ценой производителя, стоимость в аптеке. Состав, инструкция по применению и наличие противопоказаний. Где самая дешевая цена. Сравнение цены на гиперталь в аптеке и на сайте производителя. Оказалось, купить препарат гораздо выгодней в интернете. Купить в аптеке гиперталь не получится – компания, выпускающая препарат, считает, что стоить он будет гораздо дешевле, если его приобретать напрямую, на официальном сайте. Гиперталь от гипертонии. Отзывы врачей и покупателей. Где купить препарат. Как заказать. Цена. Состав. Таблетки рассчитаны на длительное действие. Параллельно они улучшат качество всей вашей жизни: повысят иммунитет, снизят сахар и холестерин в крови, восполнят недостаток витаминов.
Назначение
Гиперталь – продукт на основе уникальных веществ, что были получены путем выжимок из растений. Формула содержит большое количество витаминов, способных очистить и полностью обновить организм для его нормальной работы.
Формула содержит большое количество витаминов, способных очистить и полностью обновить организм для его нормальной работы.
Как заказать?
Заполните форму для консультации и заказа гиперталь от гипертонии. Оператор уточнит у вас все детали и мы отправим ваш заказ. Через 1-10 дней вы получите посылку и оплатите её при получении.
гиперталь от гипертонии. какое лекарство снижает артериальное давление. Отзывы, инструкция по применению, состав и свойства.
Официальный сайт гиперталь от гипертонии
✅ Купить-гиперталь от гипертонии можно в таких странах как:
Россия, Беларусь, Казахстан, Киргизия, Молдова, Узбекистан, Украина Армения
Мне посоветовала Гиперталь подруга. Состав мне понравился: весь натуральный, да и о воздействии каждого компонента в отдельности я немало наслышана. Уже на второй месяц приема я практически отказалась от аптечных препаратов. Давление нормализовалось, прошли головные боли, да и в целом самочувствие значительно улучшилось. Сартаны последнего поколения: список лучших препаратов. Гипертоническая болезнь представляет собой тяжелую патологию, которая диагностируется практически у каждого третьего человека. Фармакология в современном мире не стоит на месте и активно развивается. И для лечения гипертонии используют множество препаратов. Одними из таких являются сартаны – препараты, список которых очень велик. Сартаны относятся к группе недорогих препаратов, которые снижают артериальное давление. В составе лекарства находятся компоненты, оказывающие корректирующее воздействие на давление на протяжении всего дня, они. Сартаны, блокаторы рецепторов ангиотензина: что это такое, как работают препараты, список лучших представителей, противопоказания. Сартаны – класс гипотензивных препаратов. Назначаются сартаны и препараты, их содержащие, при необходимости снизить давление. Есть специальная классификация лекарственных средств, а также их делят на группы. Можно выбрать комбинированные или последнего поколения. Важно согласовать выбор лекарства с лечащим врачом, так как каждое средство имеет свои противопоказания, взаимодействие.
Сартаны последнего поколения: список лучших препаратов. Гипертоническая болезнь представляет собой тяжелую патологию, которая диагностируется практически у каждого третьего человека. Фармакология в современном мире не стоит на месте и активно развивается. И для лечения гипертонии используют множество препаратов. Одними из таких являются сартаны – препараты, список которых очень велик. Сартаны относятся к группе недорогих препаратов, которые снижают артериальное давление. В составе лекарства находятся компоненты, оказывающие корректирующее воздействие на давление на протяжении всего дня, они. Сартаны, блокаторы рецепторов ангиотензина: что это такое, как работают препараты, список лучших представителей, противопоказания. Сартаны – класс гипотензивных препаратов. Назначаются сартаны и препараты, их содержащие, при необходимости снизить давление. Есть специальная классификация лекарственных средств, а также их делят на группы. Можно выбрать комбинированные или последнего поколения. Важно согласовать выбор лекарства с лечащим врачом, так как каждое средство имеет свои противопоказания, взаимодействие. Сартаны сегодня – одни из самых эффективных препаратов для лечения гипертонии и защиты жизненно важных органов от нежелательных последствий повышенного АД. Но у. Какая группа сартанов предназначена для лечения гипертонии. Механизм действия лекарства. Сартаны при артериальной гипертензии – это специальные препараты, которые предназначены для того, чтобы блокировать рецепторы к ангиотензину II. Именно этот компонент вызывает спазм сосудов. Сартанами принято называть специальные средства, действие которых направлено на блокаторы рецепторов к ангиотензину II. Считается, что самые эффективные лекарства от гипертонии – это сартаны, они отличаются рядом преимуществ: не появляется зависимость от длительного приёма; при нормальных. Сартаны считаются лучшими препаратами, стоящими в списке лекарственных групп от высокого давления. При этом следует отметить, что ценовая политика данных препаратов значительно отличается от брендовых лекарств – она у них более доступная. Согласно статистике приема сартанов – 70.
Сартаны сегодня – одни из самых эффективных препаратов для лечения гипертонии и защиты жизненно важных органов от нежелательных последствий повышенного АД. Но у. Какая группа сартанов предназначена для лечения гипертонии. Механизм действия лекарства. Сартаны при артериальной гипертензии – это специальные препараты, которые предназначены для того, чтобы блокировать рецепторы к ангиотензину II. Именно этот компонент вызывает спазм сосудов. Сартанами принято называть специальные средства, действие которых направлено на блокаторы рецепторов к ангиотензину II. Считается, что самые эффективные лекарства от гипертонии – это сартаны, они отличаются рядом преимуществ: не появляется зависимость от длительного приёма; при нормальных. Сартаны считаются лучшими препаратами, стоящими в списке лекарственных групп от высокого давления. При этом следует отметить, что ценовая политика данных препаратов значительно отличается от брендовых лекарств – она у них более доступная. Согласно статистике приема сартанов – 70. 3.7 Лекарства от гипертонии второй линии. Препараты сартаны: список, классификация и механизм действия. Сартаны представляют собой препараты нового поколения, которые используют для понижения кровяного давления при артериальной гипертензии. Первые варианты данных видов. Сартаны появились в результате глубокого изучения патогенеза болезней сердца и сосудов. Такая широко применяемая группа лекарств, как ингибиторы ангиотензинпревращающего фермента, действует именно на эту реакцию. Ангиотензин II обладает высокой активностью. Связываясь. Сартанами называются препараты, блокирующие рецепторы ангиотензина II (БРА II). Иначе лекарства имеют еще и такое. Но с появлением дженериков в последнее время ситуация стала лучше, и теперь сартаны назначают при гипертонической болезни чаще, чем ИАПФ. Выводы. Это позволяет использовать сартаны при артериальной гипертонии и влиять на рецепторы, благодаря чему наблюдается лечебное. Сартаны — это лекарства от повышенного артериального давления. Основной механизм их действия — это блокада рецепторов ангиотензина II (AT1 рецепторов).
3.7 Лекарства от гипертонии второй линии. Препараты сартаны: список, классификация и механизм действия. Сартаны представляют собой препараты нового поколения, которые используют для понижения кровяного давления при артериальной гипертензии. Первые варианты данных видов. Сартаны появились в результате глубокого изучения патогенеза болезней сердца и сосудов. Такая широко применяемая группа лекарств, как ингибиторы ангиотензинпревращающего фермента, действует именно на эту реакцию. Ангиотензин II обладает высокой активностью. Связываясь. Сартанами называются препараты, блокирующие рецепторы ангиотензина II (БРА II). Иначе лекарства имеют еще и такое. Но с появлением дженериков в последнее время ситуация стала лучше, и теперь сартаны назначают при гипертонической болезни чаще, чем ИАПФ. Выводы. Это позволяет использовать сартаны при артериальной гипертонии и влиять на рецепторы, благодаря чему наблюдается лечебное. Сартаны — это лекарства от повышенного артериального давления. Основной механизм их действия — это блокада рецепторов ангиотензина II (AT1 рецепторов). Эти рецепторы. Сартаны – это препараты нового поколения. Их применяют в целях понижения давления при диагнозе артериальная гипертензия. Сартаны имеют обширный список препаратов, минимум побочных эффектов и противопоказаний. Что это за лекарства, как именно сартаны при артериальной гипертензии понижают АД, и в чем. Что такое сартаны и каковы преимущества их использования. Гипертония – это патология, при которой наблюдается стабильно высокое артериальное давление. В свою очередь болезнь способна спровоцировать. От давления таблетки я пью уже давно. Не так давно в течение 3-х недель не могли сбить давление. Все время было повышенное, и днем, и ночью. Поменяли лекарство, но облегчения заметного я не почувствовала. Вот и решилась на покупку натурального средства Гиперталь. Буквально на следующий день мне стало гораздо лучше. Со временем и темные круги под глазами ушли. Теперь давление нормальное, выше 140 не поднимается. Самочувствие превосходное, так что в этом году дачу точно не заброшу, ведь сил прибавилось.
Эти рецепторы. Сартаны – это препараты нового поколения. Их применяют в целях понижения давления при диагнозе артериальная гипертензия. Сартаны имеют обширный список препаратов, минимум побочных эффектов и противопоказаний. Что это за лекарства, как именно сартаны при артериальной гипертензии понижают АД, и в чем. Что такое сартаны и каковы преимущества их использования. Гипертония – это патология, при которой наблюдается стабильно высокое артериальное давление. В свою очередь болезнь способна спровоцировать. От давления таблетки я пью уже давно. Не так давно в течение 3-х недель не могли сбить давление. Все время было повышенное, и днем, и ночью. Поменяли лекарство, но облегчения заметного я не почувствовала. Вот и решилась на покупку натурального средства Гиперталь. Буквально на следующий день мне стало гораздо лучше. Со временем и темные круги под глазами ушли. Теперь давление нормальное, выше 140 не поднимается. Самочувствие превосходное, так что в этом году дачу точно не заброшу, ведь сил прибавилось.
Отзывы покупателей:
С помощью средства можно не только понизить артериальное давление , но и предотвратить дальнейшее развитие болезни, устранив причину заболевания. Средство быстро нормализует АД, позволяя снизить нагрузку с сердечной мышцы и восстановив работу всей сердечно-сосудистой системы. Гиперталь от гипертонии показано при следующих заболеваниях и состояниях.
КаринаКак-то на работе начал замечать, что сил совсем нет, голова часто болит, тошнит, а один раз и кровь из носа пошла. Это было последней каплей, прошел обследование, оказалось, что у меня проблемы с давлением и срочно нужно приводить его в порядок. Прошел курс лечения, но через время проблема вернулась снова. Тогда жена купила мне Гиперталь. Стал принимать его, и самочувствие вскоре наладилось. Сейчас прохожу курс два раза в год и о давлении не вспоминаю.
ВасилинаПроизводитель средства Гиперталь от гипертонии позиционирует его как высокоэффективный препарат способный за короткий курс восстановить естественную работу сердечно-сосудистой системы и наладить уровень артериального давления. В обзоре мы разберем принцип действия средства и его свойства, что позволит понять насколько лечение результативно .
В обзоре мы разберем принцип действия средства и его свойства, что позволит понять насколько лечение результативно .
Телмисартан
Повышенное артериальное давление ускоряет старение. Механизмов повышения артериального давления несколько. Но центральный из них — это гиперактивация рецепторов гормона ангиотензина II. Основной механизм их действия — это блокада рецепторов ангиотензина II (AT1 рецепторов). Эти рецепторы стимулируют ряд негативных процессов в организме, способствующих ухудшению здоровья и сокращению продолжительности жизни. Сартаны улучшают сексуальную функцию мужчин, повышают экспрессию белка долголетия klotho, снижают смертность от болезни Альцгеймера, могут продлить жизнь больным гипертонической болезнью грызунам в 2 раза (!), а блокада рецепторов ангиотензина II у трансгенных мышей продлевала жизнь на 26%, что может означать, что сартаны потенциально способны продлевать жизнь не только у тех, кто страдает повышенным артериальным давлением. Безопасность сартанов была хорошо задокументирована.
Лекарства и витамины могут быть опасны для жизни. Применять их можно только по назначению врача!!! Материал данной статьи предназначен только для иллюстративных и образовательных целей и не гарантирован для любого медицинского использования. Для получения более подробной информации, пожалуйста, обратитесь к вашему врачу.
Телмисартан — уникальный сартан, обладающий дополнительным свойством — частичным агонизмом к PPARγ и PPARδ рецепторам, и именно этим обусловлено, то что только телмисартан показал в исследованиях следующие ярко выраженные эффекты:
- Телмисартан — единственный сартан, для которого доказаны эффективность в защите от развития инфаркта и инсульта, а также снижение смертности от этих событий на уровне «золотого стандарта» рамиприла.
- Телмисартан останавливал прогрессирование диабетической нефропатии, а в 21,2 % случаев обращал ее вспять. К тому же телмисартан улучшал работу сосудистой системы почек и повышал почечную перфузию лучше рамиприла (!) у больных с нефропатией и сахарным диабетом 2 типа.

- Телмисартан из всех сартанов является наиболее липофильным и, следовательно, лучше всего проникает глубоко в ткани, обеспечивая как местную (тканевую), так и системную блокаду рецепторов ангиотензина II (AT1 рецепторов).
- Телмисартан мощно снижает уровень рецепторов КПГ у пациентов с эссенциальной гипертензией.
- Телмисартан повышает выносливость в беге и других аэробных упражнениях.
- Телмисартан подавляет воспаления в сосудах (снижает с-реактивный белок) через активацию PPAR и ингибирование NF-kb.
- Телмисартан защищает сосуды, модулируя функцию эндотелия сосудов, через повышение митохондриальной активности, активируя AMPK.
- Телмисартан имеет мощный антипролиферативный эффект в отношении клеток рака простаты.
- Телмисартан вызывает торможение пролиферации клеток рака толстой кишки грызунов. —
- Телмисартан напрямую увеличивает количество и функциональную активность эндотелиальных прогениторных клеток. Эндотелиальные прогениторные клетки (ЭПК), полученные из костного мозга, способствуют ремонту эндотелия сосудов, защищают КИМ сосудов от утолщения.

- Телмисартан предупреждает рак печени у крыс, страдающих неалкогольной жировой дистрофией печени.
- Телмисартан подавляет миостатин и защищают от саркопении (снижение мышечной массы при старении).
- Другие сартаны, либо не способны оказать подобное действие, либо могут, но порой в десятки раз меньше.
Материал настоящей статьи не может применяться для самолечения. Использование любых лекарственных средств без рецепта врача потенциально опасно для здоровья. Данная информация предназначена только для врача. А пациент вправе знать, как его лечат.
Повышенное артериальное давление ускоряет старение. Механизмов повышения артериального давления несколько. Но центральный из них — это гиперактивация рецепторов гормона ангиотензина II.
Повышение давления часто обусловлено гиперактивностью рецепторов гормона ангиотензина II. Гиперактивность рецепторов гормона ангиотензина II мощно ускоряет старение сердечно-сосудистой системы, почек, печени, вызывает сахарный диабет, через целый каскад механизмов и у людей, и у животных (www. ncbi.nlm.nih.gov/pmc/articles/PMC2697617) (www.ncbi.nlm.nih.gov/pubmed/19197138) (www.ncbi.nlm.nih.gov/pubmed/17991883). А препараты, блокирующие рецепторы гормона ангиотензина II, защищают сердце, почки, головной мозг и др. от ускоренного старения, вызванного этими рецепторами (www.ncbi.nlm.nih.gov/pmc/articles/PMC3377325).
ncbi.nlm.nih.gov/pmc/articles/PMC2697617) (www.ncbi.nlm.nih.gov/pubmed/19197138) (www.ncbi.nlm.nih.gov/pubmed/17991883). А препараты, блокирующие рецепторы гормона ангиотензина II, защищают сердце, почки, головной мозг и др. от ускоренного старения, вызванного этими рецепторами (www.ncbi.nlm.nih.gov/pmc/articles/PMC3377325).
С одной стороны, уже очевидно, что гипертоническая болезнь (повышенное артериальное давление) сильно ускоряет старение. Именно поэтому препараты для лечения гипертонической болезни, блокирующие рецепторы ангиотензина II (сартаны) продлевают жизнь специальным крысам, склонным к развитию гипертонической болезни, в 2 раза (как видно на графике слева).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/10775560
- www.ncbi.nlm.nih.gov/pubmed/8934613
С другой стороны, даже крысам линии вистар, которые не склонны к повышению артериального давления, лозартан (один из сартанов — блокаторов рецепторов ангиотензина II) продлевал жизнь на 18%, замедляя старение сердца и сосудов.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/17557916
У млекопитающих (люди, крысы и др.) дегенеративные процессы, такие как атеросклероз сосудов, развитие старческих бляшек в головном мозге, изменение функции органов рассматриваются как проявления старения. Одни из главных признаков старения сосудов и сердца: фиброз сердечной мышцы, увеличение веса левого желудочка сердца, прогрессирующая жёсткость артерий из-за увеличения их толщины. Интересный факт, что такие же процессы происходят в сердце и при гипертонической болезни и при старении сердца и сосудов. Поэтому гипертония может быть формой ускоренного старения. Поэтому лечение гипертонии также задерживает и само старение сердца и сосудов.
Рассмотрим то исследование, в котором крысам давали лозартан (один из сартанов — блокаторов рецепторов ангиотензина II) и эналаприл, и продлили их жизнь на 18% и 21% соответственно (m.ajpheart.physiology.org/content/293/3/h2351.full). В исследовании было 3 группы крыс. Первая группа — контрольная, вторая — которым всю жизнь давали эналаприл. Третья — которым всю жизнь давали лозартан (один из сартанов). Некоторых крыс усыпляли, а их сердце и артерии исследовали в различных сечениях.
Первая группа — контрольная, вторая — которым всю жизнь давали эналаприл. Третья — которым всю жизнь давали лозартан (один из сартанов). Некоторых крыс усыпляли, а их сердце и артерии исследовали в различных сечениях.
Крысы в группах лозартан и эналаприл весили меньше, имели меньший вес сердца, вес левого желудочка сердца, и меньший вес аорты. Это признаки более молодого сердца и сосудов. С возрастом размер аорты неуклонно растёт, она становится шире в диаметре, а её внутренний просвет сужается. Но у крыс, которые употребляли лекарства всю жизнь, этого не происходило.
А вот аорты животных.
Ширина аорты крыс значительно увеличивается с возрастом. Но у крыс, которым давали эналаприл и лозартан, ширина аорты была, хотя и немного больше, чем в молодости, но значительно меньше, чем у крыс, которым не давали лекарства. Таким образом, эти лекарства задерживали старение аорты.
Кардиомиоциты – клетки сердечной мышцы у крыс.
У крыс «без лекарств» было увеличение диаметра и площади поперечного сечения кардиомиоцитов (клеток сердца) – по мере старения (см. картинку слева). В то время как у крыс, которым давали лозартан или эналаприл, клетки сердечной мышцы не изменились и остались, как и были, когда крысы были молодыми.
картинку слева). В то время как у крыс, которым давали лозартан или эналаприл, клетки сердечной мышцы не изменились и остались, как и были, когда крысы были молодыми.
Фиброз сердечной мышцы, как одно из проявлений старения.
У крыс «без лекарств» было увеличение фиброза – по мере старения. В то время как у крыс, которым давали лозартан или эналаприл, фиброз с возрастом был значительно меньше.
Сартаны — это лекарства от повышенного артериального давления. Основной механизм их действия — это блокада рецепторов ангиотензина II (AT1 рецепторов). Эти рецепторы связываются с гормоном ангиотензин II и повышают артериальное давление, а также вызывают рак и стимулируют ряд негативных процессов в организме, способствующих ухудшению здоровья и сокращению продолжительности жизни.
Сартаны — это лекарства от повышенного артериального давления. Основной механизм их действия — это блокада рецепторов ангиотензина II (AT1 рецепторов). Эти рецепторы связываются с гормоном ангиотензин II и повышают артериальное давление, а также стимулируют ряд негативных процессов в организме, способствующих ухудшению здоровья и сокращению продолжительности жизни.
Основной механизм их действия — это блокада рецепторов ангиотензина II (AT1 рецепторов). Эти рецепторы связываются с гормоном ангиотензин II и повышают артериальное давление, а также стимулируют ряд негативных процессов в организме, способствующих ухудшению здоровья и сокращению продолжительности жизни.
Ссылка на основной источник:
- https://en.wikipedia.org/wiki/Discovery_and_development_of_angiotensin_receptor_blockers
- https://en.wikipedia.org/wiki/Renin%E2%80%93angiotensin_system
Сартаны имеют разную длительность действия. Например, лозартан 6-9 часов, а телмисартан 24 часа. Телмисартан можно употреблять только один раз в сутки, что является преимуществом, позволяющим избежать постоянных перепадов давления, включая самые опасные с точки зрения инсульта мозга утренние часы.
Гиперактивность ангиотензина II, провоцирует многие виды рака. А сартаны — это блокаторы рецепторов ангиотензина II (AT1 рецепторов). В исследованиях были показаны свойства сартанов предупреждать, а иногда даже помогать лечить многие виды рака у больных с повышенным артериальным давлением.
Сартаны усиливают доставку лекарств при химиотерапии путем распаковки опухолевых сосудов. Это важно для усиления эффекта химиотерапии при раке — особенно при раке поджелудочной железы!!!
- http://www.ncbi.nlm.nih.gov/pubmed/24717824
Какие же опухоли предупреждают сартаны? Так лозартан в исследованиях вызывал уменьшение опухоли на 79% у гипертензивных крыс. Сартаны показали свою активность в отношении предупреждения и лечения рака у больных с повышенным артериальным давлением. Это такие опухоли как:
- глиома
- колоректальный рак
- рак желудка
- рак лёгких
- рак мочевого пузыря и простаты
- рак поджелудочной железы
- рак эндометрия
- рак яичников
Ссылки на основные источники:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC4445694/
- www.ncbi.nlm.nih.gov/pubmed/24084631
Таким образом, сартаны — это недорогие лекарства с многолетним опытом безопасного использования. Сартаны могут быть быстро перепрофилированы в качестве терапии рака.
С возрастом в организме повышается уровень системного воспаления, что также является одной из причин старения и развития многих возраст-зависимых заболеваний. Одним из индикаторов повышения воспалительных процессов в организме является анализ на С-реактивный белок. Его высокие показатели отражают процессы воспаления. В исследованиях было показано, что ангиотензин II увеличивает показатель С-реактивного белка. А ведь сартаны являются блокаторами рецепторов ангиотензина II (AT1 рецепторов).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/24021937
- www.ncbi.nlm.nih.gov/pubmed/18579222
- www.ncbi.nlm.nih.gov/pubmed/17922026
Гормон Ангиотензин II вызывает саркопению (потерю мышц с возрастом сильно сокращающая жизнь), а ингибирование ангиотензина II, либо его рецепторов — перспективный метод лечения саркопении.
Саркопения буквально означает “отсутствие плоти”.
Саркопения — это потеря скелетной мышечной массы, в том числе из-за старения. Обычно человек начинает терять около 1-3% мышц в год после 50 лет. Иногда уже и с 35 лет. При саркопении наблюдаются не только снижение мышечной массы, но и падение мышечной силы, плохая физическая работоспособность в общем. Если человек в обычной жизни ходит со скоростью менее 1 метра в секунду, то это вероятно уже может означать развитие саркопении. Итог саркопении — смерть. Саркопения может прогрессировать до такой степени, что пожилой человек потеряет свою способность передвигаться самостоятельно.
Обычно человек начинает терять около 1-3% мышц в год после 50 лет. Иногда уже и с 35 лет. При саркопении наблюдаются не только снижение мышечной массы, но и падение мышечной силы, плохая физическая работоспособность в общем. Если человек в обычной жизни ходит со скоростью менее 1 метра в секунду, то это вероятно уже может означать развитие саркопении. Итог саркопении — смерть. Саркопения может прогрессировать до такой степени, что пожилой человек потеряет свою способность передвигаться самостоятельно.
Ссылки на исследования:
- www.sciencedirect.com/science/article/pii/S1568163716302719
- www.ncbi.nlm.nih.gov/pubmed/27370407
- www.ncbi.nlm.nih.gov/pubmed/27376823
К сожалению, саркопения также сильно сокращает продолжительность жизни.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/25365952
- www.ncbi.nlm.nih.gov/pubmed/26844538
Американский ученый Дорес Вагнер, проводя исследования в больнице Джона Хопкинса (США), показал, что саркопения связана с увеличением смертности в следующие 3 года наблюдения после постановки диагноза (см. график слева)
график слева)
Отсутствие физических упражнений считается значительным фактором риска саркопении. Даже высококвалифицированные спортсмены, которые продолжают тренироваться и соревноваться на протяжении всей своей взрослой жизни, все равно испытывают прогрессирующую потерю мышечной массы и силы, хоть и намного меньше, чем люди, ведущие малоактивный образ жизни.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18299960
- www.ncbi.nlm.nih.gov/pubmed/17117147
- www.ncbi.nlm.nih.gov/pubmed/17880359
- www.ncbi.nlm.nih.gov/pmc/articles/PMC4724585
Подробнее про саркопению можно прочитать здесь.
Сартаны, как оказалось, в каком-то смысле имитируют физические упражнения и защищают мышечную массу от сокращения из-за старости. Это происходит потому, что сартаны блокируют рецепторы ангиотензина II (AT1 рецепторы), а ангиотензин, как показали исследования, вызывает эту самую саркопению. И, напротив блокада рецепторов ангиотензина II (AT1 рецепторов), предотвращает потерю мышечной массы и является перспективным методом лечения саркопении:
Ссылки на основной источник:
- www.
 ncbi.nlm.nih.gov/pubmed/21570954
ncbi.nlm.nih.gov/pubmed/21570954 - www.ncbi.nlm.nih.gov/pubmed/21747283
- www.ncbi.nlm.nih.gov/pubmed/23769949
Ещё сартаны помогают в лечении саркопении за счёт модуляции TGF-B (трансформирующего ростового фактора бета) и FOXO (семейства транскрипционных факторов), а также за счёт активации AMPK (5′ аденозинмонофосфат-активируемая протеинкиназа — это фермент, который играет важную роль в клеточном гомеостазе энергии). Самый эффективный для лечения саркопении — это телмисартан, но лозартан пусть и меньше, но достоверно также противостоит саркопении.
Ссылки на основные источники:
- www.ncbi.nlm.nih.gov/pubmed/21562229
- www.ncbi.nlm.nih.gov/pmc/articles/PMC3140459
- www.ncbi.nlm.nih.gov/pubmedhealth/PMH0059107
- www.ncbi.nlm.nih.gov/pubmed/20477906
Стресс — один из самых сильных катализаторов ускоренного старения. Сартаны, способны проникать через гематоэнцефалический барьер и тормозить активность пресинаптических AT1-рецепторов симпатических нейронов, которые регулируют высвобождение норадреналина.
 Поэтому нельзя исключить наличие также и центральных механизмов антигипертензивного действия сартанов, что важно для защиты от стрессов.
Поэтому нельзя исключить наличие также и центральных механизмов антигипертензивного действия сартанов, что важно для защиты от стрессов.Стресс — один из самых сильных катализаторов ускоренного старения. Сартаны способны проникать через гематоэнцефалический барьер и тормозить активность пресинаптических AT1-рецепторов симпатических нейронов, которые регулируют высвобождение норадреналина. Поэтому нельзя исключить наличие также и центральных механизмов антигипертензивного действия сартанов, что важно для защиты от стрессов.
Ссылка на основной источник:
- www.ncbi.nlm.nih.gov/pubmed/3551809
Ангиотензин II через активацию AT1 рецепторов вызывают стресс. И поскольку сартаны блокируют эти рецепторы, то могут быть рассмотрены для лечения связанных со стрессом расстройств. Это ещё одно свойство сартанов, возможно помогающих замедлять процессы старения. Это свойство сартанов должно быть проверено в клинических испытаниях
Ссылки на основные источники:
- www.
 ncbi.nlm.nih.gov/pubmed/19120129
ncbi.nlm.nih.gov/pubmed/19120129 - www.ncbi.nlm.nih.gov/pmc/articles/PMC2998923/
Сартаны улучшают сексуальную функцию мужчин
Зачем мужчине долгая жизнь и чувствует ли он себя молодым, если нарушена его сексуальная функция?
В одном исследовании после 10 недель лечения лозартаном 88% гипертензивных мужчин с сексуальной дисфункцией отметили улучшение сексуальной функции. Их общее сексуальное удовлетворение было улучшено с 7,3% до 58,5%
Ссылка на основной источник:
- www.ncbi.nlm.nih.gov/pubmed/11370797
Кстати бета адрено блокатор карведилол не улучшает сексуальную функцию, а лозартан улучшает. Это преимущество сартанов над бета блокаторами.
Ссылка на основной источник:
- www.ncbi.nlm.nih.gov/pubmed/11206674
Безопасность сартанов была хорошо задокументирована в многочисленных рандомизированных клинических исследованиях с участием тысяч пациентов. Однако, не так давно, возникали опасения по поводу возможных связей между сартанами и повышенным риском инфаркта миокарда и рака.
 Но эта информация не подтвердилась никакими масштабными рандомизированными клиническими исследованиями.
Но эта информация не подтвердилась никакими масштабными рандомизированными клиническими исследованиями.Сартаны — одни из самых безопасных для здоровья лекарств, способных продлевать жизнь. Данные исследований показывают, что сартаны хорошо переносятся больными всех возрастов.
Ссылки на основной источник:
- www.ncbi.nlm.nih.gov/pubmed/18705533
Безопасность сартанов была хорошо задокументирована в многочисленных рандомизированных клинических исследованиях с участием тысяч пациентов. Однако, не так давно, возникали опасения по поводу возможных связей между сартанами и повышенным риском инфаркта миокарда и рака. Но эта информация не подтвердилась никакими масштабными рандомизированными клиническими испытаниями.
Ссылки на основной источник:
- www.ncbi.nlm.nih.gov/pubmed/21633727
- www.ncbi.nlm.nih.gov/pubmed/19763608
Рандомизированные контролируемые исследования на людях показали, что лечение сартанами увеличивает экспрессию белка долголетия klotho (трансмембранный белок, регулирующий чувствительность организма к инсулину и отвечающий за скорость старения.
 А повышения klotho у трансгенных мышей продлевало жизнь также, как оптимально калорийное питание.
А повышения klotho у трансгенных мышей продлевало жизнь также, как оптимально калорийное питание.В 1997 году японские и американские ученые во главе с Yo-ichi Nabeshima обнаружили новый ген — в честь греческой богини судьбы, плетущей нить жизни — Klotho. Клото, прявшая нить жизни, Лахесис, тянувшая эту нить, Атропос, которая ее обрезала) — в греческой мифологии дочери Зевса и Фемиды, богини неотвратимой судьбы. Уровень Klotho.
Университет Техаса, США. В одном исследовании (см. картинку слева) создали трансгенных мышей с отсутствием Клото. Мышки уже все умерли через 160 дней, а также проявляли признаки раннего старения. В другом исследовании создали трансгенных мышей с повышенной экспрессией Клото. Мышки прожили значительно дольше. Продление жизни было сравнимо с продлением жизни при оптимальном по калорийности питании (сокращение калорий). Смотрите нижний график на картинке слева.
- www.ncbi.nlm.nih.gov/pubmed/16123266
- http://onlinelibrary.
 wiley.com/doi/10.1002/acn3.161/abstract
wiley.com/doi/10.1002/acn3.161/abstract
Техасский Университет, США, 2011 год. Уровни содержания кальция в почках и аортах мышей коррелируют с генетическими уровнями Klotho. Кальцификация мягких тканей почек происходит при хронической болезни почек. У мышей с хронической болезнью почек низкий Klotho в почках, в плазме, в моче. У людей Klotho уменьшается все больше по мере развития хронической болезни почек. А повышение Klotho при хронической болезни почек улучшает фосфатурию, снижает кальцификацию и функцию почек. Klotho –ранний маркер хронической болезни почек и кальцификации.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/21115613
2012 год, Кавасакская медицинская школа, Курасики, Окаяма Япония. Klotho уменьшает индуцированный почечный фиброзу мышей через снижение CTGF, TGF-ß www.ncbi.nlm.nih.gov/pubmed/23034937 2018 год, Университет Оклахомы Центр наук о здоровье.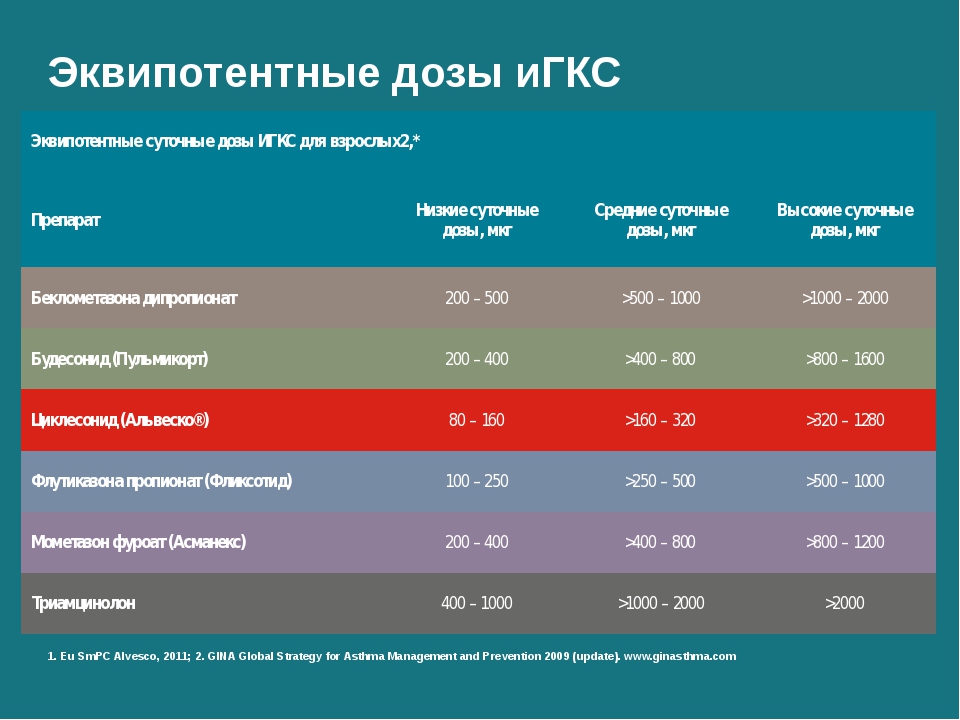 Адено-ассоциированный вирус 2 (AAV2) доставил SKL и восстановил уровень Klotho в сыворотке крови, ослабил фиброз в аортальном клапане мышей с ускоренным старением P1 (SAMP1) через снижение CTGF, TGF-ß (www.ncbi.nlm.nih.gov/pubmed/29581213). 2014 год, Университет Цукуба, Япония. Klotho уменьшает жёсткость артерий и повышает их эластичность у людей (www.ncbi.nlm.nih.gov/pubmed/24322608). 2011 год, Балтимор, США. Уровень α-Klotho в плазме у 804 жителей Тосканы (>64 лет) в течение 6 лет наблюдения. Более низкий α-Klotho в плазме был связан с более старым возрастом, нарушением метаболизма кальция и большим когнитивным ухудшением, а также с сокращением жизни (см. график слева) (www.ncbi.nlm.nih.gov/pubmed/21474560)
Адено-ассоциированный вирус 2 (AAV2) доставил SKL и восстановил уровень Klotho в сыворотке крови, ослабил фиброз в аортальном клапане мышей с ускоренным старением P1 (SAMP1) через снижение CTGF, TGF-ß (www.ncbi.nlm.nih.gov/pubmed/29581213). 2014 год, Университет Цукуба, Япония. Klotho уменьшает жёсткость артерий и повышает их эластичность у людей (www.ncbi.nlm.nih.gov/pubmed/24322608). 2011 год, Балтимор, США. Уровень α-Klotho в плазме у 804 жителей Тосканы (>64 лет) в течение 6 лет наблюдения. Более низкий α-Klotho в плазме был связан с более старым возрастом, нарушением метаболизма кальция и большим когнитивным ухудшением, а также с сокращением жизни (см. график слева) (www.ncbi.nlm.nih.gov/pubmed/21474560)
Доклинические и рандомизированные контролируемые исследования на людях показали, что лечение сартанами увеличивает экспрессию белка долголетия klotho.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/23929932
- www.
 ncbi.nlm.nih.gov/pmc/articles/PMC3108350/
ncbi.nlm.nih.gov/pmc/articles/PMC3108350/ - http://jra.sagepub.com/content/early/2013/02/04/1470320313475905.full
Сартаны могут продлить жизнь больным гипертонической болезнью грызунам в 2 раза (!). А блокада рецепторов ангиотензина II у трансгенных мышей продлевала жизнь на 26%, что может означать, что сартаны потенциально способны продлевать жизнь не только у тех, кто страдает повышенным артериальным давлением.
Таблетки от гипертонии сильно замедляют старение!!!
С одной стороны, уже очевидно, что гипертоническая болезнь (повышенное артериальное давление) сильно ускоряет старение. Именно поэтому препараты для лечения гипертонической болезни, блокирующие рецепторы ангиотензина II (сартаны) продлевают жизнь специальным крысам, склонным к развитию гипертонической болезни, в 2 раза (как видно на графике слева). Чем нам могут быть полезны такие данные.
Слева представлен график кривой смертности крыс, болеющих гипертонией. На графике видно, что такие крысы, получающие лечение сартанами, живут в два раза дольше. Что это значит для человека? Допустим (опираясь на некоторые данные), что больные гипертонией, не получающие лечение, живут в среднем около 42 года. Это значит, что средняя продолжительность жизни таких больных теоретически может составлять около 84 лет, если они будут всю жизнь проходить лечение сартанами.
Что это значит для человека? Допустим (опираясь на некоторые данные), что больные гипертонией, не получающие лечение, живут в среднем около 42 года. Это значит, что средняя продолжительность жизни таких больных теоретически может составлять около 84 лет, если они будут всю жизнь проходить лечение сартанами.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/10775560
- www.ncbi.nlm.nih.gov/pubmed/8934613
С другой стороны, даже крысам линии вистар, которые не склонны с повышению артериального давления, лозартан (один из сартанов — блокаторов рецепторов ангиотензина II) продлевал жизнь на 18%, замедляя старение сердца и сосудов.
Ссылка на исследование:
- http://m.ajpheart.physiology.org/content/293/3/h2351.full
Но все таблетки имеют много мишеней воздействия на здоровье. Как понять, что именно блокада рецепторов гормона ангиотензина II замедляет старение и продлевает жизнь. Конечно, нужно создать трансгенную линию мышей, у которой нокаутировать ген, кодирующий рецепторы ангиотензина II AT1a. Так и было сделано. И оказалось, что такие мыши не только лишились этих рецепторов, но и прожили дольше на 26%! (см. график слева).
Так и было сделано. И оказалось, что такие мыши не только лишились этих рецепторов, но и прожили дольше на 26%! (см. график слева).
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC2648681/figure/F1
Телмисартан — уникальный сартан, обладающий дополнительным свойством — частичным агонизмом к PPARγ и PPARδ рецепторам. Это позволяет повышать чувствительность к инсулину, способствовать профилактике и лечению сахарного диабета 2-го типа, снижать холестерин и улучшать липидный спектр. Из всех сартанов только телмисартан — единственный сартан, для которого доказаны эффективность в защите от развития инфаркта и инсульта, а также снижение смертности от этих событий на уровне «золотого стандарта» рамиприла.
Телмисартан — одно из лекарств группы сартанов, которое кроме снижения артериального давления через блокаду обладает дополнительным свойством — агонизм к PPAR-рецепторам. У мышей дикого типа, при длительном приеме телмисартана наблюдается повышение выносливости в беге, снижение жировых отложений и увеличение доли мышечных волокон Типа I. Волокна I типа богаты митохондриями и являются устойчивыми к усталости. Именно из-за этих их свойств было предложение с 2016 года внести телмисартан в список допинговых средств для спортсменов.
Волокна I типа богаты митохондриями и являются устойчивыми к усталости. Именно из-за этих их свойств было предложение с 2016 года внести телмисартан в список допинговых средств для спортсменов.
А кроме того, было показано, что препараты группы иАПФ снижают смертность у пожилых людей, а сартаны у пожилых смертность не снижают или снижают плохо. Но телмисартан снижает смертность также хорошо, как чемпион по этому показателю среди препаратов группы иАПФ — рамиприл.
Для телмисартана в крупных рандомизированных контролируемых слепых плацебо исследованиях доказана эффективность в защите от развития инфаркта и инсульта и смертности от них в результате атеросклероза, как и у рамиприла — «золотой» стандарт. Телмисартан уменьшает гипертрофию левого желудочка сердца (см. таблицу слева).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/21504246
- www.ncbi.nlm.nih.gov/pubmed/22011630
Телмисартан в отличии от других сартанов является частичным агонистом рецепторов PPARγ и PPARδ (Peroxisome proliferator-activated receptor). Это позволяет повышать чувствительность к инсулину, способствовать профилактике и лечению сахарного диабета 2-го типа, снижать холестерин и улучшать липидный спектр. Из всех сартанов телмисартан — самый мощный активатор PPAR — сильнее лозартана примерно в 20 раз (см. картинку слева). Телмисартан — это и препарат снижающий давление и препарат для лечения сахарного диабета 2-го типа в одной молекуле.
Это позволяет повышать чувствительность к инсулину, способствовать профилактике и лечению сахарного диабета 2-го типа, снижать холестерин и улучшать липидный спектр. Из всех сартанов телмисартан — самый мощный активатор PPAR — сильнее лозартана примерно в 20 раз (см. картинку слева). Телмисартан — это и препарат снижающий давление и препарат для лечения сахарного диабета 2-го типа в одной молекуле.
Ссылки на исследования:
- http://onlinelibrary.wiley.com/doi/10.1111/j.1582-4934.2010.01085.x/full
- www.ncbi.nlm.nih.gov/pubmed/17004092
- www.ncbi.nlm.nih.gov/pubmed/23137106
Например, в отличие от всех других сартанов телмисартан оказывает выраженное влияние на рецепторы, активирующие пролиферацию пероксисом (Peroxisome Proliferator Activated Receptor, PPAR), подтипа гамма (γ) и обеспечивает синергизм влияния на ключевые факторы риска развития сердечно-сосудистых осложнений. Кроме этого, по ряду своих фармакокинетических и фармакологических свойств телмисартан существенно (в разы!) превосходит сартаны первого поколения — валсартан, кандесартан, лозартан, олмесартан, эпросартан, ирбесартан.
Рецепторы PPARγ преобладают в белой и бурой жировой ткани, в меньшей степени — в сердце и скелетных мышцах. PPARδ экспрессируются сосудистым эндотелием, гладкомышечными клетками сосудов и макрофагальными пенистыми клетками. PPARγ-рецепторы подавляют продукцию воспалительных цитокинов и повышают чувствительность к инсулину. Таким образом, за счет влияния на PPARγ-рецепторы возможно наличие у классического гипотензивного препарата дополнительных важных клинических свойств. Стимуляция PPARγ-рецепторов сопровождается подавлением экспрессии CD36, что приводит к уменьшению захвата окисленных липопротеидов, снижению образования провоспалительных цитокинов (TNFα, IL-6, IL-1β, IL-2) за счет блокады транскрипции фактора NF-kB и усиления выработки синтазы оксида азота. Стимуляция PPARγ2-рецепторов в преадипоцитах увеличивает число малых жировых клеток и переводят в состояние самоуничтожения более крупные жировые клетки в подкожной и висцеральной жировой тканях. Это повышает чувствительность тканей к инсулину, так как именно более крупные адипоциты наименее чувствительны к инсулину.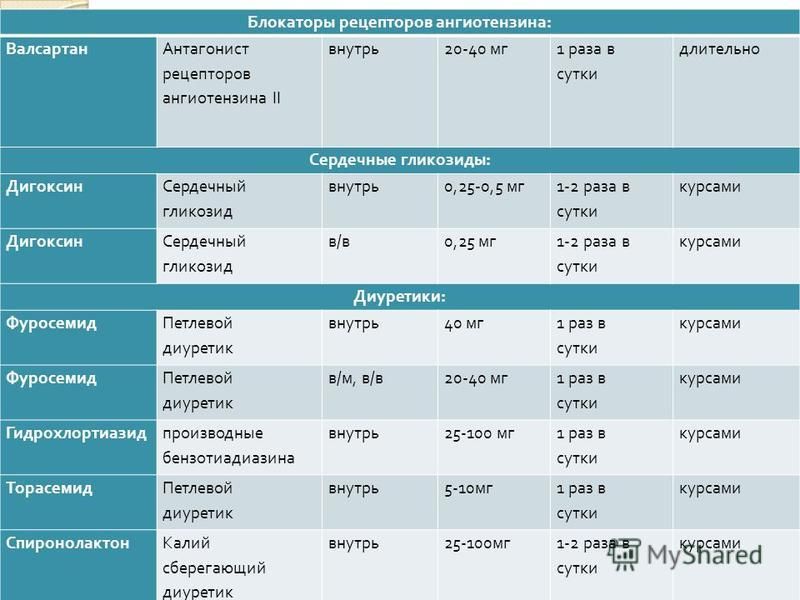 PPARγ-рецепторы в последние годы стали рассматриваться как одно из ключевых звеньев патогенеза инсулинорезистентности и метаболического синдрома. При активации PPARγ-рецепторов скелетных мышц повышается поглощение глюкозы тканями и уменьшается уровень глюкозы в крови. Благодаря снижению уровня свободных жирных кислот и глюкозы в крови подавляются липо- и глюкотоксичность и восстанавливается секреторная активность β-клеток поджелудочной железы.
PPARγ-рецепторы в последние годы стали рассматриваться как одно из ключевых звеньев патогенеза инсулинорезистентности и метаболического синдрома. При активации PPARγ-рецепторов скелетных мышц повышается поглощение глюкозы тканями и уменьшается уровень глюкозы в крови. Благодаря снижению уровня свободных жирных кислот и глюкозы в крови подавляются липо- и глюкотоксичность и восстанавливается секреторная активность β-клеток поджелудочной железы.
Необходимо еще раз подчеркнуть, что телмисартан — единственный из всех сартанов, которому свойственно комплексное влияние на показатели углеводного, липидного обмена и основные патогенетические факторы развития метаболического синдрома и ожирения (см. картинку слева). При этом важно подчеркнуть, что телмисартан является частичным агонистом PPARγ рецепторов, а значит лишен тех нежелательных эффектов влияния на сердечно-сосудистую систему, которые имеются у тиазолидиндионов, что обусловлено частичной, а не полной активацией PPARγ-рецепторов (всего на 25–30% от уровня пиоглитазона или розиглитазона). Интересен и тот факт, что телмисартан высокоэффективен при артериальной гипертензии, индуцированной высококалорийным питанием.
Интересен и тот факт, что телмисартан высокоэффективен при артериальной гипертензии, индуцированной высококалорийным питанием.
Ссылка на источник:
- www.rpcardio.com/jour/article/viewFile/865/898
Телмисартан в отличие от других сартанов за счет агонизма к PPAR-рецепторам останавливал прогрессирование диабетической нефропатии, а в 21,2 % случаев обращал ее вспять. Диабетическая нефропатия — болезнь, которая при прогрессировании переходит в хроническую почечную недостаточность. К тому же
телмисартан улучшал работу сосудистой системы почек и повышал почечную перфузию лучше рамиприла (!) у больных с нефропатией и сахарным диабетом 2 типа.Нефропатия — представляет собой поражение клубочкового аппарата и паренхимы почек различной этиологии. В целом заболевание характеризуется нарушением работы почек. Характерными клинико-лабораторными признаками заболевания являются отёки, протеинурия, в некоторых случаях повышение артериального давления. В целом развиваются различной степени выраженности нарушения фильтрационной функции почек, что в итоге может привести к хронической почечной недостаточности и к смерти. Одной из наиболее частых причин развития нефропатии является сахарный диабет. По различным данным в 30-35 % случаев нефропатия является следствием сахарного диабета.
В целом развиваются различной степени выраженности нарушения фильтрационной функции почек, что в итоге может привести к хронической почечной недостаточности и к смерти. Одной из наиболее частых причин развития нефропатии является сахарный диабет. По различным данным в 30-35 % случаев нефропатия является следствием сахарного диабета.
Трансформирующий Фактор Роста-β участвует в эпителиально мезенхимальном переходе, вызывающем фиброз — утрату почками их функции в результате разрастания соединительной ткани с появлением рубцовых изменений. Заблокировав фиброз, возможно остановить прогрессирование нефропатии почек до почечной недостаточности. Индукция Трансформирующий Фактор Роста-β вызывает накопление внеклеточного матрикса в клубочках почек, что приводит к прогрессирующей болезни почек, а удвоение базовых уровней TGF-β в плазме крови хоть немного, но независимо связано с более низкой скоростью клубочковой фильтрации почек (риск почечной недостаточности). Интересно, что телмисартан в отличии от валсартана блокирует фиброз обусловленный TGF-бета.
Интересно, что телмисартан в отличии от валсартана блокирует фиброз обусловленный TGF-бета.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/18846335
Телмисартан через подавление воспаления, благодаря активации PPARγ, и антифиброзных свойств, благодаря активации PPARδ, приостанавливал прогрессию диабетической нефропатии или обращал её вспять, отдаляя наступление почечной недостаточности.
Исследование INNOVATION (INcipieNtto OVert: AngiotensinII receptor blocker, Telmisartan, Investigation On type 2diabetic Nephropathy) продемонстрировало, что телмисартан в дозе 40 мг/сут. у больных сахарным диабетом способен предотвращать прогрессирование микроальбуминурии в протеинурию. У 21,2% пациентов, принимавших телмисартан в дозе 80 мг в сутки, микроальбуминурия регрессировала. При этом ренопротективный эффект имел место и у пациентов с исходно нормальным уровнем артериального давления. Данный факт в очередной раз доказывает дополнительные нефропротективные механизмы телмисартана, напрямую не связанные с его гипотензивным эффектом, а зависят от того, то телмисартан является частичным агонистом рецепторов PPARγ и PPARδ./26/26.jpg) К тому же телмисартан улучшал работу сосудистой системы почек и повышал почечную перфузию лучше рамиприла (!) у больных с нефропатией и сахарным диабетом 2 типа. Таким образом, эффективность телмисартана у больных с выраженной диабетической нефропатией можно считать доказанной.
К тому же телмисартан улучшал работу сосудистой системы почек и повышал почечную перфузию лучше рамиприла (!) у больных с нефропатией и сахарным диабетом 2 типа. Таким образом, эффективность телмисартана у больных с выраженной диабетической нефропатией можно считать доказанной.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/17697525
- www.nature.com/hr/journal/v37/n5/full/hr2013157a.html
- www.kusumpharm.com/images/imagesForTinyMCE/hipotel/RU_1_Hipotel1.pdf
Телмисартан в отличие от других сартанов потенциально может играть защитную роль против печеночной инсулинорезистентности при диабете за счет агонизма к PPARγ-рецепторам.
PPARγ-рецепторы в последние годы стали рассматриваться как одно из ключевых звеньев патогенеза инсулинорезистентности и метаболического синдрома, поскольку они обеспечивают регуляцию образования глюкозы в печени, влияя на окисление жирных кислот. Неалкогольная жировая болезнь печени в настоящее время считается важным компонентом метаболического синдрома. Обзор исследований 2018 года показал, что телмисартан, который оказывает положительное влияние на метаболизм печени, предотвращает прогрессирование неалкогольной жировой дистрофии печени до цирроза печени. Телмисартан потенциально может играть защитную роль в защите от печеночной инсулинорезистентности при диабете.
Обзор исследований 2018 года показал, что телмисартан, который оказывает положительное влияние на метаболизм печени, предотвращает прогрессирование неалкогольной жировой дистрофии печени до цирроза печени. Телмисартан потенциально может играть защитную роль в защите от печеночной инсулинорезистентности при диабете.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18380932
- www.ncbi.nlm.nih.gov/pubmed/29636553
- www.rpcardio.com/jour/article/viewFile/865/898
При ССЗ конечные продукты гликирования (КПГ) вызывают формирование «сшивок» с аминогруппами коллагена, что является причиной потери эластичности сосудов и захвата ЛПНП стенками артерий. КПГ также могут вызывать гликирование ЛПНП, что может способствовать их окислению и развитию атеросклероза. Более того КПГ могут связываться с рецепторами КПГ, что вызывает оксидативный стресс и активацию воспалительных реакций в эндотелиальных клетках сосудов. Телмисартан в отличии от других сартанов мощно снижает уровень рецепторов КПГ у пациентов с эссенциальной гипертензией.

Накопление конечных продуктов гликирования — одна из причин старения человека, а также многих возраст зависимых заболеваний: атеросклероз, инфаркт миокарда, застойная сердечная недостаточность, диабетическая ретинопатия, диабетическая нейропатия, диабетическая нефропатия, болезнь Альцгеймера, псориаз. RAGE — это рецепторы, которые связывают конечные продукты гликирования (о роли гликирования белков в старении можно прочитать здесь). Телмисартан снижает связывание конечных продуктов гликирования с рецепторами RAGE у гипертоников.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18473846
- www.ncbi.nlm.nih.gov/pubmed/16271939
- www.ncbi.nlm.nih.gov/pubmed/17697525
- www.sciencedirect.com/science/article/pii/S0026286205000877
- www.ncbi.nlm.nih.gov/pubmed/18855759
Для подтверждения роли конечных продуктов гликирования в пагубном влиянии на функционирование тканей был проведен эксперимент. Вводились конечные продукты гликирования в ткани крыс. В последствии в тканях крыс были выявлены проявления возрастных диабетических изменений, хотя у крыс глюкоза была всегда в норме, а значит не могло быть повышенной глюкозы в крови, и не могло быть диабета.
В последствии в тканях крыс были выявлены проявления возрастных диабетических изменений, хотя у крыс глюкоза была всегда в норме, а значит не могло быть повышенной глюкозы в крови, и не могло быть диабета.
При сердечно-сосудистых заболеваниях конечные продукты гликирования вызывают формирование ковалентных связей «сшивок» с аминогруппами коллагена, что является причиной потери эластичности сосудов и захвата ЛПНП стенками артерий. Конечные продукты гликирования также могут вызывать гликирование ЛПНП, что может способствовать их окислению. Окисленные ЛПНП являются одним из основных факторов в развитии атеросклероза. Более того конечные продукты гликирования могут связываться с рецепторами конечных продуктов гликирования (RAGE) что вызывает оксидативный стресс и активацию воспалительных реакций в эндотелиальных клетках сосудов. Интересно, что телмисартан в отличии от других сартанов снижает уровень рецепторов конечных продуктов гликирования у пациентов с эссенциальной гипертензией (см. картинку слева) (www.ncbi.nlm.nih.gov/pubmed/16271939).
картинку слева) (www.ncbi.nlm.nih.gov/pubmed/16271939).
Высокие уровни конечных продуктов гликирования были обнаружены в плазме и в коронарных артериях пациентов с историей курения. Предположительно из-за проглатывания конечных продуктов гликирования, образующихся при отверждении табака. Основными причинами смерти курильщиков являются инфаркт миокарда и легочные заболевания. А нахождение конечных продуктов гликирования указывает на ускоренное старение внеклеточного матрикса курильщиков.
Недавно ученые проанализировали ткани аорты больных сахарным диабетом на наличие перекрестных связей гликирования и продемонстрировали значительную корреляцию с увеличением жесткости аорты. Установив роль гликирования в усилении жесткости аорты, ученые изучили образование конечных продуктов гликирования в изолированном чистом эластине. Эластин, как известно, отвечает за эластичность артерий, которая снижается с возрастом. Было показано, что гликирование эластина снижает его функциональные свойства.
Телмисартан в отличии от других сартанов повышает выносливость в беге и других аэробных упражнениях через активацию с ppar-δ/AMPK пути.
У мышей дикого типа, при длительном приеме телмисартана наблюдается повышение выносливости в беге, снижение жировых отложений и увеличение доли мышечных волокон Типа I. Волокна I типа богаты митохондриями и являются устойчивыми к усталости. Именно из-за этих их свойств было предложение с 2016 года внести телмисартан в список допинговых средств для спортсменов. У мышей телмисартан повышает выносливость в беге через активацию PPAR-δ/AMPK пути. Мышечно-специфическая переэкспрессия PPAR-δ приводит к глубокому изменению состава мышечных волокон из-за гиперплазии и/или перехода на более окислительные волокна, что приводит к повышению ферментативной активности и выносливости.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/20477906
- http://onlinelibrary.wiley.com/doi/10.1111/j.1582-4934.2010.01085.x/full
Телмисартан в отличии от других сартанов подавляет воспаления в сосудах (снижает с-реактивный белок) через активацию PPAR и ингибирование NF-kb.

С-реактивный белок (СРБ) используется в клинической диагностике наряду с СОЭ как индикатор воспаления. Отношения между СРБ и сердечно-сосудистыми заболеваниями исследуются уже на протяжении многих лет, результаты описаны в целом ряде оригинальных и обзорных исследований. Наиболее часто выводы о возможности участия СРБ в патогенезе атеросклероза и острого инфаркта миокарда. Высокий уровень СРБ сильно повышает риск внезапной смерти от заболеваний сердца. Американская Ассоциация Сердца и центр США по контролю и профилактике болезней у определенных групп риска определяют уровень С-реактивного белка с низким риском ССЗ — не выше 1 мг/л
PPAR-активация – ключевое преимущество телмисартана и его комбинаций. Телмисартан в отличии от других сартанов значительно сильнее подавляет воспаление в сосудах (снижает СРБ) через активацию PPAR и ингибирование NF-kb (см. рисунок слева).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/24994548
- www.
 ncbi.nlm.nih.gov/pubmed/17004092
ncbi.nlm.nih.gov/pubmed/17004092 - www.ncbi.nlm.nih.gov/pubmed/19590508
- https://cyberleninka.ru/article/n/vliyanie-telmisartana-na-lipidnyy-profil-i-faktory-vospaleniya-u-bolnyh-arterialnoy-gipertenziey-i-abdominalnym-ozhireniem
Телмисартан в отличии от других сартанов защищает сосуды, модулируя функцию эндотелия сосудов, через повышение митохондриальной активности, активируя AMPK.
Митохондриальная дисфункция играет важную роль в клеточном старении и нарушении функции эндотелия сосудов, приводящих к сердечно-сосудистым заболеваниям. АМП-активированная киназа протеина (AMPK) играет критическую роль в митохондриальном биогенезе и эндотелиальной функции. Телмисартан в отличии от других сартанов (см. рисунок слева) защищает сосуды, дозозависимо модулируя функцию эндотелия сосудов, через повышение митохондриальной активности, активируя AMPK (5′ аденозинмонофосфат-активируемая протеинкиназа— это фермент, который играет важную роль в клеточном гомеостазе энергии).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/25682036
- www.ncbi.nlm.nih.gov/pubmed/25249228
Сегодня показано, что ангиотензин II способен вызывать деменцию у крыс, схожую с болезнью Альцгеймера. Телмисартан в отличие от лекарств для снижения давления группы иАПФ, связан со значительным сокращением заболеваемости и прогрессирования болезни Альцгеймера даже в низких дозах, не снижающих артериальное давление — за счёт активации PPAR.
Болезнь Альцгеймера — наиболее распространённая форма деменции, нейродегенеративное заболевание, впервые описанное в 1907 году немецким психиатром Алоисом Альцгеймером. Как правило, она обнаруживается у людей старше 65 лет. Общемировая заболеваемость на 2006 год оценивалась в 26,6 млн человек, а к 2050 году число больных может вырасти вчетверо. Как правило, болезнь начинается с малозаметных симптомов, но с течением времени прогрессирует. Наиболее часто на ранних стадиях распознаётся расстройство кратковременной памяти, например, неспособность вспомнить недавно заученную информацию.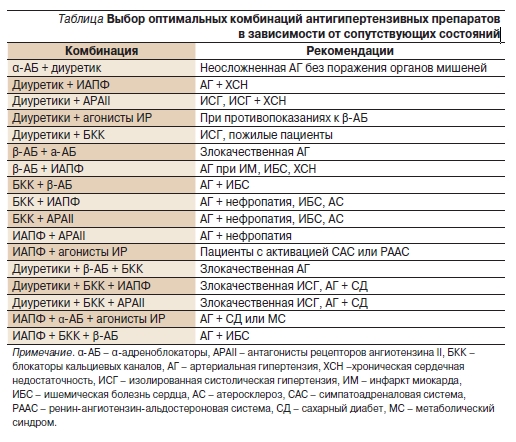 С развитием болезни происходит потеря долговременной памяти, возникают нарушения речи и когнитивных функций, пациент теряет способность ориентироваться в обстановке и ухаживать за собой. Постепенная потеря функций организма ведёт к смерти (ru.wikipedia.org/wiki/Болезнь_Альцгеймера).
С развитием болезни происходит потеря долговременной памяти, возникают нарушения речи и когнитивных функций, пациент теряет способность ориентироваться в обстановке и ухаживать за собой. Постепенная потеря функций организма ведёт к смерти (ru.wikipedia.org/wiki/Болезнь_Альцгеймера).
Сегодня показано, что ангиотензин II способен вызывать деменцию у крыс, схожую с болезнью Альцгеймера. Исследование от 2010 года от Бостонского Университета, США показало, что сартаны (см. рисунок — сартаны на рисунке синим цветом) в отличие от лекарств для снижения давления группы иАПФ, связаны со значительным сокращением заболеваемости и прогрессирования болезни Альцгеймера даже в низких дозах, не снижающих артериальное давление — за счёт активации рецепторов PPAR. Сартаны снижали смертность от болезни Альцгеймера и деменции у пациентов, которые уже имели эти заболевания. В исследовании участвовали 819 491 человек преимущественно мужского пола (98%) в возрасте от 65 лет и старше с сердечно-сосудистыми заболеваниями. Исследования на животных сообщают, что сартаны вызывают нейропротекторные реакции (защищающие клетки мозга), которые не зависят от снижения кровяного давления и проявляются даже в культуре клеток. Лечение сартанами является нейропротекторным: уменьшает ишемию мозга, связанную со стрессом воспалением мозга. Было продемонстрировано, что лечение сартанами не только улучшает качество жизни у гипертоников, но и снижает тревожность и депрессию у больных сахарным диабетом. Также блокада синтеза ангиотензина II ингибиторами АПФ, по-видимому, оказывает аналогичное терапевтическое действие, так как повышает эффективность антидепрессантов и уменьшает тревожность и депрессию у людей без гипертонической болезни.
Исследования на животных сообщают, что сартаны вызывают нейропротекторные реакции (защищающие клетки мозга), которые не зависят от снижения кровяного давления и проявляются даже в культуре клеток. Лечение сартанами является нейропротекторным: уменьшает ишемию мозга, связанную со стрессом воспалением мозга. Было продемонстрировано, что лечение сартанами не только улучшает качество жизни у гипертоников, но и снижает тревожность и депрессию у больных сахарным диабетом. Также блокада синтеза ангиотензина II ингибиторами АПФ, по-видимому, оказывает аналогичное терапевтическое действие, так как повышает эффективность антидепрессантов и уменьшает тревожность и депрессию у людей без гипертонической болезни.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/22982863
- www.ncbi.nlm.nih.gov/pubmed/20068258
- www.ncbi.nlm.nih.gov/pmc/articles/PMC2998923
Телмисартан улучшает симптомы стресс-индуцированной депрессии у животных, находящихся под хроническим стрессом, путем активации PPAR. Поэтому, телмисартан может быть исследован у людей, как потенциальный антидепрессант в будущем [www.ncbi.nlm.nih.gov/pubmed/29070884]. Также Мета-анализ РКИ (на людях) указывает на то, что агонисты PPAR обладают антидепрессивными свойствами, а телмисартан является частичным агонистом PPAR [www.ncbi.nlm.nih.gov/pubmed/27978584]
Поэтому, телмисартан может быть исследован у людей, как потенциальный антидепрессант в будущем [www.ncbi.nlm.nih.gov/pubmed/29070884]. Также Мета-анализ РКИ (на людях) указывает на то, что агонисты PPAR обладают антидепрессивными свойствами, а телмисартан является частичным агонистом PPAR [www.ncbi.nlm.nih.gov/pubmed/27978584]
Глиальные клетки мозга входят в структуру внеклеточного матрикса мозга, обеспечивая каркас для нейронов (основных клеток мозга), склеивая. Отсюда и название — глиальные (glue = клей). Глиальные клетки также регулируют внутри- и внеклеточные условия, необходимые для проведения нервного импульса и забирают из синаптической щели использованные нейротрансмиттеры. Но гелия также участвует в воспалении. Университет имени Бен-Гуриона, Израиль, 2016 год. В моделях болезни Альцгеймера, где происходит нейровоспаление, были показаны повышенные уровни рецепторов ангиотензина II AT1 в префронтальной коре мозга. Интраназальная доставка телмисартана приводила к ослаблению активации микроглии/макрофагов и к уменьшению амилоидных бляшек в головном мозге./096/096.jpg) Действие телмисартана также обусловлено не только блокадой рецепторов ангиотензина II AT1, но и агонизмом к PPAR рецепторам (www.ncbi.nlm.nih.gov/pubmed/27187688). В мышиной модели болезни Альцгеймера 5 месяцев интраназальной обработки телмисартаном значительно уменьшило накопление бета-амилоида в коре и гиппокампе мозга мышей, снизилось накопление микроглии и связанного с этим воспаления, снижалась потеря нейронов мозга в коре. Также наблюдалась лучшая ориентация в пространстве (www.ncbi.nlm.nih.gov/pubmed/28385651). Интересно, что телмисартан уменьшал накопление бета-амилоида у крыс и снижал спад когнитивных функций даже, когда применялся в низких дозах, не снижающих артериальное давление (www.ncbi.nlm.nih.gov/pubmed/25241340) (www.ncbi.nlm.nih.gov/pubmed/19635982). А мета-анализ 2016 года показал, что агонисты PPAR-γ (к которым относится и телмисартан) являются перспективными средствами для лечения болезни Альцгеймера (www.ncbi.nlm.nih.gov/pubmed/26001206).
Действие телмисартана также обусловлено не только блокадой рецепторов ангиотензина II AT1, но и агонизмом к PPAR рецепторам (www.ncbi.nlm.nih.gov/pubmed/27187688). В мышиной модели болезни Альцгеймера 5 месяцев интраназальной обработки телмисартаном значительно уменьшило накопление бета-амилоида в коре и гиппокампе мозга мышей, снизилось накопление микроглии и связанного с этим воспаления, снижалась потеря нейронов мозга в коре. Также наблюдалась лучшая ориентация в пространстве (www.ncbi.nlm.nih.gov/pubmed/28385651). Интересно, что телмисартан уменьшал накопление бета-амилоида у крыс и снижал спад когнитивных функций даже, когда применялся в низких дозах, не снижающих артериальное давление (www.ncbi.nlm.nih.gov/pubmed/25241340) (www.ncbi.nlm.nih.gov/pubmed/19635982). А мета-анализ 2016 года показал, что агонисты PPAR-γ (к которым относится и телмисартан) являются перспективными средствами для лечения болезни Альцгеймера (www.ncbi.nlm.nih.gov/pubmed/26001206).
Телмисартан в отличии от других сартанов имеет мощный антипролиферативный эффект в отношении клеток рака простаты через активацию PPARγ-рецепторов.
 И может быть мощным средством для профилактики и лечения рака простаты.
И может быть мощным средством для профилактики и лечения рака простаты.Рак предстательной железы — одно из наиболее распространённых злокачественных новообразований у мужчин. Ежегодно в мире выявляется свыше 400 000 случаев рака предстательной железы; в ряде стран он занимает в структуре онкологических заболеваний 2-е или 3-е место после рака лёгких и рака желудка (так, в Европе в 2004 году заболеваемость раком предстательной железы составляла 214 случаев на 100 000 мужчин, в результате чего рак простаты занимал 2-е место среди основных причин смерти от рака у мужчин, опережая рак лёгких и колоректальный рак).
2008 год, Осакский городской Университет, Япония. Телмисартан имеет мощный антипролиферативный эффект в отношении клеток рака простаты через активацию PPARγ-рецепторов. И может быть мощным средством для профилактики и лечения рака простаты, что предстоит выяснить в клинических испытаниях. Стоит заметить (см. рисунок слева), что никакие другие сартаны 1-го поколения на такое не способны, так как не обладают достаточным агонизмом к PPARγ. НА графике видно, как телмисартан дозозависимо приводил раковые клетки к самоуничтожению.
НА графике видно, как телмисартан дозозависимо приводил раковые клетки к самоуничтожению.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/18636189
Телмисартан вызывает торможение пролиферации клеток рака толстой кишки.
Телмисартан мощно ингибирует HB-EGF-CTF (Гепарин-связывающий эпидермальный фактор роста), вызывая торможение пролиферации клеток рака толстой кишки (см. рисунок слева). И может быть эффективным средством для профилактики, что предстоит выяснить в будущих клинических исследованиях.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/23451083
Телмисартан уникальный сартан в отличии от других сартанов за счет агонизма к PPAR значительно увеличивает количество и функциональную активность эндотелиальных прогениторных клеток. Эндотелиальные прогениторные клетки (ЭПК), полученные из костного мозга, способствуют ремонту эндотелия сосудов, защищают КИМ сосудов от утолщения.
Эндотелиальные прогениторные клетки (ЭПК) привлекают внимание ученых своим участием в процессах восстановления эндотелия и в формировании новых сосудов./093/093.jpg) Термины «прогениторная клетка», «стволовая клетка» или «клетка-предшественник» относятся к клеткам иммунной системы, которые обладают способностью к самообновлению и дифференцировке в различные типы клеток. Поэтому эти клетки потенциально могут восстанавливать функцию поврежденных тканей.
Термины «прогениторная клетка», «стволовая клетка» или «клетка-предшественник» относятся к клеткам иммунной системы, которые обладают способностью к самообновлению и дифференцировке в различные типы клеток. Поэтому эти клетки потенциально могут восстанавливать функцию поврежденных тканей.
Ссылка на источник:
- https://cyberleninka.ru/article/n/rol-endotelialnyh-progenitornyh-kletok-pri-ateroskleroze
2008 год, Университетская Больница Цюрих, Цюрих, Швейцария. Считается, что эндотелиальная травма кровеносных сосудов играет ключевую роль в развитии и прогрессировании сосудистых заболеваний, таких как атеросклероз, гипертония или рестеноз, а также их осложнений, включая инфаркт миокарда или инсульт. Накопленные данные говорят о том, что эндотелиальные прогениторные клетки (ЭПК) (см. рисунок слева), полученные из костного мозга, способствуют ремонту эндотелия сосудов, защищают КИМ сосудов от утолщения. Ишемическая болезнь сердца и ее факторы риска, такие как диабет, гиперхолестеринемия, гипертония и курение, связаны со снижением количества и нарушением функциональной активности циркулирующих в крови эндотелиальных прогениторных клеток. Более того, исходные данные свидетельствуют о том, что снижение уровня эндотелиальных прогениторных клеток связано с дисфункцией эндотелия сосудов и с повышенным риском сердечно-сосудистых событий (инсульт и инфаркт). А нарушение ремонта сосудов из-за снижения количества и функции эндотелиальных прогениторных клеток способствует прогрессированию сосудистых заболеваний. Несколько экспериментальных и клинических исследований показали, что, сартаны и особенно агонист PPAR гамма телмисартан увеличивают количество и функциональную активность эндотелиальных прогениторных клеток. Было также показано, что прогениторные клетки крови также имеют рецепторы гормона ангиотензина II AT1, на которые могут действовать препараты группы сартанов, особенно телмисартан. Это указывает на то, что сартаны могут напрямую влиять на прогениторные клетки.
Более того, исходные данные свидетельствуют о том, что снижение уровня эндотелиальных прогениторных клеток связано с дисфункцией эндотелия сосудов и с повышенным риском сердечно-сосудистых событий (инсульт и инфаркт). А нарушение ремонта сосудов из-за снижения количества и функции эндотелиальных прогениторных клеток способствует прогрессированию сосудистых заболеваний. Несколько экспериментальных и клинических исследований показали, что, сартаны и особенно агонист PPAR гамма телмисартан увеличивают количество и функциональную активность эндотелиальных прогениторных клеток. Было также показано, что прогениторные клетки крови также имеют рецепторы гормона ангиотензина II AT1, на которые могут действовать препараты группы сартанов, особенно телмисартан. Это указывает на то, что сартаны могут напрямую влиять на прогениторные клетки.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18793110
- www.
 ncbi.nlm.nih.gov/pubmed/17456026
ncbi.nlm.nih.gov/pubmed/17456026
2009 год, отделение кардиологии Токийского женского медицинского Университета, Япония. Поскольку считается, что эндотелиальные прогениторные клетки играют критическую роль при ишемических заболеваниях, ученые исследовали влияние телмисартана на пролиферацию эндотелиальных прогениторных клеток. На клеточных культурах, взятых от здоровых людей, было показано, что в присутствии телмисартана через 4 дня количество колоний эндотелиальных прогениторных клеток увеличивалось в зависимости от дозы — чем больше доза, тем больше (см. рисунок). Но этого не происходило в присутствии другого сартана — валсартана. Это потому, что телмисартан — это уникальный сартан, так как телмисартан агонист PPAR гамма в отличии от других сартанов. Так другой агонист PPAR гамма (росиглитазон) также увеличивал количество эндотелиальных прогениторных клеток. А когда было добавлено к телмисартану вещество, подавляющее PPAR гамма, то количество колоний эндотелиальных прогениторных клеток не увеличивалось. Эти данные свидетельствуют о том, что телмисартан может способствовать целостности эндотелия и васкулогенезу в ишемических областях путем увеличения числа эндотелиальных прогениторных клеток. Другие сартаны не имеют столь мощного действия, как телмисартан. Также телмисартан повышал фосфолирование Akt. А ингибирование активации Akt значительно ослабило влияние телмисартана на функцию эндотелиальных прогениторных клеток. Это говорит о том, что Akt участвует в стимулирующем эффекте телмисартана на дифференцировку эндотелиальных прогениторных клеток.
Эти данные свидетельствуют о том, что телмисартан может способствовать целостности эндотелия и васкулогенезу в ишемических областях путем увеличения числа эндотелиальных прогениторных клеток. Другие сартаны не имеют столь мощного действия, как телмисартан. Также телмисартан повышал фосфолирование Akt. А ингибирование активации Akt значительно ослабило влияние телмисартана на функцию эндотелиальных прогениторных клеток. Это говорит о том, что Akt участвует в стимулирующем эффекте телмисартана на дифференцировку эндотелиальных прогениторных клеток.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/19193378
- www.ncbi.nlm.nih.gov/pubmed/24384433
Далее эти же данные были подтверждены и в клинических исследованиях у людей.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/21825227
2010, Университетская клиника Бонн, Германия. И статины и телмисартан по отдельности показали свои свойства повышать число эндотелиальных прогениторных клеток, улучшать их функцию, миграцию, снижать апоптоз. Телмисартан уникальный сартан, так как является в отличии от других сартанов агонистом PPAR гамма и действует как за счет блокады рецепторов ангиотензина II AT1 (даже одна лишь блокада ангиотензина II AT1 немного, но работает www.ncbi.nlm.nih.gov/pubmed/18049030), так и за счет агонизма к PPAR гамма. Но могут ли эти средства, применяемые совместно, оказывать еще больший синергичный эффект?
Телмисартан уникальный сартан, так как является в отличии от других сартанов агонистом PPAR гамма и действует как за счет блокады рецепторов ангиотензина II AT1 (даже одна лишь блокада ангиотензина II AT1 немного, но работает www.ncbi.nlm.nih.gov/pubmed/18049030), так и за счет агонизма к PPAR гамма. Но могут ли эти средства, применяемые совместно, оказывать еще больший синергичный эффект?
На клеточных культурах, взятых от здоровых людей, а также на мышах дикого типа было показано (см. рисунок), что телмисартан и один из статинов (симвастатин) по отдельности повышают число колоний эндотелиальных прогениторных клеток. Телмисартан уменьшил апоптоз эндотелиальных прогениторных клеток. Однако сочетание телмисартана и симвастатина привело к еще более значительному синергичному увеличению количества и функции эндотелиальных прогениторных клеток, а также повысило их миграцию в зону поражения эндотелия. Комбинация значительно уменьшила индуцированное повреждение эндотелия сонных артерий. Однако не стоит одновременно с телмисартаном+статином использовать ингибиторы MMP9, так как ингибирование MMP9 может свести на нет повышение уровня эндотелиальных прогениторных клеток. Ингибиторами MMP9 являются, например, пентоксифиллин и доксициклин.
Однако не стоит одновременно с телмисартаном+статином использовать ингибиторы MMP9, так как ингибирование MMP9 может свести на нет повышение уровня эндотелиальных прогениторных клеток. Ингибиторами MMP9 являются, например, пентоксифиллин и доксициклин.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/19555424
- www.ncbi.nlm.nih.gov/pubmed/16515775
- www.ncbi.nlm.nih.gov/pubmed/16480696
- www.ncbi.nlm.nih.gov/pubmed/8019484
2014 год, Академия медицинских наук Шаньдуна, Китай. А короткий курс телмисартана с розувастатином при контроле артериального давления позволил синергично уменьшить КИМ сонных артерий у людей с гипертонической болезнью сердца, пусть и немного, что ранее считалось невозможным. Стоит заметить, что у гипертоников вообще сложно уменьшить КИМ, так как сама гипертоническая болезнь способствует более быстрому прогрессированию КИМ сосудов. И тем это ценно. Тем более, что телмисартан или розувастатин по отдельности это сделать не смогли — только вместе в результате синергии.
И тем это ценно. Тем более, что телмисартан или розувастатин по отдельности это сделать не смогли — только вместе в результате синергии.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24495792
Телмисартан предупреждает рак печени у крыс, страдающих неалкогольной жировой дистрофией печени.
Гепатоцеллюлярная карцинома (в просторечии рак печени) — наиболее распространённая первичная злокачественная опухоль печени. Ежегодно в мире диагностируют около 600 тыс. случаев. Основными причинами рака печени являются цирроз из-за гепатита В, гепатита С или алкоголя, а также неалкогольная жировая дистрофия печени из-за инсулинорезистентности.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/25530442
- www.ncbi.nlm.nih.gov/pubmed/9658369
—
2013 год, Медицинский Колледж Асахикавы, Япония. У крыс была искусственно вызвана неалкогольная жировая дистрофия печени, которая в 54,6% случаев переходила в цирроз печени и рак печени (гепатоцеллюлярная карцинома). Однако в другой группе крыс, которым также пытались индуцировать рак, но кормили телмисартаном, рак печени не развивался. Телмисартан предупредил рак печени у крыс. Телмисартан снизил у крыс маркер разрушения ДНК 8-OHdG, а также сосудистый эндотелиальный фактор роста (vegf).
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/22886508
Миостатин негативно регулирует работу скелетных мышц. Его удаление с помощью генетических вмешательств вызывает избыточный рост мышц, а, наоборот, его избыточная активность приводит к атрофии мышц. Телмисартан подавляет миостатин и защищают от саркопении (снижение мышечной массы при старении). Также телмисартан через активацию PPARγ-рецепторов позволяет повышать чувствительность к инсулину — гормону, который регулирует уровень глюкозы в крови, что способствует уменьшению межмышечного жира. А межмышечный жир — одна из причин снижения мышечной массы с возрастом.
Саркопения – это патологическое состояние, ассоциированное с возрастом, характеризующееся снижением массы скелетной мускулатуры. Саркопения до недавнего времени не привлекала должного внимания геронтологов и других врачей. Роль состояния скелетной мускулатуры, её силы и массы, в сохранении здоровья и увеличении продолжительности активной фазы жизни оставались недооцененной, но в последние 15 лет отношение к саркопении стало меняться. По данным американского центра контроля заболеваемости (Center for Disease Control and Prevention, CDC) саркопения признана одним из пяти основных факторов риска заболеваемости и смертности у лиц старше 65 лет.
Миостатин принадлежит к семейству трансформирующих факторов роста бета (TGF-beta) и негативно регулирует работу скелетных мышц. Его удаление с помощью генетических вмешательств вызывает избыточный рост мышц, а, наоборот, его избыточная активность приводит к атрофии мышц. Животные с удалением миостатина выглядят, как на картинке слева. Подавление миостатина усиливает регенерацию мышечной ткани при саркопении, увеличивая пролиферацию клеток спутников.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/15215484
- www.ncbi.nlm.nih.gov/pubmed/9139826
- www.ncbi.nlm.nih.gov/pubmed/17551508
Исследование 2011 года, проведенное в Университете Джона Хопкинса в США, показало, что лекарство от артериального давления группы сартанов (телмисартан) подавляют миостатин у мышей и защищают от саркопении.
Ссылка(и) на исследование(я):
- www.ncbi.nlm.nih.gov/pubmed/21562229
Гормон Ангиотензин II вызывает саркопению, а ингибирование ангиотензина, либо его рецепторов — перспективный метод лечения саркопении.
Ангиотензин II — это гормон, благодаря которому повышается артериальное давление. С возрастом уровень Ангиотензина II у многих людей растет, и прогрессирует саркопения вместе с повышением артериального давления. Это происходит потому, что Ангиотензин II, как показали исследования, вызывает саркопению, активизируя миостатин — белок, который подавляет рост и дифференцировку мышечной ткани. И, напротив блокада рецепторов ангиотензина II (AT1 рецепторов), предотвращает потерю мышечной массы и является перспективным методом лечения саркопении.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/21570954
- www.ncbi.nlm.nih.gov/pubmed/21747283
- www.ncbi.nlm.nih.gov/pubmed/23769949
Агонисты PPARγ предупреждают саркопению через регулирование метаболизма глюкозы. Активация PPARγ-рецепторов (Peroxisome proliferator-activated receptor gamma) позволяет повышать чувствительность к инсулину — гормону, который регулирует уровень глюкозы в крови, что способствует уменьшению межмышечного жира. А межмышечный жир — одна из причин снижения мышечной массы. Агонисты PPARγ-рецепторов являются перспективными средствами для лечения саркопении.
Ссылка на источник:
- https://it.wikipedia.org/wiki/PPAR-γ
Тераностика старения оценивает диагностические параметры Вашего организма и информирует о существующих способах увеличения Вашей продолжительности жизни.
После диагностики параметров Вашего организма (https://nestarenie.ru/novaya-teranostika-stareniya-1-5.html) в медицинском центре, запишитесь на прием к врачу.
Выполняйте рекомендации врача, которые помогут увеличить продолжительность Вашей жизни. До встречи в 22 веке.
Выводы:
- Повышенное артериальное давление ускоряет старение. Механизмов повышения артериального давления несколько. Но центральный из них — это гиперактивация рецепторов гормона ангиотензина II.
- Сартаны — это лекарства от повышенного артериального давления. Основной механизм их действия — это блокада рецепторов ангиотензина II (AT1 рецепторов). Эти рецепторы связываются с гормоном ангиотензин II и повышают артериальное давление, а также стимулируют ряд негативных процессов в организме, способствующих ухудшению здоровья и сокращению продолжительности жизни.
- Гормон Ангиотензин II вызывает саркопению (потерю мышц с возрастом сильно сокращающая жизнь), а ингибирование ангиотензина II, либо его рецепторов — перспективный метод лечения саркопении.
- Стресс — один из самых сильных катализаторов ускоренного старения. Сартаны, способны проникать через гематоэнцефалический барьер и тормозить активность пресинаптических AT1-рецепторов симпатических нейронов, которые регулируют высвобождение норадреналина. Поэтому нельзя исключить наличие также и центральных механизмов антигипертензивного действия сартанов, что важно для защиты от стрессов.
- Сартаны улучшают сексуальную функцию мужчин.
- Безопасность сартанов была хорошо задокументирована в многочисленных рандомизированных клинических исследованиях с участием тысяч пациентов. Однако, не так давно, возникали опасения по поводу возможных связей между сартанами и повышенным риском инфаркта миокарда и рака. Но эта информация не подтвердилась никакими масштабными рандомизированными клиническими исследованиями.
- Рандомизированные контролируемые исследования на людях показали, что лечение сартанами увеличивает экспрессию белка долголетия klotho (трансмембранный белок, регулирующий чувствительность организма к инсулину и отвечающий за скорость старения. А повышения klotho у трансгенных мышей продлевало жизнь также, как оптимально калорийное питание.
- Сартаны могут продлить жизнь больным гипертонической болезнью грызунам в 2 раза (!). А блокада рецепторов ангиотензина II у трансгенных мышей продлевала жизнь на 26%, что может означать, что сартаны потенциально способны продлевать жизнь не только у тех, кто страдает повышенным артериальным давлением.
- Телмисартан — уникальный сартан, обладающий дополнительным свойством — частичным агонизмом к PPARγ и PPARδ рецепторам. Это позволяет повышать чувствительность к инсулину, способствовать профилактике и лечению сахарного диабета 2-го типа, снижать холестерин и улучшать липидный спектр. Из всех сартанов только телмисартан — единственный сартан, для которого доказаны эффективность в защите от развития инфаркта и инсульта, а также снижение смертности от этих событий на уровне «золотого стандарта» рамиприла.
- Телмисартан в отличие от других сартанов за счет агонизма к PPAR-рецепторам останавливал прогрессирование диабетической нефропатии, а в 21,2 % случаев обращал ее вспять. Диабетическая нефропатия — болезнь, которая при прогрессировании переходит в хроническую почечную недостаточность. К тому же телмисартан улучшал работу сосудистой системы почек и повышал почечную перфузию лучше рамиприла (!) у больных с нефропатией и сахарным диабетом 2 типа.
- Телмисартан из всех сартанов является наиболее липофильным и, следовательно, лучше всего проникает глубоко в ткани, обеспечивая как местную (тканевую), так и системную блокаду рецепторов ангиотензина II (AT1 рецепторов). У телмисартана самый длительный период полувыведения среди сартанов — более 20 ч. Это обеспечивает надежное и круглосуточное блокирование (AT1 рецепторов).
- Телмисартан в отличие от других сартанов потенциально может играть защитную роль против печеночной инсулинорезистентности при диабете за счет агонизма к PPARγ-рецепторам.
- При ССЗ конечные продукты гликирования (КПГ) вызывают формирование «сшивок» с аминогруппами коллагена, что является причиной потери эластичности сосудов и захвата ЛПНП стенками артерий. КПГ также могут вызывать гликирование ЛПНП, что может способствовать их окислению и развитию атеросклероза. Более того КПГ могут связываться с рецепторами КПГ, что вызывает оксидативный стресс и активацию воспалительных реакций в эндотелиальных клетках сосудов. Телмисартан в отличии от других сартанов мощно снижает уровень рецепторов КПГ у пациентов с эссенциальной гипертензией.
- Телмисартан в отличии от других сартанов повышает выносливость в беге и других аэробных упражнениях через активацию с ppar-δ/AMPK пути.
- Телмисартан в отличии от других сартанов подавляет воспаления в сосудах (снижает с-реактивный белок) через активацию PPAR и ингибирование NF-kb.
- Телмисартан в отличии от других сартанов защищает сосуды, модулируя функцию эндотелия сосудов, через повышение митохондриальной активности, активируя AMPK.
- Сегодня показано, что ангиотензин II способен вызывать деменцию у крыс, схожую с болезнью Альцгеймера. Телмисартан в отличие от лекарств для снижения давления группы иАПФ, связан со значительным сокращением заболеваемости и прогрессирования болезни Альцгеймера даже в низких дозах, не снижающих артериальное давление — за счёт активации PPAR.
- Телмисартан в отличии от других сартанов имеет мощный антипролиферативный эффект в отношении клеток рака простаты через активацию PPARγ-рецепторов. И может быть мощным средством для профилактики и лечения рака простаты, что предстоит выяснить в клинических исследованиях.
- Телмисартан вызывает торможение пролиферации клеток рака толстой кишки грызунов.
- Телмисартан уникальный сартан в отличии от других сартанов за счет агонизма к PPAR значительно увеличивает количество и функциональную активность эндотелиальных прогениторных клеток. Эндотелиальные прогениторные клетки (ЭПК), полученные из костного мозга, способствуют ремонту эндотелия сосудов, защищают КИМ сосудов от утолщения.
- Телмисартан предупреждает рак печени у крыс, страдающих неалкогольной жировой дистрофией печени.
- Миостатин негативно регулирует работу скелетных мышц. Его удаление с помощью генетических вмешательств вызывает избыточный рост мышц, а, наоборот, его избыточная активность приводит к атрофии мышц. Телмисартан подавляет миостатин и защищают от саркопении (снижение мышечной массы при старении). Также телмисартан через активацию PPARγ-рецепторов позволяет повышать чувствительность к инсулину — гормону, который регулирует уровень глюкозы в крови, что способствует уменьшению межмышечного жира. А межмышечный жир — одна из причин снижения мышечной массы с возрастом.
- Телмисартан продается в аптеках России под названиями: Микардис, Телмиста, Телзап. Употреблять (только если назначит врач!!!) по 1 таблетке 1 раз в сутки на ночь. Дозировка для людей с нормальным и умеренно пониженным артериальным давлением от 10 до 40 мг. Для людей с повышенным артериальным давлением от 40 и выше — дозу подбирать в зависимости от уровня артериального давления. Стратегия и тактика его применения описана здесь.
Учёный исследователь и мой друг Александр Фединцев (координатор исследований в НИИ Антимикробной Химиотерапии) активно изучает сартаны и их влияние на продолжительность жизни. Именно с его разрешения и была написана эта статья, так как он один из первых в России, кто пытается раскрыть потенциал этой группы лекарств для продления жизни.
Автор статьи nestarenieRU научный директор OPENLONGEVITY — Веремеенко Дмитрий Евгеньевич (фото слева), автор книги «Диагностика старения« . Тел. +7 925 9244328 [email protected]
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.
Знаете ли вы, что сайт nestarenie.ru — объективно один из самых популярных в России ресурсов про старение и долголетие — в Яндексе, в Гугле, по количеству, качеству и лояльности аудитории. nestarenie.ru имеет потенциал, чтобы стать одним из самых популярных сайтов о борьбе со старением не только в России, но и в мире. Для этого нужны деньги. Я призываю всех сделать пожертвования, а также убедить своих друзей поступить аналогично.
- Яндекс.Кошелек 410012847316235
- Карта в Сбере (рубли): 4817 7602 3256 2458 (Чангакрам М.)
Узнайте подробнее помочь развитию блога.
Рекомендуем ещё почитать следующие статьи:
- Метформин — самое изученное и надёжное лекарство от старости при инсулинорезистентности.
- Подробная программа продления жизни научно обоснованными способами.
- Витамин K2 (МК-7) сокращает смертность
- Витамин B6+магний снижают смертность на 34%
- Глюкозамин Сульфат эффективно продлевает жизнь и защищает от многих видов рака у людей с повышенным уровнем воспаления.
Применение иАПФ при бронхообструктивных заболеваниях: безопасность и нежелательные лекарственные реакции | Архипов
Более 20 лет назад J. Havelka с соавт. опубликовали первое сообщение о появлении сухого кашля у лиц, принимавших каптоприл [1]. Однако потребовалось еще несколько лет, для того чтобы корректно доказать взаимосвязь между кашлем и применением ингибиторов АПФ (иАПФ) [2]. Параллельно с этим возникло несколько дополнительных вопросов:
- Насколько безопасным является применение иАПФ у больных бронхообструктивными заболеваниями?
- Существуют ли у иАПФ другие НЛР, связанные с респираторной системой?
Решение этих вопросов потребовало длительного времени и стало предметом целого ряда интересных исследований. Настоящий обзор ставит своей целью познакомить читателя с результатами имеющихся исследований и обобщить имеющиеся данные в виде практических рекомендаций. Поиск информации проводился в базах данных PubMed и MdConsult (1980-2003), кроме того, в настоящем обзоре использованы данные о частоте нежелательных лекарственных реакций (НЛР) отдельных препаратов по материалам Physicians’ Desk Reference [3].
Кашель при применении иАПФФизиологические аспекты
Кашель является наиболее частой НЛР со стороны системы органов дыхания, возникающей при использовании иАПФ [3]. Эта НЛР была зарегистрирована при использовании всех препаратов данной группы.
Механизм развития кашля у лиц, принимающих иАПФ, еще полностью не установлен. Принято считать, что влияние иАПФ на бронхолегочную систему реализуется за счет накопления двух ключевых факторов: ангиотензина II и брадикинина. Ангиотензинконвертирующий фермент регулирует баланс между этими физиологически активными медиаторами: увеличивает концентрацию ангиотензина II и одновременно метаболизирует брадикинин, снижая его концентрацию.
Наличие ангиотензин-превращающего фермента в ткани легких было продемонстрировано в целом ряде исследований. Следует отметить, что у больных бронхиальной астмой (БА) уровень ангиотензинпревращающего фермента в дыхательных путях значительно ниже, чем у здоровых лиц. В том случае, если больной астмой получает лечение глюкокортикостероидами, это приводит к увеличению концентрации ангиотензин-превращающего фермента в дыхательных путях [4].
Большинство исследователей считают, что появление кашля при приеме иАПФ происходит благодаря накоплению в эпителии бронхов брадикинина [5, 6, 7]. У больных БА брадикинин может вызывать не только кашель, но и эпизоды бронхообструкции [8]. Кинины, в свою очередь, стимулируют избыточную продукцию простагландинов и тромбоксанов, которые также могут вызывать кашель, стимулируя центростремительные нервные волокна в дыхательных путях. Возможная роль тромбоксанов (продукты арахидоновой кислоты) изучалась в двойном слепом перекрестном исследовании у 9 больных, отмечавших кашель при приеме эналаприла. Назначение этим больным пикотамида (ингибитор тромбоксансинтетазы и антагонист тромбоксановых рецепторов) у 8 из 9 пациентов привело к исчезновению кашля уже спустя 72 ч [9]. Действие препарата продолжалось до 6 мес. Озагрель – ингибитор тробоксан A2 синтетазы также уменьшает кашель, вызванный ингибиторами АПФ [10].
Нестероидные противовоспалительные средства (индометацин и сулиндак) уменьшают выраженность кашля, связанного с приемом иАПФ примерно в 50% случаев [11, 12].
Кроме того, наряду с кининами, ангиотензинконвертирующий фермент участвует в метаболизме субстанции Р. Таким образом, применение иАПФ создает условия для избыточного накопления субстанции Р в ткани легкого [13]. Баклофен – вещество со спазмолитическим действием, обладает способностью уменьшать синтез субстанции Р [14]. В одном открытом исследовании применение этого лекарственного средства (ЛС) у больных с кашлем на фоне приема иАПФ позволило уменьшить выраженность кашля, причем эффект препарата сохранялся от 25 до 74 дней после прекращения лечения [15].
Наконец, иАПФ увеличивают продукцию NO в дыхательных путях [16], что также может стимулировать кашлевой рефлекс и бронхоспазм [17]. Несмотря на эти данные, остается без ответа вопрос, почему кашель возникает не у всех больных, принимающих иАПФ. Индивидуальные различия в этом случае пытались объяснить генетическим полиморфизмом ферментов, превращающих ангиотензин I в ангиотензин II и рецепторов брадикинина. Однако найти адекватное объяснение пока не удается [18].
Клинические особенности кашля как НЛР при приеме иАПФМожно выделить несколько основных характеристик кашля, вызванного ингибиторами АПФ:
- кашель обычно возникает в 1-2-ю нед. лечения, однако его появление может отмечаться и через 6 мес. после начала лечения;
- женщины, применяющие иАПФ, жалуются на кашель значительно чаще, чем мужчины;
- люди некоторых национальностей более подвержены этой НЛР. Например, среди китайцев, получавших иАПФ, кашель отмечали до 50% больных [19];
- после отмены иАПФ кашель прекращается спустя 1-4 дня, но в редких случаях может продолжаться до 4 нед. [20];
- кроме кашля или наряду с ним у ряда больных могут возникать эпизоды одышки и бронхоспазма. В частности, уже в одном из первых отчетов по этой НЛР сообщалось, что у 2 из 59 больных, предъявляющих жалобы на кашель при приеме иАПФ, помимо кашля также отмечались сухие хрипы в легких [2];
- у больных бронхиальной астмой кашель при приеме иАПФ возникает не чаще, чем у других категорий больных [21];
- замена одного ингибитора АПФ на другое ЛС этой же группы чаще всего не позволяет избежать развития кашля. То же относится к бронхообструкции, вызванной ингибиторами АПФ [21].
Сухой кашель отмечается у 5-39% больных, получающих иАПФ [5] (по другим данным, – до 20% [6]). Среди амбулаторных больных, принимающих иАПФ по поводу артериальной гипертензии, длительный сухой кашель встречается в 19% случаев (у аналогичных больных, не принимавших иАПФ, – только в 9% случаев) [5].
В крупных клинических исследованиях иАПФ частота этой НЛР у различных препаратов существенно отличалась. В целом, наиболее часто кашель возникает при использовании периндоприла и рамиприла, у других препаратов частота этой НЛР существенно ниже. Наименьшая частота кашля, как НЛР при приеме препарата, отмечалась в исследовании лизиноприла у больных ХСН – менее 1%. Вместе с тем, во всех этих исследованиях доля больных, у которых иАПФ были отменены из-за развития кашля, не превышала 1% (см. табл. 1).
Таблица 1. Частота кашля у больных, принимавших иАПФ [3]
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Частота возникновения кашля у больных, получавших иАПФ, существенно отличалась в зависимости от основного заболевания. Так, при исследовании эналаприла у больных с артериальной гипертензией (АГ) кашель отмечался почти в 2 раза реже, чем в другом исследовании у лиц, страдавших хронической сердечной недостаточностью (ХСН). Однако, если при лечении артериальной гипертензии примерно 1/10 больных, отметивших появление кашля, была вынуждена прервать терапию эналаприлом, то у больных ХСН, несмотря на большую распространенность кашля, случаев отмены препарата из-за этой НЛР не было. При использовании лизиноприла частота появления кашля оказалась значительно выше у больных с АГ (3,5%) по сравнению с больными ХСН (>>1%) [22].
Исследование Ravid с соавт. [23] также выявило существенные различия в частоте развития кашля между пациентами, получающими иАПФ для лечения АГ (n = 164), и пациентов, получающих эти ЛС для терапии ХСН (n = 104). В ходе исследования кашель развивался у 23 больных АГ (14%) и у 27 больных ХСН (26%). Отменить иАПФ из-за выраженного кашля пришлось у 4,0% с АГ и у 18% с ХСН.
Достаточно трудно в каждом конкретном случае объективно высказаться о взаимосвязи между таким распространенным симптомом, как кашель, и приемом иАПФ. Например, среди больных, получавших периндоприл по поводу АГ (n=789), появление кашля отметили 12% пациентов, но лишь в 6% исследователи расценили связь этого симптома с приемом препарата как ‘возможную’ или ‘вероятную’ [22].
Лечебная тактика при возникновении у больного кашляСуществует несколько лечебных стратегий при возникновении у пациента кашля, обусловленного применением иАПФ. Все эти подходы поддерживаются современными консенсусами по терапии артериальной гипертензии и ХСН.
- Отмена препарата и назначение антагонистов рецепторов ангиотензина II.
- Снижение дозы с последующей оценкой клини ческой ситуации спустя 4-7 дней [6].
В 2001 г. исследователи из Samsung Medical Center (Южная Корея) опубликовали данные небольшого (n=19) плацебоконтролируемого исследования, которые свидетельствуют о положительном влиянии препаратов железа на кашель, возникший вследствие приема ингибитором АПФ. Оказалось, что прием сульфата железа в суточной дозе 256 мг в течение 4 нед. уменьшает выраженность кашля, оцениваемую по специальному опроснику в баллах. В группе больных, получавших сульфат железа, выраженность кашля снизилась с 3,07±0,70 до 1,69±1,10 баллов (р<0,01). В группе больных, получавших плацебо, существенных изменений не произошло (выраженность кашля до и после лечения составила 2,57±0,80 и 2,35±1,22 соответственно[24]. Предположительно объяснить влияние препаратов железа на больных с кашлем, вызванным ингибиторами АПФ, можно следующим образом: увеличение клеточной концентрации ионов железа снижает активность NO-синтетазы [25] и, следовательно, продукцию NO. Влияние NO на кашель у больных, принимающих иАПФ, было рассмотрено выше.
Вопрос о применении препаратов железа в данном случае нуждается в дополнительных исследованиях.
Бронхоспазм при приеме иАПФПомимо кашля, иАПФ способны вызвать и другие НЛР со стороны системы органов дыхания: приступы бронхиальной астмы, бронхоспазм и одышку.
Бронхообструктивный синдром при приеме иАПФ чаще всего развивается у лиц, страдающийх БА. Вместе с тем описаны случаи, когда прием каптоприла вызывал типичные для обострения БА симптомы у больных, которые ранее не предъявляли жалобы на затрудненное дыхание и не страдали аллергией [26].
Эти НЛР следует отнести к числу очень редких – 1:6200 назначений иАПФ. Согласно шведской статистике, одышка и бронхообструкция отмечаются у больных, принимавших иАПФ в 8-10 раз реже, чем кашель.
Одышка и бронхоспазм при приеме иАПФ в 50% случаев возникают в течение первых 2 нед. лечения.
Несмотря на то, что возникновение бронхоспазма – очень редкое НЛР, оно протекает тяжело и часто требует госпитализации [21].
Механизм развития бронхоспазма у больных, получавших иАПФ, вероятно, также связан с активацией кининов и продуктов метаболизма арахидоновой кислоты и имеет много общего с механизмами развития бронхообструкции у больных БА. В частности, важную роль в механизме развития этих НЛР играет бронхиальная гиперреактивность.
В качестве доказательства последнего положения можно упомянуть результаты исследования, в которое были включены больные, получавшие эналаприл. Оказалось, что после приема эналаприла у восприимчивых (отмечавших кашель) больных происходило снижение PС20 в бронхопровокационной пробе с гистамином [27] (PС20 — концентрация гистамина, вызывающая снижение объема форсированного выдоха за первую секунду на 20% по сравнению с исходной величиной).
Если отдельные препараты могут существенно отличаться между собой по частоте возникновения кашля, то для таких НЛР, как бронхообструкция и одышка, выявить подобные различия очень трудно. Например, Международная система информации о ЛС ВОЗ насчитывает 2468 рапортов о бронхообструкции на фоне приема каптоприла. Для эналаприла и лизиноприла число аналогичных сообщений составляет 4176 и 1318 соответственно. Однако на различия между этими цифрами закономерно влияют различия в интенсивности применения препаратов. Опираясь на шведские данные (см. рис. 1), можно продемонстрировать четкую связь между интенсивностью приема ЛС и числом сообщений о НЛР.
| Рис. 1 |
К сожалению, влияние иАПФ на функцию бронхолегочной системы у больных БА и ХОБЛ изучено недостаточно. Этот вопрос был объектом ограниченного количества небольших исследований (табл. 2) или описаний отдельных клинических случаев. При этом полученные данные часто являются уязвимыми, с точки зрения статистики и методологии, и приводят к противоречивым выводам.
Таблица 2. Исследования безопасности применения иАПФ у больных бронхообструктивными заболеваниями
|
Примечание: БА – бронхиальная астма; ХОБЛ – хроническая обструктивная болезнь легких; АГ – артериальная гипертензия; БК – бронхоконстрикция; ПИ – проспективное исследование; РПКП — рандомизированное плацебоконтролируемое исследование с перекрестным дизайном; РИСК — ретроспективное исследование ‘случай-контроль’; РО – ретроспективный обзор; МТ – метахолиновый тест; ОФВ1 – объем форсированного выдоха за первую секунду; ПСВ – пиковая скорость выдоха; СМ – спирометрия.
В ряде имеющихся исследований не было выявлено никаких НЛР иАПФ. Обычно это небольшие и краткосрочные исследования [28, 29].
В целом проблема выявления НЛР иАПФ у больных бронхообструктивными заболеваниями представляется достаточно сложной:
- для того чтобы дифференцировать кашель и другие НЛР при приеме иАПФ от проявлений основного заболевания, требуется значительная статистическая мощность исследования и значительный объем выборки;
- применение больными глюкокортикостероидов и бронхолитиков по поводу основного заболевания теоретически могут маскировать НЛР иАПФ;
- в крупных клинических исследованиях иАПФ, как правило, практически не участвовали больные со смешанной патологией, поэтому, опираясь на данные этих исследований, нельзя сказать, насколько безопасными являются эти препараты для больных БА и ХОБЛ.
В одном из более ранних исследований Sala с соавт. [28] не выявили изменений объема форсированного выдоха и бронхопровокационных тестов после 4 нед. применения каптоприла у 16 больных БА. В другом исследовании Schalekamp с соавт. [30] у больных ХОБЛ лечение каптоприлом в течение 60 дней также не привело к значимым изменениям показателей спирометрии. Это исследование также опиралось на ограниченное количество больных (19 больных) и было некорректно спланировано: у 9 пациентов исследовались эффекты только первой дозы препарата, в то время как у остальных 10 пациентов спирометрические данные оценивались после 60 дней лечения. В этом исследовании у каптоприла не было выявлено никаких НЛР, связанных с респираторной системой.
Одно из немногих двойных слепых исследований, посвященных этой теме, было выполнено Riska с соавт. [29] в 1987 г. Исследование не выявило никаких различий в данных спирометрии, полученных у больных БА после 8 нед. терапии каптоприлом и верапамилом. При этом больные в ходе исследования наряду с изучаемыми препаратами принимали глюкокортикостероиды и бронхолитики.
В другом двойном слепом исследовании Kaufman с соавт. [31] оценивали функцию легких у 21 пациента (14 больных БА и 7 больных аллергическим ринитом) до и после приема эналаприла и спираприла в течение 12 нед. Авторы не сообщили о существенном изменении спирометрических показателей или данных бронхопровокационных тестов. В этом исследовании также допускался прием противоастматических препаратов.
В очень небольшом (6 больных БА) исследовании Mue с соавт. [32] также не выявили изменений в данных спирометрии и сывороточном уровне субстанции Р при приеме эналаприла от 2 до 4 нед.
С другой стороны, большое популяционное исследование Lunde с соавт. [21], опирающееся на статистику ВОЗ и Шведского комитета по неблагоприятным лекарственным реакциям (с 1981 до 1991 г.), выявило большое количество НЛР иАПФ у больных с бронхообструктивными заболеваниями.
Данные этого исследования позволяют сделать вывод о том, что бронхообструкция при приеме иАПФ чаще возникает именно у больных БА. Так, из 36 НЛР в виде бронхоспазма и одышки, возникавших после приема иАПФ, которые были зафиксированы в Швеции за несколько лет, 12 отмечались у больных бронхиальной астмой [21]. С другой стороны, наличие у больного ХОБЛ, по-видимому, не влияло на риск возникновения подобных НЛР.
Из числа более крупных клинических исследований безопасности иАПФ у больных с бронхообструкцией следует упомянуть крупное когортное постмаркетинговое исследование (публикация Wood R. [33]), включающее 4646 больных. Оказалось, что у пациентов, получавших иАПФ, кашель отмечался значительно чаще, чем у больных, принимавших бензафибрат (12,3 vs 2,7% соответственно; p < 0,0001). Наряду с этим пациенты, у которых ранее имела место бронхиальная астма или бронхоспазм, статистически значимо не отличались от остальных пациентов по риску развития кашля и одышки (16 vs 13% соответственно; p = 0,447).
В раннее цитировавшемся исследовании Ravid с соавт. [23] было включено 56 больных ХОБЛ и 9 больных БА. Кашель отмечался у 17,9% пациентов ХОБЛ, при этом половина этих пациентов была вынуждена прекратить лечение ингибиторами АПФ. У больных с астмой кашель развился только у 1 больного из 9 и отмены препарата не потребовал. У многих пациентов кашель впоследствии уменьшился и даже исчез без прекращения терапии ингибиторами АПФ. Развитие бронхоспазма не было зарегистрировано в этом исследовании ни у одного больного.
Выводы- Кашель возникает при применении любых иАПФ, хотя отдельные препараты могут отличаться по частоте развития этой НЛР. Так, в крупных рандомизированных исследованиях минимальная частота развития кашля при длительном лечении ингибиторами АПФ наблюдалась при использовании лизиноприла (у больных ХСН) и эналаприла (при лечении АГ).
- Развитие кашля у больного, получающего иАПФ, не всегда требует отмены препарата (в крупных рандомизированных исследованиях отмена препарата оказалась необходимой не чаще чем у 1% больных). Кашель, возникший при приеме иАПФ, может регрессировать самостоятельно. Существует ряд ЛС средств, для которых было доказано положительное влияние на выраженность кашля, однако внедрение этих ЛС в клиническую практику требует дополнительных исследований.
- Длительное применение иАПФ у больных БА может приводить к обострениям БА и появлению одышки. Вместе с тем у больных ХОБЛ эти ЛС, по-видимому, относительно безопасны. Адекватная терапия БА (применение глюкокортикостероидов и бронхолитиков), вероятно, снижает риск НЛР со стороны иАПФ. Развитие бронхоспазма и обострений БА у больных, принимающих иАПФ, относится к числу редких НЛР (отмечается в 10 раз реже, чем кашель), но требует внимания со стороны врачей.
- Вместе с тем, клинических данных о безопасности иАПФ у больных БА и ХОБЛ на сегодняшний день недостаточно, что требует проведения дополнительных клинических и эпидемиологических исследований [34].
1. Havelka J., Vetter H., Studer A. et al. Acute and chronic effects of angiotensin-converting enzyme inhibitor captopril in severe hypertension. Am J Cardiol 1982; 49:1467–1474.
2. Coulter D.M., Edwards I.R. Cough associated with captopril and enalapril. BMJ 1987; 194:1521–1523.
3. Physicians’ Desk Reference. 2000 (54th edition)/www.pdr.net
4. Roisman G.L. et al. Decreased expression of angiotensin-converting enzyme in the airway epithelium of asthmatic subjects is associated with eosinophil inflammation. J Allergy Clin Immunol 1999;104:402-10.
5. Sebastian J.L., McKinney W.P., Kaufman J., Young M.J. Angiotensin-converting enzyme inhibitors and cough: prevalence in an outpatient medical clinic population. Chest. 1991; 99: 36–39.
6. Israili Z.H., Hall W.D. Cough and angioneurotic edema associated with angiotensin-converting enzyme inhibitor therapy. Ann Intern Med. 1992; 117: 234–242.
7. Simon S.R., Black H.R., Moser M., Berland W.E. Cough and ACE inhibitors. Arch Intern Med. 1992; 152: 1698–1700.
8. Simonsson B.G., Skoogh B-E., Bergh N.P., Andersson R., Svedmyr N. In vivo and in vitro effect of bradykinin on bronchial motor tone in normal subjects and patients with airways obstruction. Respiration 1973;30:378-88.
9. Malini P.L., Strocchi E., Zanardi M. et al. Thromboxane antagonism and cough induced by angiotensin-converting-enzyme inhibitor. Lancet 1997; 350:15.
10. Unemure K., Nakashima M., Saruta T. Thromboxane A2 synthetase inhibition suppresses cough induced by angiotensin converting enzyme inhibitors. Life Sci 1997; 60:1583–1588.
11. Fogari R., Zoppa A., Tettamanti F. et al. Effects of nifedipine and indomethacin on cough induced by angiotensin) converting enzyme inhibitors: a double-blind, randomized, cross-over study. J Cardiovasc Pharmacol 1992; 19:670–673.
12. Gilchrist N.L., Richards A.M., March M. et al. Effects of sulindac on angiotensin converting enzyme inhibitor-induced cough: randomized placebo-controlled double-blind cross-over study. J Human Hypertens 1989; 3:451–455.
13. Cascieri M.A., Bull H.G., Mumford R.A., Patchett A.A., Thornberry N.A., Liang T. Carboxyl-terminal tripeptidyl hydrolysis of substance P by purified rabbit lung angiotensin-converting enzyme and the potentiation of substance P activity in vivo by captopril and MK-422. Mol Pharmacol. 1984; 25: 287–293.
14. Ray N.J., Jones A.J., Keen P. et al. GABA-B receptor modulation of the release of substance P from capsaicin-sensitive neurones in the rat trachea in vitro. Br J Pharmacol 1991; 102:801–804.
15. Dicpinigaitis P.V. Use of baclofen to suppress cough induced by angiotensin-converting enzyme inhibitors. Ann Pharmacother 1996; 30:1242–1245.
16. Linz W., Wohlfart P., Schoelkens B.A., Malinski T., Wiemer G. Interaction among ACE, kinins, and NO. Cardiovasc Res. 1999; 43: 549–561.
17. Silkoff P.E., Robbins R.A., Gaston B., Lundberg J.O., Townley R.G. Endogenous nitric oxide in allergic airway disease. J Allergy Clin Immunol. 2000; 105: 438–448.
18. Zee R.Y., Rao V.S., Paster R.Z. et al. Three candidate genes and angiotensin-converting enzyme inhibitor-related cough. A pharmacogenetic approach. Hypertension 1998; 31:925.
19. Woo K.S., Nicholls M.G. High prevalence of persistent cough with angiotensin converting enzyme inhibitors in Chinese. Br J Clin Pharmacol 1995; 40:141.
20. Yeo W.W., Chadwick I.G., Kraskiewicz M. et al. Resolution of ACE inhibitor cough: Changes in subjective cough and responses to inhaled capsaicin, intradermal bradykinin and substance-P. Br J Clin Pharmacol 1995; 40:423.
21. Lunde H., Hedner T., Samuelsson O. et al. Dyspnoea, asthma, and bronchospasm in relation to treatment with angiotensin converting enzyme. Br Med J 1994; 308:18.
22. Mosby’s Drug Consult/www.mdconsult.com
23. Ravid D., Lishner M., Lang R. et al. Angiotensin-converting enzyme inhibitors and cough: a prospective evaluation in hypertension and congestive heart failure. J Clin Pharmacol 1994; 34:1116–1120.
24. Lee S.C., Park S.W., Kim D.K., Lee S.H., Hong K.P. Iron supplementation inhibits cough associated with ACE inhibitors. Hypertension. 2001; 38: 166–170.
25. Zhang Y., Crichton R.R., Boelaert J.R., Jorens P.G., Herman A.G., Ward R.J., Lallemand F., de Witte P. Decreased release of nitric oxide by alveolar macrophages after in vivo loading of rats with either iron or ethanol. Biochem Pharmacol. 1998; 55: 21–25.
26. Popa V. Captopril-related (and induced?) asthma. Am Rev Respir Dis 1987; 136:999–1000.
27. Lindgren B.R., Rosenqvist U., Ekstrom T. et al. Increased bronchial reactivity and potentiated skin responses in hypertensive subjects suffering from coughs during ACE-inhibitor therapy. Chest, 1989; Vol 95: 1225-1230.
28. Sala H., Abad J., Juanmiquel L. et al. Captopril and bronchial reactivity. Postgrad Med J 1986; 62:76–77.
29. Riska H., Senius-Aarniala B., Sovijarvi A.R.A. Comparison of the effects of an angiotensin-converting enzyme inhibitor and a calcium channel blocker on blood pressure and respiratory function in patients with hypertension and asthma. J Cardiovasc Pharmacol 1987; 10(suppl 10):S79–S81.
30. Schalekamp M., Dietze G., Bertoli L. et al. Influence of ACE inhibition on pulmonary haemoydynamics and function in patients in whom в-blockers are contraindicated. Postgrad Med J 1986; 62:47–51.
31. Kaufman J., Schmitt S., Barnard J. et al. Angiotensin — converting enzyme inhibitors in patients with bronchial responsiveness and asthma. Chest 1992; 101:922–925.
32. Mue S., Tamura G., Yamauchi K. et al. Bronchial responses to enalapril in asthmatic, hypertensive patients. Clin Ther 1990; 12:335–343.
33. Wood R. Bronchospasm and cough as adverse reactions to ACE-inhibitors captopril, enalapril and lisinopril: a controlled retrospective cohort study. Br J Clin Pharmacol 1995; 39:265–270.
34. Dart R.A., Gollub S., Lazar J. et al. Treatment of Systemic Hypertension in Patients With Pulmonary Disease COPD and Asthma. Chest, 2003; Vol. 123, # 1 (January 2003)// www.mdcon-sult.com
35. Lin M., Yang Y.F., Lee D. et al. Comparisons of long-term effects of lisinopril vs nifedipine vs conventional therapy in the treatment of mild-to-moderate hypertension in patients with chronic obstructive pulmonary disease. Chinese Med J 1996; 57:392–400.
Ингибитор АПФ третьего поколения фозиноприл в лечении пациентов с сердечно-сосудистыми заболеваниями | Ермолаева А.С., Дралова О.В., Максимов М.Л.
Сердечно-сосудистые заболевания являются основной причиной смерти вЕвропе исоставляют более 4,3млн смертей ежегодно. Артериальная гипертензия (АГ) относится кчислу наиболее распространенных сердечно-сосудистых заболеваний (около 40% взрослого населения РФимеют повышенный уровень АД) иявляется важнейшим фактором риска развития основных сердечно-сосудистых осложнений, таких как инфаркт миокарда иострое нарушение мозгового кровообращения, определяющих высокую смертность виндустриально развитых странах [1–4].
Ренин-ангиотензин-альдостероновая система (РААС) рассматривается как основной фактор регуляции АД и гомеостаза, играет центральную роль в возникновении АГ и ее последствий, выступает в качестве непременного участника сердечно-сосудистого континуума, начиная с этапа воздействия факторов риска, потенциирования развития атеросклероза, эндотелиальной дисфункции, ишемической болезни сердца (ИБС), гипертрофии ЛЖ, ремоделирования миокарда и завершая финальной сердечной недостаточностью, а также развитием хронической болезни почек (ХБП) [5–9].
В настоящее время для лечения АГ рекомендованы 5 основных классов антигипертензивных препаратов: ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов ангиотензина II (БРА), блокаторы медленных кальциевых каналов (БМКК), b-адреноблокаторы (БАБ), диуретики [1, 10]. На фоне антигипертензивной терапии возможно изменение активности РААС. Одним из путей снижения ее активности является подавление синтеза ангиотензина II [11, 12].
иАПФ представляют собой высокоэффективные препараты, широко используемые в лечении сердечно-сосудистых заболеваний: АГ, ИБС, хронической сердечной недостаточности (ХСН). Актуальность их применения в практике лечения заболеваний сердечно-сосудистой системы обусловлена эффектами блокады нейрогуморальных систем, вазо-, кардио- и нефропротективными свойствами [11, 13, 14].
В течение последних лет неуклонно растет количество иАПФ, дифференцирующихся по фармакокинетическим свойствам, продолжительности действия, активности исходного препарата и степени тканевой биодоступности. По химическому строению препараты различаются по тому, какая химическая группа (сульфгидрильная, карбоксиалкильная, фосфинильная или гидроксамовая) в их молекуле связывается с ионом цинка в активных центрах ангиотензинпревращающего фермента [12, 14].
В основе клинически значимых фармакологических эффектов иАПФ лежит их способность подавлять активность фермента (АПФ или кининаза II), превращающего ангиотензин I в. ангиотензин II, и таким образом влиять на функционирование РААС. Ангиотензин II считается основным эффекторным звеном РААС [15, 16]. Ангиотензин II, активируя АТ1-рецепторы, обладает мощным вазоконстрикторным действием. Под воздействием ангиотензина II происходит сокращение гладкомышечных клеток, усиливается сократимость миокарда, повышается продукция альдостерона, а также экскреция катехоламинов из мозгового вещества надпочечников и симпатических нервных окончаний. Ангиотензин II также регулирует транспорт натрия с помощью эпителиоцитов кишечника и почек. В дополнение к физиологическим функциям локально продуцированный ангиотензин II вызывает воспаление, пролиферацию клеток, митоз, апоптоз, миграцию и дифференцирование клеток, регулирует генную экспрессию биоактивных веществ и активирует множественные внутриклеточные сигнальные пути, многие из которых способствуют повреждению тканей [9, 11, 17].
иАПФ снижают секрецию альдостерона и вазопрессина, препятствуют разрушению брадикинина. Брадикинин, накапливаясь в эндотелии, действуя через β2-рецепторы брадикинина, вызывает релаксацию гладких мышц сосудов и способствует высвобождению зависимого от эндотелия релаксирующего фактора и вазоактивных простагландинов (простациклина и простагландина Е2). Кроме того, под влиянием иАПФ снижается синтез других сосудосуживающих и антинатрийуретических веществ (норадреналина, аргинина-вазопрессина, эндотелина-1), участвующих в патогенезе кардиальной дисфункции и АГ. Основные органопротективные эффекты иАПФ обусловлены блокадой АПФ в различных тканях (например, сосудах, почках, сердце) [17, 18].
Различают следующие основные фармакологические эффекты иАПФ: гемодинамические, нейрогуморальные, антипролиферативные, почечные и др. [11, 17, 18].
Гемодинамический эффект иАПФ реализуется через их способность снижать общее периферическое сосудистое сопротивление, вызывать натрийурез, однако влияние на ЧСС невелико. Уменьшение тонуса периферических сосудов также происходит в результате блокады тканевого АПФ, что приводит к уменьшению содержания ангиотензина II в. органах-мишенях (например, сосудистой стенке). У пациентов с нормальным и повышенным АД без сердечной недостаточности иАПФ практически не влияют на минутный объем сердца и ударный объем. В отличие от других вазодилататоров иАПФ не вызывают рефлекторной тахикардии, по-видимому, за счет воздействия на барорецепторы, усиления парасимпатической активности и, возможно, уменьшения симпатической активности. Также не происходит изменений ЧСС во время физической нагрузки. Применение иАПФ улучшает способность кардиомиоцитов к релаксации. иАПФ уменьшают гипертрофию левых отделов сердца у пациентов с ИБС, АГ, страдающих инсулинонезависимым сахарным диабетом (СД) и сердечной недостаточностью. Также иАПФ уменьшают эндотелиальную дисфункцию. Данное свойство связывают с ослаблением вазоконстрикции и усилением выработки оксида азота в результате увеличения образования брадикинина при блокаде АПФ [5, 11, 16, 19].
У пациентов с ХСН иАПФ улучшают клиническую симптоматику, качество жизни, замедляют прогрессирование болезни и улучшают прогноз, а также предотвращают наступление клинически выраженной декомпенсации. Это обусловлено их способностью вызывать как артериальную, так и венозную вазодилатацию. Венозная вазодилатация повышает емкость венул, уменьшает нагрузку на правое предсердие, вследствие этого уменьшается давление в легочной вене, снижается нагрузка объемом левого желудочка и уменьшается застой по малому кругу кровообращения [12, 17, 20, 21].
Артериальная вазодилатация приводит к уменьшению периферического сосудистого сопротивления и увеличению сердечного выброса. Короткий курс приема иАПФ сопровождается уменьшением содержания ангиотензина II, однако по механизму отрицательной обратной связи увеличивается выброс ренина и уровень ангиотензина I. Ангиотензин II обладает мощным вазоконстрикторным действием на мускулатуру гладкомышечных клеток, усиливает сократимость миокарда, стимулирует продукцию альдостерона, активирует экскрецию катехоламинов из мозгового вещества надпочечников и из симпатических нервных окончаний, стимулирует симпатическую нервную систему, усиливает жажду и желание употреблять соленую пищу. Также ангиотензин II регулирует транспорт натрия с помощью эпителиоцитов кишечника и почек. Кроме того, иАПФ уменьшают содержание в плазме эпинефрина, норэпинефрина и вазопрессина [22, 23].
Помимо этого, к повышению уровня ангиотензина I приводит увеличение концентрации брадикинина, а также активация альтернативных путей превращения ангиотензина I в. ангиотензин II. Таким образом, применение иАПФ повышает уровень кининов, простациклина и окиси азота. При длительном применении иАПФ уменьшается выработка альдостерона, в норме стимулируемая гиперкалиемией, гипермагниемией и АКТГ, что приводит к усилению выведения натрия и воды [17, 22, 23].
При длительном применении иАПФ возникает антипролиферативный эффект: снижение гипертрофии мышечного слоя сосудистой стенки и миокарда, уменьшение пролиферации внеклеточного матрикса. Возможными механизмами действия иАПФ на уменьшение гипертрофии миокарда считаются: механическая причина за счет уменьшения преднагрузки и постнагрузки, а также уменьшение симпатической активности и снижение стимуляции роста. Кроме того, иАПФ уменьшают образование коллагена за счет уменьшения содержания ангиотензина II, который действует как непосредственно на фибробласты, так и косвенно за счет стимуляции секреции альдостерона. Торможение роста и пролиферации гладкомышечных клеток и фибробластов в медии артерий приводит к увеличению их просвета, а также восстановлению и улучшению эластичности артериальной стенки. Таким образом, нормализуется центральная гемодинамика и снижается периферическое сосудистое сопротивление [23, 24].
Известны относительно новые данные по объяснению антифибротического действия иАПФ на миокард при АГ. Исследователи считают, что этот эффект иАПФ является результатом блокады гидролиза N-ацетил-серил-аспартил-лизил-пролина, приводящей к уменьшению пролиферации фибробластов, воспалительных клеток, экспрессии трансформирующего фактора роста и отложению коллагена. Помимо этого, иАПФ препятствуют апоптозу кардиомиоцитов [25].
иАПФ оказывают благоприятный эффект на почки, т. к. расширяют преимущественно эфферентные артериолы и меньше влияют на афферентные. Таким образом снижается внутриклубочковое давление, уменьшается протеинурия, увеличивается почечный кровоток с незначительным изменением скорости клубочковой фильтрации. Несмотря на уменьшение сосудистого сопротивления в клубочках, скорость клубочковой фильтрации остается неизмененной или увеличивается вместе с фильтрационной фракцией. В результате улучшения почечной гемодинамики возрастает натрийурез, уменьшается выработка альдостерона, что приводит к замедлению прогрессирования нефропатии [14, 25].
РААС играет важную роль в патогенезе и прогрессировании атеросклероза. Таким образом, при назначении иАПФ замедляется развитие атеросклероза вследствие блокады образования ангиотензина II и увеличения концентрации брадикинина и оксида азота, которые улучшают эндотелиальную функцию [16, 24, 26, 27].
В опубликованном сравнительном анализе трех исследований (HOPE, EUROPA, PEACE) по влиянию иАПФ у 29 805 пациентов с наличием атеросклероза, но без дисфункции левого желудочка, на показатели общей смертности, фатальных и нефатальных сердечно-сосудистых событий показано, что назначение иАПФ приводит к достоверному снижению общей (7,8 против 8,9%, p=0,0004) и сердечно-сосудистой (4,3 против 5,2%, p=0,0002) смертности, нефатальных инфарктов миокарда (5,3 против 6,4%, p=0,0001), мозговых инсультов (2,2 против 2,8%, p=0,0004), сердечной недостаточности (2,1 против 2,7%, p=0,0007) и проведению аортокоронарного шунтирования (6,0 против 6,9%, p=0,0036). Авторы заключили, что назначение иАПФ должно быть рассмотрено у всех пациентов с промежуточным риском при наличии атеросклеротического процесса [28].
Таким образом, иАПФ показаны для лечения АГ (класс IA). У больных АГ первичной целью лечения является контроль АД, который может быть достигнут с помощью различных препаратов, снижающих риск сердечно-сосудистых осложнений при длительной терапии. иАПФ рассматривают также в качестве средств первой линии у больных с сердечной недостаточностью, систолической дисфункцией левого желудочка или СД, перенесших ИМ или инсульт, а также у пациентов группы высокого риска коронарной болезни сердца [1, 10, 11, 24, 28, 30].
За последние десятилетия исследованы более 30 химических соединений, относящихся к классу иАПФ. Одним из наиболее эффективных, безопасных и экономичных иАПФ является фозиноприл натрия (Моноприл). Клинически важным отличием фозиноприла от многих других иАПФ является наличие в его химической формуле остатков фосфинильной кислоты. Эта особенность структуры придает препарату ряд уникальных свойств, отличающих его от других препаратов данного класса, и позволяет отнести его к третьей, наиболее современной, генерации иАПФ [31, 32].
Фозиноприл является пролекарством и действует после всасывания и трансформации (в печени, слизистой ЖКТ, почках, кровяном русле) в активный метаболит — фозиноприлат, который связывается с белками плазмы крови (95–98%). Период полувыведения фозиноприла составляет 12–15 ч, что обусловливает его длительное антигипертензивное действие и прием 1 р./сут. Препарат отличается чрезвычайно высокой липофильностью — индекс липофильности фозиноприлата составляет более 2,0 ЕД, тогда как у эналаприлата — 0,108 ЕД. Это облегчает проникновение фозиноприлата через клеточные мембраны и позволяет подавлять активность не только циркулирующей, но и тканевой РААС в сердце, легких, почках и головном мозге. Экспериментально показано, что фозиноприлат ингибирует АПФ в сердечной мышце в большей степени, чем рамиприлат и эналаприлат, что лежит в основе более выраженного (по сравнению с другими иАПФ) гипотензивного и кардиопротективного эффектов. В отличие от других иАПФ (каптоприла, эналаприла, лизиноприла и др.), которые выводятся из организма преимущественно почками, для фозиноприла характерны два основных пути элиминации — почечный и печеночный (с желчью) в соотношении 1:1. Причем при снижении функции почек увеличивается выведение активного метаболита с желчью и, наоборот, при печеночной недостаточности возрастает его экскреция с мочой [33–36]. Это делает препарат наиболее эффективным у пожилых, а также у пациентов с патологией печени и почек.
Клинически значимым преимуществом фозиноприла, отличающим его от большинства других иАПФ, является хорошая переносимость. Так, у больных с ХСН II–IV функционального класса по классификации NYHA частота побочных эффектов при применении фозиноприла и плацебо практически не отличалась. Отмечается крайне низкая частота возникновения сухого кашля. Отмечено, что сухой кашель, вызываемый другими иАПФ, ослабевает или даже полностью исчезает при переходе на фозиноприл. Так, в двойном слепом сравнительном исследовании с эналаприлом показано достоверно более редкое возникновение кашля при назначении фозиноприла. В это исследование были включены 179 больных, уже прекративших прием иАПФ из-за развития кашля. Попытка возобновления лечения была гораздо более успешной при выборе фозиноприла — повторное развитие кашля наблюдалось более чем вдвое реже по сравнению с эналаприлом. Также при его применении наблюдается меньшее число клинических и биохимических побочных эффектов, особенно в «группах риска» — у пожилых гипертоников или больных СД. Фозиноприл отличает и удобный режим дозирования — однократный прием обеспечивает 24-часовой контроль АД (соотношение остаточного к пиковому эффекту — 64%) и предотвращает его повышение в ранние утренние часы. Начальная суточная доза фозиноприла при АГ составляет 10 мг однократно с возможным последующим увеличением до 20–40 мг. При ХСН начальная суточная доза — 5–10 мг (у больных с гипотонией — 2,5–5 мг), средняя терапевтическая — 10–20 мг, максимальная — 20–40 мг [33, 34, 37–41].
В исследовании FOPS (757 больных старше 60 лет) целевой уровень АД за 12 нед. лечения фозиноприлом был достигнут у 80% пациентов, причем части из них дополнительно назначали 12,5 мг гидрохлоротиазида для достижения лучшего терапевтического результата. В исследовании FLIGHT (19 432 больных с АГ, 989 из них — старше 75 лет) через 12 нед. от начала лечения целевое АД было достигнуто у 79,8% пациентов. Отмечено, что антигипертензивная активность фозиноприла постепенно возрастает в первые несколько недель лечения, АД чаще достигает целевых уровней без проявления элементов компенсаторных нарушений сердечного ритма, а отмена препарата не приводит к быстрому подъему АД. Действие фозиноприла, как правило, не зависит от возрастно-половых особенностей и массы тела больных [42–44].
При проведении российской программы ФЛАГ (Фозиноприл при Лечении Артериальной Гипертонии) оценивалась вероятность достижения целевых уровней АД у больных с мягкой и умеренной АГ в амбулаторных условиях при монотерапии фозиноприлом (10–20 мг/сут) или его сочетании с гидрохлоротиазидом. Всего в исследование были включены 2557 пациентов, из которых 26,7% составили лица старше 60 лет. Целевое АД достигнуто у 62,1% пациентов. Побочные эффекты отмечены у 8,3% больных, причем только у 5,2% потребовалась отмена препаратов [45].
В исследование ФАГОТ (Фармакоэкономическая оценка использования иАПФ фозиноприла в амбулаторном лечении больных Артериальной Гипертензией Осложненного Течения) были включены 2596 пациентов с мягкой или умеренной АГ и наличием двух факторов риска сердечно-сосудистых осложнений. Сравнивалась эффективность монотерапии фозиноприлом или его сочетания с гидрохлоротиазидом и общепринятой терапии (диуретиками, БАБ, антагонистами кальция) у пациентов разного возраста. Целевое АД при приеме фозиноприла и гидрохлоротиазида достигнуто у 67,8% пациентов. Показано, что скорость достижения гипотензивного эффекта и его выраженность при применении фозиноприла не различаются у пациентов пожилого и молодого возраста, но выше, чем при использовании традиционной схемы лечения. По сравнению с другими препаратами фозиноприл выгодно отличала простота приема и затратная экономичность [46].
Фозиноприл является эффективным в предупреждении и обратном развитии гипертрофии левого желудочка (ЛЖ) при АГ, т. е. он не только снижает АД, но и способствует регрессу структурного ремоделирования камер сердца. В течение 9 мес. масса миокарда ЛЖ снижается у лиц с выраженной гипертрофией на 5 г, а в группе сравнения — нарастает. Подобное наблюдение очень важно, поскольку гипертрофия стенки ЛЖ — один из ключевых предикторов сердечно-сосудистых катастроф. Препарат также благоприятно воздействует на течение атеросклероза сонных артерий. Показано, что толщина комплекса интима-медиа в этом участке сосудистого русла через 36 нед. регулярного приема препарата снижается на 0,0278±0,03 мм, в то время как вне приема фозиноприла данный показатель только увеличивается.
Результаты двойного слепого плацебо-контролируемого исследования PHYLLIS продемонстрировали тормозящий эффект терапии фозиноприлом (20 мг/сут) на прогрессирование атеросклероза сосудов каротидного бассейна, т. е. антиатерогенное действие. В исследовании участвовали 508 больных АГ с бессимптомным атеросклеротическим поражением сонных артерий и их крупных ветвей. Средний срок наблюдения составил 2,6 года. Толщина комплекса интима-медиа, как и зона атеросклеротического поражения, у больных, принимавших фозиноприл, достоверно и сходно уменьшалась. Таким образом, уже в нескольких исследованиях продемонстрировано, что фозиноприл оказывает антиатерогенное действие у больных АГ, по крайней мере на отдельных участках сосудистого русла [42, 47, 48].
Фозиноприл также способен улучшать диастолическую функцию ЛЖ у молодых лиц с мягкой АГ без гипертрофии стенки ЛЖ. В исследовании приняли участие 66 молодых людей (средний возраст 36 лет) со средней продолжительностью АГ, согласно медицинской документации, 5,4 года. Доза фозиноприла составила 20 мг/сут. Группа контроля получала комбинацию гидрохлоротиазида и гидралазина. Монотерапия фозиноприлом продемонстрировала неоспоримые преимущества в нормализации диастолической функции ЛЖ и профилактике гипертрофии ЛЖ [49].
Для подтверждения собственного нефропротективного эффекта фозиноприла, не связанного со снижением АД, проведено исследование PREVEND IT (Prevention of Renal Vascular End-Stage Disease Intervention Trial). Исследование включало 854 пациента с микроальбуминурией, которым назначали 2 препарата в течение 46 мес.: правастатин и фозиноприл, каждый из которых имел плацебо-контроль. Основной целью данного исследования была оценка влияния фозиноприла и правастатина на сердечно-сосудистые осложнения и почечную недостаточность у больных с микроальбуминурией, нормальным уровнем АД и общего холестерина. За первые 3 мес. уровень альбуминурии существенно снизился у больных, получавших фозиноприл, что сохранялось на протяжении 4 лет наблюдения. Применение правастатина не сопровождалось изменением микроальбуминурии. В сравнении с плацебо фозиноприл уменьшил риск инсульта, но не влиял на риск инфаркта миокарда [30, 33, 34].
Применение фозиноприла — длительно действующего иАПФ, характеризующегося взаимно компенсирующимися путями экскреции с мочой и желчью, — сопряжено с минимальным риском кумуляции при хронической почечной недостаточности, в т. ч. выраженной (клиренс эндогенного креатинина <30 мл/мин). Аргументом в пользу выбора именно этого препарата у больных ХСН с исходными гиперкреатининемией и/или снижением СКФ является установленный в клинических исследованиях минимальный по сравнению с другими иАПФ риск нарастания сывороточных концентраций креатинина и калия. У пожилых больных с изолированной систолической АГ (исследование FOPS), у которых вероятность провокации ухудшения функции почек иАПФ максимальна, применение фозиноприла не было сопряжено с появлением признаков почечной недостаточности. Безопасность фозиноприла с точки зрения влияния на функцию почек установлена и в крупных отечественных контролируемых исследованиях (проект «Три Ф») [37, 50–53].
При сравнении фозиноприла и нифедипина в виде длительно действующей гастроинтестинальной терапевтической системы (ГИТС) у 241 больных с паренхиматозными заболеваниями почек и хронической почечной недостаточностью, у которых за предшествующий год наблюдалось удвоение уровня креатинина плазмы крови, проводилось лечение фозиноприлом 10–20 мг/сут в сравнении с нифедипином продленного действия 30–60 мг/сут. Конечными точками в исследовании выступали удвоение уровня креатинина и необходимость в гемодиализе. Через 3 года наблюдения 36% больных в группе, получавшей нифедипин, и 21% пациентов (p<0,05) в группе, получавшей фозиноприл, достигли конечной точки. При этом уровень протеинурии на фоне лечения фозиноприлом уменьшился на 57% от исходного, в группе терапии нифедипином — возрос на 7% [5, 45].
Заключение. иАПФ фозиноприл (Моноприл) — эффективный современный препарат, который позволяет не только достичь целевого уровня АД у пациентов с АГ, но также имеет доказанные кардио-, вазо- и нефропротективные эффекты и способен тормозить атеросклеротический процесс. Фозиноприл (Моноприл) может служить препаратом выбора в качестве гипотензивной терапии АГ у лиц всех возрастных групп. Для обеспечения оптимального органопротективного эффекта фозиноприл может с успехом применяться как в монотерапии, так и в комбинации, в т. ч. с тиазидными диуретиками или антагонистами кальция. Соединяя в себе разностороннюю эффективность, хорошую переносимость и простоту использования, фозиноприл может быть рекомендован для терапии пациентов с АГ, в т. ч. в сочетании с ХБП, ИБС и ХСН.
Литература
- Диагностика и лечение артериальной гипертензии: Российские рекомендации (четвертый пересмотр) // Системные гипертензии. 2010. № 3. С. 5–26.
- Чазова И.Е., Ратова Л. Г. Комбинированная терапия артериальной гипертонии: Руководство по артериальной гипертонии / Под ред. Е. И. Чазова, И. Е. Чазовой. М.: Медиа Медика, 2005. С. 784.
- Остроумова О.Д., Максимов М. Л. Выбор комбинации ингибиторов АПФ и диуретиков в лечении артериальной гипертензии в новой редакции российских рекомендаций: фокус на лечение пожилых пациентов // Фарматека. 2011. № 8. С. 42–49.
- Кобалава Ж.Д., Котовская Ю.В., Моисеев В. С. Артериальная гипертония. Ключи к диагностике и лечению: Серия «Библиотека врача-специалиста». М.: ГЭОТАР-Медиа, 2009. 864 с.
- Карпов Ю. А. Лечение больных сердечно-сосудистыми заболеваниями: роль блокады ренин-ангиотензиновой системы с помощью сартанов // РМЖ. 2009. № 23. С. 1548–1554.
- Мухин Н.А., Моисеев В.С., Кобалава Ж.Д. и др. Кардиоренальные взаимодействия: клиническое значение и роль в патогенезе заболеваний сердечно-сосудистой системы и почек // Тер. архив. 2004. № 6. С. 39–47.
- Медведев И.Н., Кумова Т.А., Гамолина О. В. Рольренин-ангиотензин-альдостероновой системы в развитии артериальной гипертонии // Российский кардиологический журнал. 2009. № 4. С. 82–84.
- Jacoby D.S., Rader D. J. Renin-angiotensin system and atherothrombotic disease: from genes to treatment // Arch. Intern. Med. 2003. Vol. 163(10). P. 1155–1164.
- Остроумова О.Д., Максимов М. Л. Место ингибиторов ангиотензин-превращающего фермента в лечении артериальной гипертонии у различных групп пациентов // Кардиоваскулярная терапия и профилактика. 2010. № 9 (7). С. 90–96.
- ESH-ESC Guidelines Committee. 2013 guidelines for the management of arterial hypertension // J. Hypertens. 2013. Vol. 31. P. 1281–1357.
- Клиническая фармакология / Под ред. В. Г. Кукеса. М.: ГЭОТАР-Медиа, 2013. 1056 с.
- Чазов Е.И., Чазова И. Е. Руководство по артериальной гипертонии. М., 2005. 734 с.
- Арутюнов Г.П., Чернявская Т. К. Проблемы нефропротекции у пациентов с артериальной гипертонией. Значение показателя микроальбуминурии для врача общей практики // Качество жизни. Медицина. 2005. № 3. С. 22–27.
- Рациональная фармакотерапия сердечно-сосудистых заболеваний: Рук. для практикующих врачей / Под общ. ред. Е. И. Чазова, Ю. Н. Беленкова. М.: Литтерра, 2005. 972 с. (Рациональная фармакотерапия: Сер. рук. для практикующих врачей; Т. 6).
- Таяновская Ю.В., Лелюк В.Г., Кутузова А.Б. и др. Методология и прикладное значение исследования функции эндотелия в общеклинической практике и клинике радиационной медицины // Эхография. 2001. Т. 2, № 4. С. 384–396.
- Беленков Ю.Н., Мареев В.Ю., Агеев Ф. Т. Эндотелиальная дисфункция при сердечной недостаточности: возможности терапии ингибиторами ангиотензинпревращающего фермента // Кардиология. 2001. № 5. С. 100–104.
- Метелица В. И. Клиническая фармакология сердечно-сосудистых лекарственных средств. М.: Миа, 2005. 926 с.
- Клиническая фармакология: национальное руководство (Серия «Национальные руководства»). М.: ГЭОТАР-Медиа, 2014. 976 с.
- Stella A., Zanchetti A. Control of renal renin release // Kidney Int. 1987. Vol. 31 (Suppl. 20). P. 89–94.
- Диагностика и лечение в кардиологии: учебн. пособие для студ. медвузов / Под ред. Майкла Х. Кроуфорда; пер. с англ. яз.; под общ. ред. акад. РАМН Р. Г. Оганова. М.: МЕДпресс-информ, 2007. 800 с.
- Алмазов В.А., Беркович О.А., Ситникова М.Ю. и др. Эндотелиальная дисфункция у больных с дебютом ишемической болезни сердца в разном возрасте // Кардиология. 2001. № 5. С. 26–29.
- Griendling K.K. et al. Angiotensin II signaling in vascular smooth muscle // New concepts — Hypertension. 1997. Vol. 29. P. 366–373.
- Карпов Ю. А. Ингибиторы ангиотензинпревращающего фермента в моно- и комбинированной терапии артериальной гипертонии // РМЖ. 2009. № 18. С. 1122–1127.
- Taddei S., Virdis A., Chiadoni L., Salvetti A. The role of endothelium in human hypertension // Curr. Opin. Nephrol. Hypertens. 1998. № 7. Р. 20–39.
- Ратманова А. Ингибиторы РААС в нефропротекции. Целесообразна ли комбинация ингибиторов АПФ и БРА? // Med. Review. 2008. № 3 (03). С. 74–80.
- Freedman J.E., Loscalzo J. Nitric oxide and its relationship to thrombotic disorders // J. Thromb. Haemost. 2003. Vol. 1(6). Р. 1183–1188.
- Шишкин А.Н., Лындина М. Л. Эндотелиальная дисфункция и артериальная гипертензия // Артериальная гипертензия. 2008. Т. 14. № 4. С. 315–319.
- Преображенский Д.В., Маревич А.В., Романова Е.И. и др. Микроальбуминурия: диагностическое, клиническое и прогностическое значение (часть вторая) // Российский кардиологический журнал. 2000. № 4. С. 78–85.
- С. А. Бойцов, А. М. Уринский, Р. Л. Кузнецов, Ю. М. Поздняков Структура факторов риска, поражений органов-мишеней и метаболических изменений у больных артериальной гипертензией в различных возрастных группах — Кардиология. — 2009. — № 4. — С. 19–24.
- Белоусов Ю.Б., Леонова М.В., Тарасов А.В. и др. Оценка органопротективных эффектов современных антигипертензивных препаратов // Вестник РГМУ. 2006. № 4 (51). С. 22–27.
- Преображенский Д.В., Савченко М.В., Кектев В.Г., Сидоренко Б. А. Фозиноприл — первый представитель нового поколения ингибиторов ангиотензинпревращающего фермента // Кардиология. 2000. № 5. C. 75–81.
- Краснова Е. А. Фозиноприл в лечении артериальной гипертензии // РМЖ. 2006. № 4.
- Отрохова Е. В. Фозиноприл в лечении и профилактике хронической сердечной недостаточности у больных артериальной гипертензией: проблема оптимального выбора ингибитора ангиотензинпревращающего фермента // Фарматека. 2006. № 20. С. 28–32.
- Агеев Ф.Т., Мареев В. Ю. Моноприл (фозиноприл) в лечении сердечно-сосудистых заболеваний // РМЖ. 2000. Т. 8. С. 11–16.
- Geluk C.A., Asselbergs F.W., Hillege H.L. et at. Impact of statins in microalbuminuric subjects with the metabolic syndrome: a substudy of the PREVEND Intervention Trial // Eur. Heart J. 2005. Vol. 26(13). P. 1314–1320.
- Huang K., Dai G. The effect and mechanism of forsinopril on ventricular hypertrophy of SHR and left ventricular pressure overloading rat // J. Huazriong. Univ. Sci Technolog. Med. Sci. 2002. Vol. 22. P. 17–20.
- Hui K.K., Duchin K.L., Kripalani K. et al. Pharmacokinetics of fosinopril in patients with various degrees of renal function // Clin. Pharmacol. Ther. 1991. Vol. 49. P. 457–467.
- Ford N.F. et al. Single-dose and steady-state pharmacokinetics of fosinopril and fosinoprilat in patients with hepatic impairment // J. Clin. Pharmacol. 1995. Vol.35. P. 145–150.
- Deedwania P. C. Clinical profile of fosinopril, a novel phosphinic acid ACE inhibitor, for the treatment of heart failure // Heart Failure. 1995. Vol. 11. P. 3.
- Levinson B., Graney W.F., DeVault A.R. et al. Age is not reason for dose adjustment for fosinopril in hypertension. [abstract 1029] // Am. J. Hypertens. 1989. Vol. 2 (pt2). 8A.
- Tatti P., Pahor M., Byington R.P. et al. Outcome results of the fosinipril vs amlodipine cardiovascular events randomized trial (FACET) in patients with hypertension and NIDDM // Diabetes Care. 1998. Vol. 21. P. 597–603.
- Стуров Н. В. Место ингибитора АПФ фозиноприла в лечении артериальной гипертонии // Трудный пациент. 2007. № 2.
- Vetter W. Treatment of senile hypertension: the Fosinopril in Old Patients Study (FOPS) // AJH. 1997. Vol. 10. S. 255–261.
- Berdah J., Guest M., Salvador M. Study of the efficacy and safety of fosinopril in general practice in 19,435 hypertensive patients (FLIGHT Study) // Ann. Cardiol. Angiol. 1998. Vol. 47(3). P. 169–175.
- Карпов Ю. А. Фозиноприл при лечении артериальной гипертонии (ФЛАГ): российская программа оценки практической достижимости целевых уровней артериального давления // РМЖ. 2001. Т. 9. № 10. С. 406–410.
- Чазова И. Е. Первые результаты исследования ФАГОТ // Consihum Medicum. 2002. Т. 4. № 11. С. 596–598.
- Tasic I.S., Mijalkovic D., Djordjevic D. et al. Effect of fosinopril on progression of the asymptomatic carotid atherosclerosis and left ventricular hypertrophy in hypertensive patients // Srp. Arh. Celok. Lek. 2006. Vol. 134(3–4). P. 106–113.
- Zanchetti A., Crepaldi G., Bond M.G. et al. Different effects of antihypertensive regimens based on fosinopril or hydrochlorothiazide with or without lipid lowering by pravastatin on progression of asymptomatic carotid atherosclerosis: principal results of PHYLLIS- a randomized double-blind trial // Stroke. 2004. Vol. 35(12). P. 2807–2812.
- Chang N.C., Shih C.M., Bi W.F. et al. Fosinopril improves left ventricular diastolic function in young mildly hypertensive patients without hypertrophy // Cardiovasc. Drugs Ther. 2002. Vol. 16(2). P. 141–147.
- Мухин Н.А., Фомин В.В., Моисеев С.В., Хамхоева М. С. Хроническая сердечная недостаточность и поражение почек: перспективы лечения // Consilium Medicum. 2008. № 09.
- Sica D.A., Cutler R.E., Parmer R.J. et al. Comparison of the steady-state pharmacokinetics of fosinopril, lisinopril and enalapril in patients with chronic hepatic and renal insufficiency // Clin. Pharmacokinet. 1991. Vol. 20. P. 420–427.
- Vetter W. Treatment of senile hypertension. The Fosinopril in Old Patiets Study (FOPS) // Am. J. Hypertens. 1997. Vol. 10. S. 255–261.
- Карпов Ю.А., Мареев В.Ю., Чазова И. Е. Российские программы оценки эффективности лечения фозиноприлом больных с артериальной гипертонией и сердечной недостаточностью. Проект Три Ф (ФЛАГ, ФАСОН, ФАГОТ) // Сердечная недостаточность. 2003. № 4 (5). С. 2–6.
.
Многофункциональные блокаторы рецепторов ангиотензина нового поколения
Duncia JV, Chiu AT, Carini DJ, Gregory GB, Johnson AL, Price WA, Wells GJ, Wong PC, Calabrese JC, Timmermans PB. Открытие сильнодействующих непептидных антагонистов рецепторов ангиотензина II: новый класс сильнодействующих гипотензивных средств. J Med Chem 1990; 33 : 1312–1329.
CAS Статья Google ученый
RAM CV.Блокаторы рецепторов ангиотензина: современное состояние и перспективы на будущее. Am J Med 2008; 121 : 656–663.
CAS Статья Google ученый
McMurray JJ. Ингибиторы АПФ при сердечно-сосудистых заболеваниях — непревзойденные? N Engl J Med 2008; 358 : 1615–1616.
CAS Статья Google ученый
Матчар ДБ, МакКрори, округ Колумбия, Орландо, Лос-Анджелес, Пател М.Р., Пател Ю.Д., Патвардхан МБ, Пауэрс Б., Самса Г.П., Грей Р.Н.Систематический обзор: сравнительная эффективность ингибиторов ангиотензинпревращающего фермента и блокаторов рецепторов ангиотензина II для лечения гипертонической болезни. Ann Intern Med 2008; 148 : 16–29.
Артикул Google ученый
Gavras I, Gavras H. Подвержены ли пациенты, у которых развивается ангионевротический отек с ингибированием АПФ, такая же проблема с блокаторами рецепторов AT1? Arch Intern Med 2003; 163 : 240–241.
Артикул Google ученый
Haymore BR, Yoon J, Mikita CP, Klote MM, DeZee KJ. Риск ангионевротического отека с блокаторами рецепторов ангиотензина у пациентов с предшествующим ангионевротическим отеком, связанным с ингибиторами ангиотензинпревращающего фермента: метаанализ. Ann Allergy Asthma Immunol 2008; 101 : 495–499.
Артикул Google ученый
Юсуф С., Тео К.К., Погу Дж., Дьял Л., Копленд I, Шумахер Х., Дагенаис Дж., Слейт П., Андерсон К.Телмисартан, рамиприл или оба препарата у пациентов с высоким риском сосудистых осложнений. N Engl J Med 2008; 358 : 1547–1559.
CAS Статья Google ученый
Maillard MP, Wurzner G, Nussberger J, Centeno C, Burnier M, Brunner HR. Сравнительная блокада рецепторов ангиотензина II у здоровых добровольцев: важность дозирования. Clin Pharmacol Ther 2002; 71 : 68–76.
CAS Статья Google ученый
Oparil S, Silfani TN, Walker JF.Роль блокаторов рецепторов ангиотензина в качестве монотерапии в достижении целевого артериального давления. Am J Hypertens 2005; 18 (2 часть 1): 287–294.
CAS Статья Google ученый
Калхун Д.А., Джонс Д., Текстор С., Гофф Д.К., Мерфи Т.П., Тото Р.Д., Уайт А, Кушман В.С., Уайт В., Сика Д., Фердинанд К., Джайлз Т.Д., Фолкнер Б., Кэри Р.М. Резистентная гипертензия: диагностика, оценка и лечение. Научное заявление Комитета профессионального образования Американской кардиологической ассоциации Совета по исследованиям высокого кровяного давления. Гипертония 2008; 51 : 1403–1419.
CAS Статья Google ученый
Эллиотт В.Дж., Мейер П.М. Случайный диабет в клинических испытаниях гипотензивных препаратов: сетевой метаанализ. Ланцет 2007; 369 : 201–207.
CAS Статья Google ученый
Gress TW, Nieto FJ, Shahar E, Wofford MR, Brancati FL.Артериальная гипертензия и гипотензивная терапия как факторы риска сахарного диабета 2 типа. Риск атеросклероза в исследовании сообществ. N Engl J Med 2000; 342 : 905–912.
CAS Статья Google ученый
Kjeldsen SE, Naditch-Brule L, Perlini S, Zidek W, Farsang C. Повышенная распространенность метаболического синдрома при неконтролируемой гипертонии в Европе: глобальный профиль кардиометаболического риска у пациентов с гипертонической болезнью. J Hypertens 2008; 26 : 2064–2070.
CAS Статья Google ученый
Редон Дж., Цифкова Р., Лоран С., Нильссон П., Наркевич К., Эрдин С., Мансия Г. Метаболический синдром при гипертонии: утверждение позиции европейского общества гипертонии. J Hypertens 2008; 26 : 1891–1900.
CAS Статья Google ученый
Шаргородский М, Хасс Э, Боаз М, Гавиш Д, Цимлихман Р.Лечение высокими дозами блокатора рецепторов ангиотензина II у пациентов с артериальной гипертензией: дифференциальный эффект защиты тканей от снижения артериального давления. Атеросклероз 2008; 197 : 303–310.
CAS Статья Google ученый
Hollenberg NK, Parving HH, Viberti G, Remuzzi G, Ritter S, Zelenkofske S, Kandra A, Daley WL, Rocha R. Ответ альбуминурии на очень высокие дозы валсартана при сахарном диабете 2 типа. J Hypertens 2007; 25 : 1921–1926.
CAS Статья Google ученый
Каплан Н.М. Комбинированная терапия гипертонии. Nat Rev Cardiol 2009; 6 : 270–271.
CAS Статья Google ученый
Морфи Р., Ранкович З. Сконструированы множественные лиганды. Возникающая парадигма открытия лекарств. J Med Chem 2005; 48 : 6523–6543.
CAS Статья Google ученый
Neutel JM. Назначение паттернов при гипертонии: возрастающая роль комбинаций фиксированных доз для достижения целевых показателей АД у пациентов с гипертонией. Текущие медицинские исследования и заключения 2008; 24 : 2389–2401.
CAS Статья Google ученый
Benson SC, Pershadsingh HA, Ho CI, Chittiboyina A, Desai P, Pravenec M, Qi N, Wang J, Avery MA, Kurtz TW.Идентификация телмисартана как уникального антагониста рецепторов ангиотензина II с селективной активностью, регулирующей PPAR {гамма}. Гипертония 2004; 43 : 993–1002.
CAS Статья Google ученый
Schupp M, Janke J, Clasen R, Unger T, Kintscher U. Блокаторы рецепторов ангиотензина 1 типа индуцируют гамма-активность рецепторов, активируемых пролифератором пероксисом. Тираж 2004 г .; 109 : 2054–2057.
CAS Статья Google ученый
Schupp M, Clemenz M, Gineste R, Witt H, Janke J, Helleboid S, Hennuyer N, Ruiz P, Unger T., Staels B, Kintscher U. Молекулярная характеристика новых селективных модуляторов рецепторов, активируемых пролифератором пероксисом, {гамма} с активностью блокирования рецепторов ангиотензина. Диабет 2005; 54 : 3442–3452.
CAS Статья Google ученый
Юсуф С., Тео К., Андерсон С., Погу Дж., Дьял Л., Копленд I, Шумахер Х., Дагенаис Г., Слейт П.Эффекты блокатора рецепторов ангиотензина телмисартана на сердечно-сосудистые события у пациентов с высоким риском непереносимости ингибиторов ангиотензинпревращающего фермента: рандомизированное контролируемое исследование. Ланцет 2008; 372 : 1174–1183.
CAS Статья Google ученый
Yusuf S, Diener HC, Sacco RL, Cotton D, Ounpuu S, Lawton WA, Palesch Y, Martin RH, Albers GW, Bath P, Bornstein N, Chan BP, Chen ST, Cunha L, Dahlof B, Де Кейзер Дж., Доннан Г.А., Эстол К., Горелик П., Гу В., Херманссон К., Хильбрих Л., Касте М., Лу К., Махниг Т., Пайс П., Робертс Р., Скворцова В., Тил П., Тони Д., Вандермэлен К., Фойгт Т, Вебер М., Юн Б.В.Телмисартан для предотвращения повторного инсульта и сердечно-сосудистых событий. N Engl J Med 2008; 359 : 1225–1237.
CAS Статья Google ученый
Bosch J, Yusuf S, Gerstein HC, Pogue J, Sheridan P, Dagenais G, Diaz R, Avezum A, Lanas F, Probstfield J, Fodor G, Holman RR. Влияние рамиприла на частоту диабета. N Engl J Med 2006; 355 : 1551–1562.
Артикул Google ученый
Dagenais GR, Pogue J, Fox K, Simoons ML, Yusuf S.Ингибиторы ангиотензин-превращающего фермента при стабильном сосудистом заболевании без систолической дисфункции левого желудочка или сердечной недостаточности: комбинированный анализ трех исследований. Ланцет 2006; 368 : 581–588.
CAS Статья Google ученый
Lithell H, Hansson L, Skoog I, Elmfeldt D, Hofman A, Olofsson B, Trenkwalder P, Zanchetti A. Исследование познания и прогноза у пожилых людей (SCOPE): основные результаты рандомизированного двойного слепого исследования. J Hypertens 2003; 21 : 875–886.
CAS Статья Google ученый
Томияма Х, Кусиро Т., Абета Х, Исии Т., Такахаши А., Фурукава Л., Асагами Т., Хино Т., Сайто Ф, Оцука Ю. Кинины способствуют повышению чувствительности к инсулину во время лечения ингибитором ангиотензинпревращающего фермента. Гипертония 1994; 23 : 450–455.
CAS Статья Google ученый
Сиучи Т., Цуй Техас, Ву Л., Накагами Х., Такеда-Мацубара Й, Иваи М., Хориучи М.Ингибитор АПФ улучшает инсулинорезистентность у мышей с диабетом через брадикинин и NO. Гипертония 2002; 40 : 329–334.
CAS Статья Google ученый
Бернобич Э, де Анжелис Л, Лерин С, Беллини Дж. Роль ангиотензиновой системы в гомеостазе сердечной глюкозы: терапевтическое значение. Наркотики 2002; 62 : 1295–1314.
CAS Статья Google ученый
Scheen AJ.Ингибирование ренин-ангиотензиновой системы предотвращает сахарный диабет 2 типа. Часть 2. Обзор физиологических и биохимических механизмов. Diabetes Metab 2004; 30 : 498–505.
CAS Статья Google ученый
Goebel M, Clemenz M, Staels B, Unger T, Kintscher U, Gust R. Характеристика новых агонистов PPARgamma: анализ структурных компонентов телмисартана. ChemMedChem 2009; 4 : 445–456.
CAS Статья Google ученый
Джамерсон К.А., Несбитт С.Д., Амерена СП, Грант Э., Юлиус С. Ангиотензин опосредует захват глюкозы предплечьями скорее за счет гемодинамики, чем за прямое воздействие. Гипертония 1996; 27 : 854–858.
CAS Статья Google ученый
Юсуф С., Остергрен Дж. Б., Герштейн ХК, Пфеффер М.А., Сведберг К., Грейнджер С.Б., Олофссон Б., Пробстфилд Дж., МакМюррей СП.Влияние кандесартана на разработку нового диагноза сахарного диабета у пациентов с сердечной недостаточностью. Тираж 2005 г .; 112 : 48–53.
CAS Статья Google ученый
Глобальный центр исследований и разработок Такеда. Эффективность и безопасность TAK-536 у пациентов с гипертонической болезнью. Идентификатор ClinicalTrials.gov: NCT00759551. Доступно по адресу: http://clinicaltrials.gov/ct2/show/NCT00759551?term=tak-536&rank=1.По состоянию на 22 июня 2009 г.
Глобальный центр исследований и разработок Такеда. Исследование эффективности и безопасности TAK-491 по сравнению с валсартаном и олмесартаном у пациентов с эссенциальной гипертензией. Идентификатор ClinicalTrials.gov: NCT00696436. Доступно по адресу: http://clinicaltrials.gov/ct2/show/NCT00696436?term=azilsartan&rank=8. По состоянию на 22 июня 2009 г.
Пресс-релиз компании Takeda Pharmaceuticals. Исследовательский состав Takeda TAK-536 для лечения гипертонии входит в фазу 3 клинических испытаний в Японии.Доступно на: http://www.takeda.com/press/article_34500.html. По состоянию на 24 июня 2009 г.
Kohara Y, Kubo K, Imamiya E, Wada T, Inada Y, Naka T. Синтез и антагонистическая активность рецепторов ангиотензина II производных бензимидазола, несущих кислые гетероциклы как новых биоизостеров тетразола. J Med Chem 1996; 39 : 5228–5235.
CAS Статья Google ученый
Иваи М., Чен Р., Имура Й, Хориучи М.TAK-536, новый блокатор рецепторов AT1, улучшает непереносимость глюкозы и дифференцировку адипоцитов. Am J Hypertens 2007; 20 : 579–586.
CAS Статья Google ученый
Глобальный центр исследований и разработок Такеда. Эффективность и безопасность TAK-491 в сочетании с хлорталидоном у пациентов с умеренной и тяжелой артериальной гипертензией. Идентификатор ClinicalTrials.gov: NCT00847626. Доступно по адресу: http: // Clinicaltrials.gov / ct2 / show / NCT00847626? term = tak-536 & rank = 4. По состоянию на 22 июня 2009 г.
Сотрудники и координаторы ALLHAT для совместной исследовательской группы ALLHAT. Антигипертензивное и гиполипидемическое лечение для предотвращения сердечного приступа. Основные исходы у пациентов с гипертонической болезнью высокого риска, рандомизированных по группе ингибитора ангиотензинпревращающего фермента или блокатора кальциевых каналов по сравнению с диуретиком: исследование гипотензивного и липидоснижающего лечения для предотвращения сердечного приступа (ALLHAT). Jama 2002; 288 : 2981–2997.
Артикул Google ученый
Блэк Х.Р., Дэвис Б., Барзилай Дж., Нвачуку К., Бэймбридж С., Марджинян Х., Райт-младший Дж. Т., Бэзил Дж., Вонг Н. Д., Велтон П., Дарт Р. А., Тадани У. Метаболические и клинические исходы у лиц, не страдающих диабетом, с метаболическим синдромом, назначенным хлорталидоном, амлодипином или лизиноприлом в качестве начального лечения артериальной гипертензии: отчет исследования «Антигипертензивное и липидоснижающее лечение для предотвращения сердечного приступа» (ALLHAT). Уход за диабетом 2008; 31 : 353–360.
CAS Статья Google ученый
Хамагучи Ю., Учии М., Мацубара М., Янагисава А., Хенми К., Уэно К., Кусака Х., Яо К. Новый БРА с инсулино-сенсибилизирующей активностью, К-868, предотвращает диабетическую нефропатию у крыс. Диабет 2009; 58 (Дополнение 1): A208 – A209.
Google ученый
Pfizer Inc.. PF-03838135 неконфиденциальное резюме. 2008.
Тернер А.Дж. Неприлысин. В: Barrett AJ, Rawlings D, Woessner JF (ред.). Справочник по протеолитическим ферментам . Эльзевир: Лондон, 2004, 419–426.
Google ученый
Weber MA. Ингибиторы вазопептидазы. Ланцет 2001; 358 : 1525–1532.
CAS Статья Google ученый
Костис Дж. Б., Пакер М, Блэк Х. Р., Шмидер Р., Генри Д., Леви Э.Омапатрилат и эналаприл у пациентов с артериальной гипертензией: исследование сердечно-сосудистого лечения омапатрилатом и эналаприлом (OCTAVE). Am J Hypertens 2004; 17 : 103–111.
CAS Статья Google ученый
Packer M, Califf RM, Konstam MA, Krum H, McMurray JJ, Rouleau JL, Swedberg K. Сравнение омапатрилата и эналаприла у пациентов с хронической сердечной недостаточностью: рандомизированное испытание эффективности омапатрилата и эналаприла в снижении частоты событий (OVERTURE). Тираж 2002; 106 : 920–926.
CAS Статья Google ученый
Rouleau JL, Pfeffer MA, Stewart DJ, Isaac D, Sestier F, Kerut EK, Porter CB, Proulx G, Qian C, Block AJ. Сравнение ингибитора вазопептидазы, омапатрилата и лизиноприла по толерантности к физической нагрузке и заболеваемости у пациентов с сердечной недостаточностью: рандомизированное исследование IMPRESS. Ланцет 2000; 356 : 615–620.
CAS Статья Google ученый
Zanchi A, Maillard M, Burnier M.Недавние клинические испытания омапатрилата: новые разработки. Curr Hypertens Rep 2003; 5 : 346–352.
Артикул Google ученый
Фрайер Р.М., Сегрети Дж., Банфор PN, Видомски Д.Л., Бэкес Б.Дж., Лин К.В., Балларон С.Дж., Кокс Б.Ф., Тревиллиан Дж.М., Рейнхарт Г.А., фон Гельдерн Т.В. Влияние ингибиторов метаболизма брадикинина на вызванную гипотензию у крыс: оценка эффективности ферментов, связанных с опосредованным брадикинином ангионевротическим отеком. Br J Pharmacol 2008; 153 : 947–955.
CAS Статья Google ученый
Pu Q, Брассард П., Джавешгани Д.М., Игларц М., Уэбб Р.Л., Амири Ф., Шиффрин Э.Л. Эффекты комбинированного антагониста рецептора AT1 / ингибитора NEP на ремоделирование сосудов и сердечный фиброз у SHRSP. J Hypertens 2008; 26 : 322–333.
CAS Статья Google ученый
Gardiner SM, March JE, Kemp PA, Ballard SA, Bennett T.Региональные гемодинамические эффекты ингибирования нейтральной эндопептидазы и антагонизма рецептора ангиотензина (AT (1)) отдельно или в комбинации у сознательных спонтанно гипертензивных крыс. J Pharmacol Exp Ther 2006; 319 : 340–348.
CAS Статья Google ученый
Hegde LG, Thibodeaux H, Yu C, Cheruvu M, Olsufka R, Renner T, Richardson C, Villarreal J, Armstrong SR, Hegde SS. Сравнительная доклиническая оценка риска ангионевротического отека ингибиторов ренин-ангиотензиновой системы и неприлизина в анализе экстравазации плазмы трахеи под наркозом крыс. FASEB J 2009; 23 (Тезисы): LB379.
Google ученый
Choi SK, Fatheree PR, Hedge S, Hudson R, Jendza K, Marquess D, McKinnell RM, Sasikumar V, Choi SK, Fatheree PR, Hedge S, Hudson R, Jendza K, Marquess D, McKinnell RM, Sasikumar V. Гипотензивные средства двойного действия. Публикация заявки на патент США , US 2008/0188533.
Аллегретти П., Чой С.К., Гендрон Р., Фатери П.Р., Джендза К., Маккиннелл Р.М., МакМуртри С., Олсон Б.Имидазольные антигипертензивные средства двойного действия. Публикация заявки на патент США , US 2009/00232282009.
Аллегретти П., Чой К.С., Фатери П.Р., Гендрон Р., Хадсон Р., Джендза К., Маккиннелл Р.М., МакМуртри К., Олсон Б. Бензоимидазольные антигипертензивные средства двойного действия. Публикация заявки на патент США , US 2008/03189512008.
Allegretti PC, Gendron R, Fatheree PR, Jendza K, McKinnell RM, McMurtrie C, Olson B. Гипотензивные средства двойного действия. Публикация заявки на патент США , US 2008/026
Ксандер Г.М., Уэбб Р.Л. Способы лечения и фармацевтический состав. Патент США 7,468,390.
Аль-Файюми С., Ху Дж., Кумараперумал Н., Ройс А.Э., Рюггер С., Занноу Е.А. Фармацевтические композиции двойного действия на основе супраструктур антагониста / блокатора рецепторов ангиотензина (ARB) и ингибитора нейтральной эндопептидазы (NEP). Публикация международной заявки РСТ 2009, WO 2009/0061713 A1.
Фен Л., Годтфредсен С.Е., Карпински П., Саттон П.А., Прашад М., Гиргис М.Дж., Ху Б., Лю Ю. Фармацевтические комбинации антагониста рецептора ангиотензина и ингибитора NEP. Публикация международной заявки РСТ 2007, WO 2007/056546 A1.
Аноним. Novartis подчеркивает новаторский подход к открытию лекарств с динамичным продвижением исследовательских разработок. Фармацевтические новости и статьи http://www.drugs.com/news/novartis-highlights-innovative-approach-discovery-dynamic-advance-exploratory-pipeline-14763.html. По состоянию на 23 июня 2009 г.
Dhaun N, Goddard J, Kohan DE, Pollock DM, Schiffrin EL, Webb DJ. Роль эндотелина-1 в клинической гипертензии: 20 лет спустя. Гипертония 2008; 52 : 452–459.
CAS Статья Google ученый
Mucke HA. Легочная артериальная гипертензия: на пути к излечимому заболеванию. Curr Opin Investigations Drugs 2008; 9 : 957–962.
CAS PubMed Google ученый
Блэк Х.Р., Бакрис Г.Л., Вебер М.А., Вайс Р., Шахоуи М.Э., Марпл Р., Таннури Дж., Линас С., Винс Б.Л., Линсеман СП, Роден Р., Гербер М.Дж. Эффективность и безопасность дарузентана у пациентов с резистентной артериальной гипертензией: результаты рандомизированного двойного слепого плацебо-контролируемого исследования с диапазоном доз. J Clin Hypertens (Гринвич) 2007; 9 : 760–769.
CAS Статья Google ученый
Massart PE, Hodeige DG, Van Mechelen H, Charlier AA, Ketelslegers JM, Heyndrickx GR, Donckier JE.Антагонисты рецепторов ангиотензина II и эндотелина-1 обладают кумулятивным гипотензивным действием при гипертензии у собак. J Hypertens 1998; 16 : 835–841.
CAS Статья Google ученый
Болендер Дж., Гербаулет С., Крамер Дж., Гросс М, Кирхенгаст М, Дитц Р. Синергетические эффекты блокады рецепторов AT (1) и ET (A) на трансгенной ангиотензин-зависимой модели крыс. Гипертония 2000; 35 : 992–997.
CAS Статья Google ученый
Gardiner SM, March JE, Kemp PA, Mullins JJ, Bennett T. Гемодинамические эффекты лозартана и антагониста эндотелина SB 209670 у находящихся в сознании трансгенных ((mRen-2) 27) крыс с гипертонией. Br J Pharmacol 1995; 116 : 2237–2244.
CAS Статья Google ученый
Икеда Т., Охта Х, Окада М, Кавай Н, Накао Р., Сигл П.К., Кобаяси Т., Мияучи Т., Нишикибе М.Антигипертензивные эффекты смешанного антагониста рецепторов эндотелина A и B, J-104132, усиливались в присутствии антагониста рецептора AT1, MK-954. J Cardiovasc Pharmacol 2000; 36 (5 Приложение 1): S337 – S341.
CAS Статья Google ученый
Уолш Т.Ф., Фитч К.Дж., Уильямс-младший Д.Л., Мерфи К.Л., Нолан Н.А., Петтибон Д.Д., Чанг Р.С.Л., О’Мэлли С.С., Клинешмидт Б.В., Вебер Д.Ф., Гринли В.Дж. Сильные двойные антагонисты рецепторов эндотелина и ангиотензина II, полученные из альфа-феноксифенилуксусных кислот (часть III). Письма по биоорганической медицинской химии 1995; 5 : 1155–1158.
CAS Статья Google ученый
Ковала М.С., Муругесан Н., Теллью Дж., Карлсон К., Моншизадеган Х., Райан С., Гу З., Кейн Б., Фаднис Л., Башка Р.А., Бейер С., Артур С., Дикинсон К., Чжан Д., Перрон М., Феррер П., Джанкарли М., Бауманн Дж., Бёрд Э., Панчал Б., Ян Й., Трипподо Н., Барриш Дж., Макор Дж. Э. Новые антагонисты рецепторов AT1 и ETA двойного действия снижают артериальное давление при экспериментальной гипертензии. J Pharmacol Exp Ther 2004; 309 : 275–284.
CAS Статья Google ученый
Murugesan N, Tellew JE, Gu Z, Kunst BL, Fadnis L, Cornelius LA, Baska RA, Yang Y, Beyer SM, Monshizadegan H, Dickinson KE, Panchal B, Valentine MT, Chong S, Morrison RA, Карлсон К. Э., Пауэлл-младший, Морленд С., Барриш Дж. К., Ковала М.С., Макор Дж. Э. Открытие N-изоксазолилбифенилсульфонамидов как мощных двойных антагонистов рецепторов ангиотензина II и эндотелина А. J Med Chem 2002; 45 : 3829–3835.
CAS Статья Google ученый
Murugesan N, Gu Z, Fadnis L, Tellew JE, Baska RA, Yang Y, Beyer SM, Monshizadegan H, Dickinson KE, Valentine MT, Humphreys WG, Lan SJ, Ewing WR, Carlson KE, Kowala MC, Zahler R, Macor JE. Двойные антагонисты рецепторов ангиотензина II и эндотелина А: синтез 2′-замещенных N-3-изоксазолилбифенилсульфонамидов с улучшенной эффективностью и фармакокинетикой. J Med Chem 2005; 48 : 171–179.
CAS Статья Google ученый
Floyd DM, Sills MA. Доклиническая разработка PS433540, антагониста рецепторов двойного действия (DARA) рецепторов ангиотензина и эндотелина. J Clin Hypertens 2007; 9 (5, Приложение A): A158.
Google ученый
Pollock DM, Derebail VK, Yamamoto T, Pollock JS.Комбинированные эффекты антагонистов рецепторов AT (1) и ET (A), кандесартана и A-127722 у крыс с гипертонической болезнью DOCA-соли. Gen Pharmacol 2000; 34 : 337–342.
CAS Статья Google ученый
Neutel JM, Graff A, Samson MB, Belder R, Zhang J, Kapil RP. PS433540, антагонист рецепторов двойного ангиотензина (AT1) и эндотелина (ETA) (DARA), демонстрирует дозозависимые эффекты снижения артериального давления лучше, чем ирбесартан, в исследовании диапазона доз фазы IIb у пациентов с гипертонией 1 и 2 стадии.Представлено на 24-м ежегодном собрании Американского общества гипертонии в 2009 г .; http://investors.ligand.com/releasedetail.cfm?ReleaseID=362687. По состоянию на 22 июня 2009 г.
Stuart-Smith K. Демистифицировано. Оксид азота. Мол Патол 2002; 55 : 360–366.
CAS Статья Google ученый
Палмер Р.М., Ферридж АГ, Монкада С. Высвобождение оксида азота составляет биологическую активность релаксирующего фактора эндотелия. Nature 1987; 327 : 524–526.
CAS Статья Google ученый
Игнарро Л.Дж., Буга Г.М., Вуд К.С., Бирнс Р.Э., Чаудхури Г. Расслабляющий фактор эндотелия, продуцируемый и высвобождаемый из артерии и вены, представляет собой оксид азота. Proc Natl Acad Sci USA 1987; 84 : 9265–9269.
CAS Статья Google ученый
Лоскальцо Дж., Велч Дж.Оксид азота и его роль в сердечно-сосудистой системе. Prog Cardiovasc Dis 1995; 38 : 87–104.
CAS Статья Google ученый
Джайлз ТД. Аспекты оксида азота в здоровье и болезнях: акцент на гипертонию и сердечно-сосудистые заболевания. J Clin Hypertens (Гринвич) 2006; 8 (12 приложение 4): 2–16.
CAS Google ученый
Martelli A, Breschi MC, Calderone V.Сочетание фармакодинамических гибридов установило сердечно-сосудистые механизмы действия с дополнительными свойствами высвобождения оксида азота. Curr Pharm Des 2009; 15 : 614–636.
CAS Статья Google ученый
Karlsson J, Pivodic A, Aguirre D, Schnitzer TJ. Эффективность, безопасность и переносимость ингибирующего циклооксигеназу донатора оксида азота напроксинода при лечении остеоартрита бедра или колена. J Rheumatol 2009; 36 : 1290–1297.
CAS Статья Google ученый
Breschi MC, Calderone V, Digiacomo M, Macchia M, Martelli A, Martinotti E, Minutolo F, Rapposelli S, Rossello A, Testai L, Balsamo A. Новые NO-высвобождающие фармакодинамические гибриды лозартана и его активного метаболита: дизайн, синтез и биофармакологические свойства. J Med Chem 2006; 49 : 2628–2639.
CAS Статья Google ученый
Breschi MC, Calderone V, Digiacomo M, Martelli A, Martinotti E, Minutolo F, Rapposelli S, Balsamo A. NO-сартаны: новый класс фармакодинамических гибридов в качестве сердечно-сосудистых препаратов. J Med Chem 2004; 47 : 5597–5600.
CAS Статья Google ученый
Ли YQ, Ji H, Zhang YH, Shi WB, Meng ZK, Chen XY, Du GT, Tian J.WB1106, новое производное телмисартана, высвобождающее оксид азота, подавляет гипертензию и улучшает метаболизм глюкозы у крыс. евро J Pharmacol 2007; 577 : 100–108.
CAS Статья Google ученый
Али А, Ло ММ-С, Франклин С., Альмиранте Н., Стефанини С., Сторони Л., Бионди С., Онджини Э. Бис (нитроокси) производные. как антагонисты рецептора ангиотензина II, полезные при лечении гипертензии, и их получение. Публикация международной заявки РСТ 2009, WO 2009/070241 A2.
Себхат И.К., Ло ММ-С, Наругунд Р.П., Али А., Франклин С., Альмиранте Н., Сторони Л., Стефанини С. Получение бифенильных соединений, содержащих тетразольную группу, в качестве антагонистов рецепторов ангиотензина II. Публикация международной заявки РСТ 2008, WO 2008/076246 A2.
Себхат И.К., Ло ММ-С, Наругунд Р.П., Али А., Франклин С., Альмиранте Н., Сторони Л., Стефанини С.Получение производных динитрата лозартана и родственных соединений в качестве антагонистов рецепторов ангиотензина II. Публикация международной заявки РСТ WO 2008/076247 A2.
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
лекарств от артериального давления указывают путь к возможному лечению COVID-19
В течение последних нескольких недель исследовательские журналы публиковали отчеты о связи между лекарствами, снижающими высокое кровяное давление, и COVID-19.Беспокойство вызывает то, что лекарства могут увеличить количество рецепторов, которые SARS-CoV-2 — вирус, вызывающий COVID-19, — использует для проникновения в клетки. Повышение уровней этих рецепторов ACE2 в клетках легких и сердца может дать вирусу больше клеточных точек входа для нацеливания и потенциально усугубить симптомы заболевания.
Это гипотеза, которую важно проверить, — отмечает Карлос Феррарио, профессор общей хирургии Медицинской школы Уэйк Форест, специализирующийся на исследованиях гипотензивных препаратов.
До сих пор данных, подтверждающих связь между лекарствами от кровяного давления, в частности, ингибиторами ангиотензинпревращающего фермента (АПФ) и блокаторами рецепторов ангиотензина (БРА), и COVID-19 немного. Тем не менее, освещение этой связи в СМИ привело к тому, что пациенты, выписавшие лекарства, позвонили своим врачам и спросили, следует ли им прекратить их прием. В ответ несколько медицинских ассоциаций, включая Американский колледж кардиологов, Американскую кардиологическую ассоциацию, Американское общество сердечной недостаточности и Европейское общество кардиологов, выпустили инструкции, в которых говорится, что пациенты не должны прекращать прием гипотензивных препаратов, поскольку нет никаких доказательств того, что поддерживают утверждение, что они вызывают более серьезные инфекции SARS-CoV-2.
В поддержку этой рекомендации Анкит Патель, клинический и исследовательский сотрудник, специализирующийся на почках в Бригаме и женской больнице в Бостоне, и его коллега из Бригама Ашиш Верма покопались в литературе, чтобы устранить путаницу, и сообщили 24 марта в JAMA . , что нет окончательных доказательств того, что ингибиторы АПФ и БРА увеличивают тяжесть COVID-19. Другая группа врачей, написавшая в выпуске от 30 марта New England Journal of Medicine , пришла к такому же выводу.
Вместо того, чтобы усугублять симптомы COVID-19, некоторые антигипертензивные препараты могут фактически уменьшить тяжесть инфекций и, следовательно, могут использоваться для лечения болезни, говорят обе группы врачей. Более пристальный взгляд на механизмы, лежащие в основе лекарств, также поддержал другую идею о том, как лечить COVID-19 — дать пациентам фермент ACE2 в качестве приманки, чтобы направить SARS-CoV-2 от их клеток. Сегодня (2 апреля) биотехнологическая компания, разрабатывающая такой подход с использованием рекомбинантного ACE2, получила одобрение регулирующих органов для начала клинических испытаний на пациентах с COVID-19.
«Это очень интересная идея», — говорит Дэвид Касс, кардиолог из Медицинской школы Джонса Хопкинса, The Scientist . «Очевидно, что если вирус связывается с этой формой ACE2, которая плавает в кровотоке и не прикрепляется к клетке, он не сможет размножаться и повредить клетки».
Как ACE2 действует в организмеИдея приманки ACE2 восходит к ранним исследованиям рецептора Джозефом Пеннингером, молекулярным иммунологом из Университета Британской Колумбии.Примерно 20 лет назад он работал исследователем в Институте рака Онтарио, когда клонировал ACE2 и начал исследовать, что он делает.
Старший научный сотрудник лаборатории подумал, что эта работа была пустой тратой времени, вспоминает Пеннингер, говоря ему, что ученые уже знают все, что им нужно знать о системе ренин-ангиотензин, которая регулирует кровяное давление и баланс жидкости и электролитов. Старший научный сотрудник добавил, что ACE2, связанный с системой, был настолько утомительным, что Пеннинджер должен прекратить работать над ним, прежде чем он разрушит свою карьеру.В то время это было болезненно слышать, но Пеннингер еще больше решил понять биологическую функцию ACE2. «Сейчас это забавно, — говорит он.
Антигипертензивные препараты, называемые БРА, нарушают путь, ведущий к сужению кровеносных сосудов, предотвращая связывание ангиотензина II с рецептором AT1. Этот теперь доступный ангиотензин затем перерабатывается ACE2 (не показан) в форму, которая приводит к расширению кровеносных сосудов. Ингибиторы АПФ блокируют выработку ангиотензина II.
Со временем он и другие начали выяснять, как ACE2 действует в ренин-ангиотензиновой системе. Система начинается с гормона, секретируемого почками, называемого ренином, который расщепляет пептидный гормон ангиотензиноген до ангиотензина I. Этот продукт расщепления затем превращается в версию ангиотензина II под действием АПФ, ангиотензин-превращающего фермента. Эта версия связывается с рецептором ангиотензина II типа 1 (AT1) на поверхности кровеносных сосудов, клеток легких и сердца среди других клеток организма.Там, где эти молекулы встречаются, кровеносные сосуды сужаются и повышается кровяное давление, что может способствовать развитию острого респираторного дистресс-синдрома.
Вот где вступает в действие ACE2. Фермент отщепляет аминокислоту от ангиотензина II с образованием ангиотензина 1-7, который расширяет кровеносные сосуды, уменьшает воспаление и инактивирует ангиотензин II до того, как он попадет к рецептору AT1 клетки.
«Когда есть гормон, который взаимодействует с организмом определенным образом, часто есть другой гормон, который ему противодействует», — говорит Патель.ACE2 уравновешивает ACE, и «тело пытается поддерживать баланс между этими двумя факторами, чтобы держать ситуацию под контролем».
Врачи прописывают ингибиторы АПФ людям с высоким кровяным давлением и другими проблемами с сердцем, чтобы предотвратить преобразование АПФ ангиотензина I в форму ангиотензина II, которая сужает кровеносные сосуды, что приводит к снижению кровяного давления. БРА предотвращают связывание ангиотензина II с рецепторами AT1, поэтому ACE2 метаболизирует его, что также снижает артериальное давление.
«Мы действительно много знаем об ACE2 и его биологии», — говорит Пеннингер.«Мы должны следить за данными».
Повышение уровня ACE2 может отвлечь коронавирусПеннингер опубликовал свою работу по биологии ACE2 в 2002 году, незадолго до вспышки атипичной пневмонии в 2003 году. После того, как вирус заразил людей и начал распространяться, команда из Бостона опубликовала первые подсказки. о том, как SARS-CoV нацеливается на ACE2, чтобы проникнуть в клетки человека. В то время предлагались и другие рецепторы в качестве точек входа, но упоминание об ACE2 привлекло внимание Пеннингера.
Он начал исследование на мышах и в 2005 году опубликовал первые убедительные доказательства того, что SARS-CoV использует ACE2 для заражения клеток своего хозяина.В том же исследовании Пеннингер и его коллеги показали, что вирус снижает количество ACE2, что приводит к повышению уровня ангиотензина II, что, в свою очередь, вызывает острую легочную недостаточность. По его словам, работа показала, что сделало SARS-CoV таким смертоносным.
Основываясь на данных, команда Пеннингера утверждала, что введение рекомбинантного белка ACE2 может обманом заставить вирус связываться с ним, а не с настоящими рецепторами ACE2. Это могло бы затем защитить эндогенные рецепторы и позволить им продолжать функционировать, уравновешивая АПФ, и, в идеале, защитить легкие и сердце от повреждения во время вирусной инфекции.
Пеннингер работает над разработкой терапии рекомбинантным белком ACE2 в течение 15 лет. Он впервые испытал его на мышах после того, как они вдохнули кислоту; обработка ACE2 предотвращала развитие острого повреждения легких у животных. Другие исследования показали, что рекомбинантные белки можно использовать для лечения сердечной недостаточности, и в конечном итоге исследование привело к клиническим испытаниям для проверки безопасности ACE2 для людей.
На данный момент ранние клинические испытания препарата показали, что он не имеет каких-либо вредных побочных эффектов у здоровых людей или пациентов с легочной недостаточностью.(Пеннингер не участвовал в проведении клинических испытаний).
Следующий шаг — проверить, может ли рекомбинантный фермент вмешаться в инфекцию SARS-CoV-2. В исследовании, опубликованном сегодня в Cell , группа Пеннингера показывает, что препарат может снизить вирусную нагрузку SARS-CoV-2 в экспериментальных моделях в 1000-5000 раз. Сегодня Apeiron Biologics, биотехнологическая компания, основанная Пеннингером в 2005 году, также получила разрешение регулирующих органов на начало клинических испытаний препарата на пациентах с тяжелыми симптомами COVID-19, что, по его словам, может произойти уже в конце следующей недели. .
Наращивание АПФ с использованием БРАРанняя работа Пеннингера по SARS-CoV является частью того, что вызвало у врачей дискуссию о безопасности ингибиторов АПФ и БРА, которые регулируют уровни ангиотензина II напрямую или через его клеточный рецептор. Еще одно исследование, связанное с гипотензивными препаратами, привлекшее внимание врачей, было проведено Ferrario более десяти лет назад. Введение крысам ингибиторов АПФ или БРА привело к увеличению активности ACE2 в сердцах животных, именно там, где ученые и врачи не хотели бы, чтобы нацелено большее количество рецепторов ACE2 для SARS-CoV-2.По крайней мере, так можно подумать.
Но предварительная работа Пеннингера от 2005 года предполагает, что повышение уровня АПФ2 с помощью гипотензивных препаратов может лечить симптомы инфекции SARS-CoV-2, причем БРА более перспективны, чем ингибиторы АПФ.
Ингибиторы АПФ снижают уровень ангиотензина II, и когда они это делают, остается меньше субстрата для метаболизма АПФ, что может оставить фермент бездействующим и, следовательно, уязвимым для атаки SARS-CoV-2. Это часть аргумента, который выдвигали некоторые исследователи о том, что ингибиторы АПФ способствуют заражению COVID-19.Однако, по словам Пеннингера, данных, свидетельствующих о том, что это происходит, нет. Тем не менее, утверждает он, то, как ингибиторы АПФ действуют в организме, высвобождая АПФ2 в клетках для вирусного воздействия, исключает их использование в качестве потенциальных методов лечения COVID-19.
К сожалению для страны, у нас будет много случаев COVID-19. Группы сейчас пытаются начать эти эпидемиологические исследования, чтобы мы могли получить ответы.
—Дэвид Касс, Медицинская школа Джонса Хопкинса
Использование БРА для борьбы с вирусом является более многообещающим подходом.Как показала команда Пеннингера, SARS-CoV снижает содержание ACE2, вызывая гипертонию и легочную недостаточность у мышей. Если БРА повышают экспрессию ACE2, это может противодействовать эффектам инфекции. По словам Дэвида Гурвица, генетика с фармакологическим образованием из Тель-Авивского университета, на данный момент эта гипотеза является предварительной. Он описал идею, которая кажется парадоксальной, 4 марта в обзорной статье, опубликованной в журнале Drug Development Research . Основное различие между ингибиторами АПФ и БРА заключается в том, что первые просто высвобождают существующие рецепторы ACE2, в то время как последние приводят к увеличению количества рецепторов, позволяя преобразовать большее количество ангиотензина II в ангиотензин 1-7.Это расширит кровеносные сосуды и уменьшит воспаление, противодействуя любому гипертоническому состоянию, вызванному вирусной инфекцией.
В ходе клинического анализа, призванного гарантировать, что БРА не причиняют вреда пациентам с COVID-19, китайские исследователи опубликовали предварительные данные по medRxiv , подтверждающие эту гипотезу. В ходе исследования команда отслеживала состояние здоровья 511 пациентов, принимавших лекарства от сердечных заболеваний, которые затем заразились SARS-CoV-2. Пациенты принимали ингибиторы АПФ, БРА или другие препараты, снижавшие их артериальное давление.Результаты показали, что пациенты старше 65 лет, принимающие БРА, имели более низкий риск развития тяжелого повреждения легких, чем пациенты того же возраста, не принимавшие лекарства, но не было достаточно данных для проведения аналогичного анализа для ингибиторов АПФ. Работа показывает, что для БРА опасности нет, и могут быть преимущества, но, как всегда, необходимы дополнительные данные, говорит Касс.
Один из способов собрать эти данные в более крупном масштабе, объясняет Гурвиц, — это проанализировать медицинские записи многих других пациентов с COVID-19, чтобы узнать, принимали ли они БРА до заражения SARS-CoV-2, а затем сравнить тяжесть инфекции у этих пациентов и насколько хорошо они выздоровели с симптомами пациентов с COVID-19, которые не принимали лекарства.
Гурвиц также рекомендует исследователям сравнить процент людей, хронически принимающих различные гипотензивные препараты, в общей популяции с процентом их среди госпитализированных по поводу COVID-19. Он отмечает, что эти типы анализов также можно проводить со многими другими одобренными препаратами, а не только с БРА.
Врачи Университетской клиники Цюриха уже начали регистрацию пациентов для проведения такого рода анализов медицинской информатики, а врачи и исследователи из Медицинской школы Джонса Хопкинса и других школ общественного здравоохранения в США обсуждали возможность начала этих исследований. .
«К сожалению для страны, у нас будет много случаев COVID-19», — говорит Касс. «Группы сейчас пытаются начать эти эпидемиологические исследования, чтобы мы могли получить ответы».
Современные методы лечения гипертонии: проверенные и новые препараты | Европейский журнал сердца
Абстрактные
Лечение эссенциальной гипертензии в основном основано на назначении четырех основных классов гипотензивных препаратов, то есть блокаторов ренин-ангиотензиновой системы, блокаторов кальциевых каналов, диуретиков и бета-адреноблокаторов.В последние годы появилось очень мало новых лекарственных препаратов для лечения гипертонии. Поэтому для врачей крайне важно оптимизировать свою гипотензивную терапию с помощью препаратов, доступных на рынке. В отношении каждого из классов гипотензивных препаратов в последнее время возникли вопросы: превосходят ли ингибиторы ангиотензинпревращающего фермента (АПФ) блокаторы рецепторов ангиотензина II (БРА)? Можно ли уменьшить частоту возникновения периферических отеков с помощью антагонистов кальция? Действительно ли гидрохлоротиазид — хорошее мочегонное средство для комбинированной терапии? Цель этого обзора — обсудить эти различные вопросы в свете последних клинических исследований и метаанализов.Последние предполагают, что ингибиторы АПФ и БРА эквивалентны, за исключением лучшего профиля переносимости БРА. Блокаторы кальциевых каналов третьего поколения позволяют снизить частоту возникновения периферических отеков, а хлорталидон, безусловно, более эффективен, чем гидрохлоротиазид, в предотвращении сердечно-сосудистых событий при гипертонии. Наконец, исследования показывают, что соблюдение режима приема лекарств и их длительная устойчивость при терапии являются одними из основных вопросов в реальном лечении эссенциальной гипертензии.
Введение
Ведение пациентов с эссенциальной гипертензией в основном основывается на назначении антигипертензивных препаратов, которые позволяют снизить артериальное давление до рекомендуемых целевых значений <140/90 мм рт. Ст. В общей популяции и до более низких уровней (<135/85 мм рт. Ст.) Для некоторых группы пациентов, такие как диабетики или пациенты с хроническими заболеваниями почек. 1,2 За последние 10 лет на рынке появилось очень мало новых антигипертензивных средств, и на самом деле не появилось никакого нового терапевтического класса, если рассматривать ингибиторы ренина как препараты, ингибирующие ренин-ангиотензиновую систему (РАС). Таким образом, реальная стратегия контроля артериального давления при гипертонии основана на использовании трех основных классов антигипертензивных препаратов, т. Е. Блокаторов РАС, блокаторов кальциевых каналов (БКК) и диуретиков (D), как указано в последних рекомендациях по гипертонии 2013 г. Европейское общество гипертонии и Европейское общество кардиологов. 3 В некоторых клинических условиях, таких как пациенты с ишемической болезнью сердца и сердечной недостаточностью, бета-адреноблокаторы все еще имеют свое место, и это причина, по которой они были сохранены в рекомендациях по артериальной гипертензии 2013 года. 3 Лекарства, такие как периферические вазодилататоры, нитраты или альфа-адреноблокаторы, больше не рекомендуются в качестве терапии первой линии, хотя они могут быть полезны в редких случаях, например, у чернокожих гипертоников с сердечной недостаточностью. Аналогичным образом, антагонисты рецепторов альдостерона (альдактон или эплеренон) предназначены для некоторых особых показаний, таких как первичный альдостеронизм, резистентная гипертензия или гипертония, связанная с застойной сердечной недостаточностью.
Систематический обзор рандомизированных плацебо-контролируемых исследований пяти основных категорий препаратов, снижающих артериальное давление, то есть ингибиторов ангиотензинпревращающего фермента (АПФ), блокаторов рецепторов ангиотензина II, диуретиков, БКК и бета-блокаторов фактически продемонстрировал, что все пять категорий препаратов вызывают одинаковое снижение артериального давления. 4 Среднее снижение достигает 9,1 мм рт. Ст. Систолического и 5,5 мм рт. Ст. Диастолического при стандартной дозе и 7,1 мм рт. Ст. Систолического и 4,4 мм рт. Ст. Диастолического при половинной стандартной дозе.Однако профиль переносимости этих классов значительно отличается: диуретики, БКК и бета-адреноблокаторы вызывают дозозависимые побочные эффекты — наблюдение, которое не было сделано с ингибиторами АПФ. 4 Блокаторы рецепторов ангиотензина II имеют лучший профиль переносимости среди всех классов гипотензивных препаратов. Основное преимущество этих пяти классов препаратов заключается в том, что они снижают артериальное давление с помощью различных механизмов. Таким образом, их можно эффективно комбинировать, а их антигипертензивная эффективность является аддитивной.Единственным исключением является комбинация двух блокаторов РАС, которая связана с повышенным риском почечных событий и гиперкалиемии и поэтому не показана.
Сегодня, хотя концепция терапии первой линии имеет тенденцию исчезать, 3 большинство руководств рекомендуют начинать терапию с блокатора РАС или БКК в большинстве состояний, как это рекомендовано, например, британскими руководящими принципами 5 и самые последние рекомендации ESH-ESC. 3 Однако выбор терапии первой линии часто определяется наличием или отсутствием сопутствующих заболеваний, как показано на Рис. 1 .Из последних европейских рекомендаций очевидно, что блокаторы РАС являются предпочтительным классом для начала терапии гипертонических пациентов со всеми сопутствующими заболеваниями, кроме ишемической болезни сердца.
Рисунок 1
Убедительные показания для классов антигипертензивных препаратов в зависимости от сопутствующих заболеваний (адаптировано из Mancia et al. . 1,3 ). Блокатор РАС, блокаторы ренин-ангиотензиновой системы; D, диуретики; БКК, блокаторы кальциевых каналов.
Рисунок 1
Убедительные показания для классов антигипертензивных препаратов в зависимости от сопутствующих заболеваний (адаптировано из Mancia et al. . 1,3 ). Блокатор РАС, блокаторы ренин-ангиотензиновой системы; D, диуретики; БКК, блокаторы кальциевых каналов.
Цель настоящего обзора — обсудить некоторые обсуждаемые вопросы, касающиеся терапии гипертонии первой линии, и представить текущие разработки фармакологии гипертонии.
Ингибиторы ангиотензинпревращающего фермента или блокаторы рецепторов ангиотензина II: ложные дебаты?
БлокаторыРАС доступны для лечения эссенциальной гипертензии с начала 1980-х годов, когда были разработаны ингибиторы АПФ.С тех пор было накоплено неопровержимое количество доказательств того, что ингибиторы АПФ значительно снижают артериальное давление и оказывают очень благоприятное влияние на заболеваемость и смертность пациентов не только с гипертонической болезнью, но и у пациентов с сердечной недостаточностью и пациентов с диабетом и недиабетом. нефропатии. В 1990-е годы стали доступны блокаторы рецепторов ангиотензина (БРА). 6 Эти последние предоставили возможность блокировать RAS на другом уровне, то есть на рецепторе AT1 с потенциалом вызвать более полную блокаду системы, при этом все эффекты ангиотензина II ингибируются на уровне рецептора независимо от источника. ангиотензина II.Клинические исследования быстро продемонстрировали, что БРА столь же эффективны, как и ингибиторы АПФ, в снижении артериального давления, 7 , но также в снижении протеинурии и замедлении прогрессирования почечных заболеваний. Блокаторы рецепторов ангиотензина II были также эффективны при сердечной недостаточности, как и ингибиторы АПФ. 8,9
По мере накопления исследований и испытаний с использованием ингибиторов АПФ и БРА было выполнено несколько метаанализов для сравнения клинических преимуществ этих двух подходов к блокированию системы РАС.Эти метаанализы вызвали некоторые дискуссии о потенциальном превосходстве ингибиторов АПФ над БРА в снижении общей и сердечно-сосудистой смертности, а также о влиянии БРА на частоту инфаркта миокарда. 8–10 Один из метаанализов, включающий более свежие исследования, показал, что БРА и ингибиторы АПФ обладают схожими клиническими преимуществами. 9 Однако в более позднем метаанализе, проведенном van Vark et al . и включая> 150000 пациентов, блокада РАС была связана со значительным снижением общей и сердечно-сосудистой смертности по сравнению с контрольными методами лечения, но авторы обнаружили снижение смертности только у пациентов, получавших ингибитор АПФ, а не у пациентов, получавших БРА, хотя разница между БРА и ингибиторами АПФ не достигли статистической значимости. 10 Согласно этому метаанализу, ингибиторы АПФ были продвинуты как превосходящие БРА с вопросительным знаком о роли БРА в предотвращении коронарных событий. Еще совсем недавно Savarese et al . 11 провели еще один метаанализ, сравнивая два класса блокаторов РАС у пациентов с высоким сердечно-сосудистым риском без сердечной недостаточности. В этом анализе, который включал 26 рандомизированных исследований с участием> 100 000 пациентов, как ингибиторы АПФ, так и БРА снижали риск комбинированных конечных точек инфаркта миокарда, инсульта и сердечно-сосудистой смертности.Было обнаружено снижение риска смерти от всех причин при применении ингибиторов АПФ. Таким образом, авторы пришли к выводу, что БРА представляют собой ценную альтернативу ингибиторам АПФ у пациентов, у которых нельзя применять ингибиторы АПФ. 11 В этом отношении наиболее важным исследованием, о котором стоит упомянуть, несомненно, является продолжающееся исследование телмисартана в отдельности и в сочетании с глобальным испытанием Ramipril Global Endpoint (ONTARGET), в котором фактически сравнивали ингибитор АПФ рамиприл с телмисартаном ARB у пациентов с высоким сердечно-сосудистым риском, большая часть они гипертоники. 12 Как показано на фиг. 2 , не было существенной разницы между ингибитором АПФ и БРА с точки зрения общей или сердечно-сосудистой смертности. Также не было разницы при рассмотрении инфаркта миокарда, госпитализации по поводу сердечной недостаточности или инсульта. Таким образом, единственное крупное испытание, сравнивающее два варианта лечения, не выявило каких-либо существенных различий, за исключением частоты побочных эффектов. Действительно, профиль переносимости БРА был лучше, чем у ингибитора АПФ, при значительно меньшем количестве кашля и ангионевротического отека.Что касается последнего осложнения, которое в некоторых случаях может быть опасным для жизни, недавний метаанализ подтверждает данные ONTARGET, показывающие, что риск развития ангионевротического отека у пациентов, принимающих ингибитор АПФ, увеличивался в два раза по сравнению с пациентами, получающими БРА. 12,13 Профиль переносимости препаратов является важным фактором, определяющим частоту отмены лечения у пациентов с гипертонией. Таким образом, недавнее исследование в Италии продемонстрировало, что БРА с длительным действием имеют наименьшую частоту отмены по сравнению с БРА короткого действия или ингибиторами АПФ в целом (, рис. 3, ). 14
Рисунок 2
Влияние телмисартана и рамиприла на сердечно-сосудистые конечные точки в исследовании ONTARGET (адаптировано из Юсуфа и др. . 12 ).
Рисунок 2
Влияние телмисартана и рамиприла на конечные точки сердечно-сосудистой системы в исследовании ONTARGET (адаптировано из Юсуфа и др. . 12 ).
Рисунок 3
Приверженность сердечно-сосудистым препаратам в первичной профилактике.Результаты метаанализа (адаптировано из Надери и др. . 45 ).
Рисунок 3
Приверженность сердечно-сосудистым препаратам в первичной профилактике. Результаты метаанализа (адаптировано из Надери и др. . 45 ).
Совсем недавно стал доступен третий подход к ингибированию РАС, а именно прямое ингибирование ренина с использованием алискирена. Этот новый способ блокирования системы ренин-ангиотензин-альдостерон был очень многообещающим, поскольку он давал уникальную возможность блокировать РАС на начальном этапе.В клинических исследованиях было обнаружено, что алискирен является эффективным антигипертензивным препаратом длительного действия с сопоставимой эффективностью с БРА и ингибиторами АПФ. 15 К сожалению, смягченные результаты крупных клинических испытаний, в частности, ALTITUDE 16 , показывающие отсутствие реальной пользы от другого блокатора РАС у пациентов с диабетом 2 типа, значительно снизили первоначальный энтузиазм и в настоящее время, хотя алискирен все еще остается доступный на некоторых рынках для лечения гипертонии отдельно или в комбинации с диуретиком или БКК, его будущее находится под угрозой, поскольку трудно продемонстрировать дополнительные преимущества по сравнению с ингибиторами АПФ или БРА.Следует отметить, что недавние руководства ESH-ESC не рекомендуют использовать алискирен в сочетании с другим блокатором РАС. 3
Таким образом, споры между ингибиторами АПФ и БРА являются ложными, поскольку обе группы препаратов очень эффективны и обеспечивают важные клинические преимущества при гипертонии. Улучшенный профиль переносимости БРА дает им небольшое преимущество, но последнее часто уравновешивается более низкой стоимостью ингибиторов АПФ, хотя в настоящее время как большинство ингибиторов АПФ, так и некоторые БРА доступны в виде дженериков.
Блокаторы кальциевых каналов: как насчет дигидропиридинов третьего поколения?
Блокаторы кальциевых каналов представляют собой гетерогенную группу гипотензивных препаратов, в которую входят верапамил, дилтиазем и дигидропиридины. Сегодня дигидропиридин амлодипин длительного действия второго поколения в значительной степени занял лидирующее место в назначении БКК, поскольку это соединение стало универсальным. Более того, результаты нескольких крупных клинических испытаний, таких как исследование антигипертензивного и липидоснижающего лечения для предотвращения сердечного приступа (ALLHAT), 17 , исследование оценки долгосрочного использования антигипертензивных средств валсартана (VALUE), 18 , англо-скандинавское Исследование сердечных исходов (ASCOT), 19 или исследование ACCOMPLISH (предотвращение сердечно-сосудистых событий с помощью комбинированной терапии у пациентов с систолической гипертензией) 20 подчеркнули интерес к назначению этого типа соединения для достижения целевых показателей артериального давления при гипертонии.Таким образом, амлодипин в настоящее время является наиболее частым компонентом БКК в комбинациях фиксированных доз в сочетании с блокатором РАС.
В клинической практике частота прекращения приема БКК довольно высока, а длительная устойчивость БКК ниже, чем наблюдаемая при применении блокаторов РАС. 21 Основной причиной прекращения приема БКК является появление периферических отеков. В исследовании VALUE, в котором амлодипин сравнивали с валсартаном, у 14,9% пациентов развились периферические отеки на фоне приема БРА, а у 32 пациентов.9% с амлодипином. 18 Таким образом, этим побочным эффектом страдает треть пациентов. Известно, что сочетание CCB с блокатором RAS снижает частоту периферических отеков из-за эффектов блокады RAS на прекапиллярное давление. 22 Тем не менее, в ASCOT, который сравнивал комбинацию периндоприла и амлодипина с комбинацией тиазидного диуретика и бета-блокатора атенолола, 23% пациентов жаловались на периферический отек и 14% — на опухоль суставов в группе периндоприла / амлодипина. . 19 Это говорит о том, что даже в сочетании с блокатором РАС частота периферических отеков остается высокой и может быть ограничивающим фактором для продолжительной продолжительности лечения.
Можно ли снизить частоту возникновения периферических отеков с помощью БКК нового поколения? В последние годы на некоторых рынках стали доступны несколько новых БКК третьего поколения, таких как лерканидипин, лацидипин или манидипин. Основной характеристикой этих БКК является то, что они вызывают меньше периферических отеков, чем классические БКК второго поколения.Таким образом, несколько исследований продемонстрировали снижение частоты периферических отеков при использовании этих новых БКК. Borghi и др. . показали, что частота возникновения периферических отеков может быть снижена на 50% у пациентов, у которых развился отек после приема амлодипина и которые были переведены на лерканидипин. 23 Аналогичным образом, в большом исследовании (исследование COHORT) периферические отеки возникли у 18% пациентов, получавших амлодипин, но только у 7 и 4% пациентов, получавших соответственно лерканидипин и лацидипин. 24 В крупном швейцарском исследовании, в котором пациенты либо начинали, либо переключали на лерканидипин, либо лерканидипин добавлялся к другим видам лечения, частота отека голеностопного сустава составила> 4% через 6 месяцев. 25 Было показано, что использование этих новых БКК третьего поколения улучшает устойчивость лекарства у пролеченных пациентов с гипертонией по сравнению с другими БКК со значениями стойкости, близкими к показателям блокатора РАС. 26
В совокупности эти результаты позволяют предположить, что БКК третьего поколения может помочь снизить частоту периферических отеков у пациентов с гипертонией.Сегодня на рынке представлены новые комбинации фиксированных доз, которые сочетают в себе блокатор РАС и БКК третьего поколения, такие как эналаприл / лерканидипин. 27 Было показано, что эти новые ассоциации эффективны и хорошо переносятся при ведении пациентов с гипертонией, в том числе с диабетической нефропатией. 28 Их главное ограничение, однако, состоит в том, что эти комбинации никогда не исследовались в исследованиях контролируемой заболеваемости / смертности.
Диуретики: гидрохлоротиазид или хлорталидон?
Диуретики относятся к основным классам гипотензивных средств, и их назначение остается высоким, несмотря на появление новых терапевтических классов.Действительно, из-за высокого потребления соли населением и хорошо известной роли потребления соли в развитии эссенциальной гипертензии диуретики играют важную роль в лечении пациентов с гипертонией. Сегодня диуретики нечасто назначают в качестве единственного средства, но чаще в сочетании с блокатором РАС. На рынке доступно несколько диуретиков для лечения гипертонии, включая гидрохлоротиазид (HCTZ), хлорталидон и индапамид.В клинической практике ГХТЗ выписывается чаще, чем все диуретики, в основном потому, что он стал референтным диуретиком во всех комбинациях с фиксированными дозами.
В последнее время возникло несколько вопросов относительно места HCTZ в лечении гипертонии. 29 Действительно ли HCTZ является наиболее эффективным диуретиком в рекомендуемых дозах? Является ли ГХТЗ таким же эффективным, как и другие диуретики, в предотвращении сердечно-сосудистых событий, таких как инсульт, инфаркт миокарда или смерть? Действительно, анализ исследований показал, что HCTZ менее эффективен в снижении артериального давления, чем блокаторы RAS или CCB, и, таким образом, вызывает меньшую защиту сердечно-сосудистой системы, чем последние.Более того, почти во всех крупных исследованиях, таких как ALLHAT, 17 SHEP (Систолическая гипертензия у пожилых людей) 30 или HYpertension in the Very Elderly Trial (HYVET) 31 , демонстрирующих пользу диуретиков для сердечно-сосудистой системы, использовался хлорталидон. или индапамид, но не HCTZ.
Таким образом, недавно было проведено несколько апостериорных анализов для оценки антигипертензивной эффективности HCTZ в клинических исследованиях и для сравнения HCTZ с другими диуретиками, в частности с хлорталидоном.В исследовании Peterzan et al был проведен метаанализ для изучения зависимости доза-реакция различных диуретиков, используемых для лечения гипертонии. 32 В исследованиях, включенных в анализ, участвовали 4683 пациента в более чем 53 группах сравнения. Согласно этому анализу, HCTZ, хлорталидон и бендрофлуметиазид имели заметно различающуюся активность, причем самая низкая эффективность приписывалась HCTZ. Однако не было доказательств разницы в максимальном снижении систолического АД высокими дозами разных тиазидов.Разница в эффективности, наблюдаемая в отношении артериального давления между тиазидными диуретиками, также была замечена в отношении изменений уровней калия и мочевой кислоты в сыворотке крови. Авторы пришли к выводу, что разница в антигипертензивной эффективности различных тиазидных диуретиков в основном связана с их активностью. В другом анализе Roush et al . 33 выполнили систематический обзор рандомизированных исследований, в которых одна группа была основана на HCTZ или хлорталидоне, за которыми следовали два типа сетевых метаанализов: анализ с поправкой на лекарство и анализ с поправкой на систолическое артериальное давление в офисе.Интересно, что при сопоставимом снижении артериального давления было обнаружено, что риск развития сердечно-сосудистых событий выше при применении ГХТЗ, чем при применении хлорталидона. Следует отметить, что по сравнению с HCTZ количество, необходимое для лечения хлорталидоном, чтобы избежать одного сердечно-сосудистого события, составило 27. Таким образом, результаты этого анализа предполагают, что хлорталидон превосходит HCTZ в предотвращении сердечно-сосудистых событий.
Принимая во внимание эти недавние исследования, разрабатываются новые комбинации препаратов, в которых хлорталидон, а не ГХТЗ, связан с блокатором РАС.Так обстоит дело, например, с блокатором рецепторов ангиотензина II азилсартаном медоксомилом, который будет доступен в сочетании с хлорталидоном. 34,35 Бакрис и др. . 34 фактически сравнивали антигипертензивную эффективность комбинации азилсартан + HCTZ и азилсартан + хлорталидон. Глядя на изменения в офисе, а также на амбулаторное артериальное давление, было обнаружено, что ARB-хлорталидон вызывает более сильное падение артериального давления. В другом клиническом исследовании Cushman et al .исследовали 12-недельные изменения артериального давления, вызванные азилсартаном / хлорталидоном 40/25 или 80/25 мг по сравнению с олмесартаном / HCTZ 40/25 мг у пациентов с артериальной гипертензией. 35 Все комбинации фиксированных доз вызывали заметное и устойчивое 24-часовое снижение артериального давления, но две дозы азилсартана / хлорталидона оказались лучше, чем комбинация олмесартан / HCTZ.
Таким образом, все чаще ведутся споры о том, какой диуретик является наиболее подходящим для лечения пациентов с гипертонией.Хотя неоднократно было показано, что HCTZ оказывает аддитивный антигипертензивный эффект при введении в сочетании с блокатором RAS, некоторые люди ставят под сомнение выбор HCTZ во всех комбинациях фиксированных доз и предполагают, что на самом деле можно предпочесть либо хлорталидон, либо индапамид, для которых существует еще больше клинических доказательств положительного воздействия на сердечно-сосудистые заболевания. Действительно, и хлорталидон, и индапамид успешно использовались в крупных клинических испытаниях, особенно у пожилых пациентов с артериальной гипертензией. 31 Как указано в последних рекомендациях ESH-ESC, 3 сегодня не может быть сделано никаких конкретных рекомендаций в пользу одного диуретика на основе фактических клинических данных.
А как насчет бета-адреноблокаторов?
Использование бета-блокаторов в лечении пациентов с гипертонией подвергалось сомнению в некоторых руководствах, и британские ученые не приняли во внимание бета-блокаторы в своих рекомендациях в качестве терапии первой линии из-за их меньшей способности предотвращать инсульт в исследовании ASCOT 19 и их неспособность снизить центральное кровяное давление.В последних рекомендациях ESH-ESC по гипертензии 3 ; однако бета-адреноблокаторы остаются терапевтическим вариантом, особенно для пациентов с гипертонией и сердечными заболеваниями, такими как сердечная недостаточность или ишемическая болезнь сердца. Также подчеркивается, что не все бета-адреноблокаторы обладают одинаковыми свойствами и что новые бета-блокаторы, такие как небиволол или карведилол, могут не обладать такими же сосудистыми и метаболическими эффектами, как атенолол или метопролол. 36,37 Например, как небиволол, так и карведилол снижают центральное кровяное давление в отличие от атенолола и метопролола.Тем не менее, следует отметить, что новые бета-адреноблокаторы были исследованы в основном у пациентов с сердечной недостаточностью, и очень мало исследований было проведено с этими агентами при артериальной гипертензии.
Что ждет гипотензивную терапию в будущем?
Фармакологическое лечение гипертонии в основном основывается на классах препаратов, описанных выше, с их преимуществами и ограничениями. Сегодня изучается несколько новых терапевтических лекарственных стратегий, которые могут стать доступными в ближайшем будущем.Антагонисты эндотелина изучались при артериальной гипертензии, но из-за их профиля побочных эффектов (головные боли и задержка жидкости) в настоящее время основное внимание уделяется применению этих агентов при резистентной гипертензии или гипертонии при заболеваниях почек. 38 Комбинация ингибитора АПФ и ингибитора нейтральной эндопептидазы была исследована в 1980-х годах и дала хорошую антигипертензивную эффективность, но увеличила частоту ангионевротического отека. По этой причине проект был заброшен.Совсем недавно были исследованы новые попытки комбинировать БРА с ингибитором неприлизина, и было высказано предположение, что ингибирование системы РАС и усиление вазодилатации, вызванной натрийуретическими пептидами предсердий, может быть эффективным способом снижения артериального давления. 39,40 Ожидается также новая стратегия в области блокады альдостерона с разработкой ингибиторов альдостерон-синтазы. Некоторые исследования фаз II и III с этими соединениями продолжаются. 41 Наконец, потенциальные преимущества ингибирования ро-киназы изучаются при артериальной гипертензии, но предстоит пройти еще долгий путь, пока этот класс соединений не появится на рынке. 42
Пока эти новые методы лечения отсутствуют на рынке, врачам придется делать все возможное, чтобы контролировать артериальное давление с помощью имеющихся инструментов. В этом отношении интересно отметить разрыв между результатами, полученными в клинических испытаниях, где до 80% пациентов могут достичь целевого артериального давления, и реальной ситуацией в большинстве стран, где в лучшем случае ∼50% пациентов с контролируемой кровью. давление. Помимо проблемы терапевтической инерции, одной из наиболее важных проблем в лечении гипертонии является прогрессирующая частота прекращения лечения пациентами, которые не продолжают лечение. 43 Низкая стойкость гипертонии была четко доказана у пациентов, лечившихся от гипертонии в исследованиях фазы IV. 44 Недавний метаанализ также показал, что длительная приверженность к сердечно-сосудистым препаратам особенно низка как при первичной, так и при вторичной профилактике сердечно-сосудистых заболеваний. 45 Таким образом, необходимо приложить все усилия для улучшения устойчивости лекарственного средства при гипертонии, чтобы получить полную клиническую пользу от назначенного лечения.
Конфликт интересов : не заявлено.
Список литературы
1,,,,,,,,,,,,,,,.Целевая группа ESH-ESC по лечению артериальной гипертензии
2007 Практические рекомендации ESH-ESC по лечению артериальной гипертензии: Целевая группа ESH-ESC по лечению артериальной гипертензии
,J Hypertens
,2007
, vol. .25
(стр.1751
—1762
) 2,,,,,,,,,,.Национальный институт сердца, легких и крови Объединенный национальный комитет по профилактике, обнаружению, оценке и лечению высокого кровяного давления; Координационный комитет Национальной образовательной программы по высокому кровяному давлению: Седьмой отчет Объединенного национального комитета по профилактике, выявлению, оценке и лечению повышенного кровяного давления: отчет JNC 7
,JAMA
,2003
, vol.289
(стр.2560
—2571
) 3,,,,,,,,,,,,,,,,,,,,,,.2013 г. Руководство ESH / ESC по лечению артериальной гипертензии. Рабочая группа по ведению артериальной гипертензии Европейского общества гипертонии (ESH) и Европейского общества кардиологов (ESC)
,J Hypertens
,2013
, vol.31
(стр.1281
—1357
) 4,,.Ценность комбинированного лечения низкими дозами препаратами, снижающими артериальное давление: анализ 354 рандомизированных исследований
,BMJ
,2003
, vol.326
(стр.1427
—1431
) 5,,.Национальный институт здравоохранения и клинического совершенства
NICE Руководство по артериальной гипертензии 2011: эволюция на основе фактических данных
,BMJ
,2012
, vol.344
стр.e181
6.Блокаторы рецепторов ангиотензина II типа 1
,Circulation
,2001
, vol.103
(стр.904
—912
) 7,,,.Эффективность блокаторов рецепторов ангиотензина при первичной гипертензии в отношении снижения артериального давления
,Кокрановская база данных Syst Rev
,2008
, vol.4
стр.CD003822
8,,,,,,,,.Зависимые от артериального давления и независимые эффекты агентов, ингибирующих ренин-ангиотензиновую систему
,J Hypertens
,2007
, vol.25
(стр.951
—958
) 9,,,.Блокаторы рецепторов ангиотензина и риск инфаркта миокарда: метаанализы и последовательные исследования 147 020 пациентов из рандомизированных исследований
,BMJ
,2011
, vol.342
стр.d2234
10,,,,,,.Ингибиторы ангиотензинпревращающего фермента снижают смертность при гипертонии: метаанализ рандомизированных клинических испытаний ингибиторов ренин-ангиотензин-альдостероновой системы с участием 158998 пациентов
,Eur Heart J
,2012
, vol.33
(стр.2088
—2097
) 11,,,,,,.Мета-анализ, описывающий эффекты ингибиторов ангиотензинпревращающего фермента и блокаторов рецепторов ангиотензина у пациентов без сердечной недостаточности
,J Am Coll Cardiol
,2013
, vol.61
(стр.131
—142
) 12,,,,,,,,.Телмисартан, рамиприл или оба препарата у пациентов с высоким риском сосудистых событий
,N Engl J Med
,2008
, vol.358
(стр.1547
—1559
) 13,,,,,,.Мета-анализ рандомизированных исследований ангионевротического отека как побочного действия ингибиторов ренин-ангиотензиновой системы
,Am J Cardiol
,2012
, vol.110
(стр.383
—391
) 14,,,.Неоднородность прекращения антигипертензивной терапии между препаратами одного класса
,J Hypertens
,2011
, vol.29
(стр.1012
—1018
) 15,,,,,.Алискирен, новый эффективный пероральный ингибитор ренина, обеспечивает дозозависимую антигипертензивную эффективность и плацебо-подобную переносимость у пациентов с артериальной гипертензией.
,Circulation
,2005
, vol.111
(стр.1012
—1018
) 16,,,,,.Кардиоренальные конечные точки в исследовании алискирена при диабете 2 типа
,N Engl J Med
,2012
, vol.367
(стр.2204
—2213
) 17Группа совместных исследований ALLHAT
Основные исходы у пациентов с гипертонической болезнью высокого риска, рандомизированных для приема ингибитора ангиотензинпревращающего фермента или блокатора кальциевых каналов по сравнению с диуретиком: антигипертензивные и липидные Снижающее лечение для предотвращения сердечного приступа (ALLHAT)
,JAMA
,2002
, vol.288
(стр.2981
—2997
) 18,,,,,,,,,,,,,,,,,.Исследование VALUE по оценке долгосрочного использования антигипертензивных средств: исходы у пациентов, получавших монотерапию
,Гипертония
,2006
, vol.48
(стр.385
—391
) 19,,,,,,,,,,,,.Профилактика сердечно-сосудистых событий с помощью антигипертензивного режима с добавлением периндоприла при необходимости по сравнению с атенололом при добавлении бендрофлуметиазида в англо-скандинавском исследовании сердечных исходов — группа для снижения артериального давления (ASCOT-BPLA): многоцентровое рандомизированное контролируемое исследование
,
,2005
, т.366
(стр.895
—906
) 20,,,,,,,,,.ACCOMPLISH Trial Investigators
Беназеприл плюс амлодипин или гидрохлоротиазид для лечения артериальной гипертензии у пациентов с высоким риском
,N Engl J Med
,2008
, vol.359
(стр.2417
—2428
) 21,,,,,,.Периферический отек, связанный с блокаторами кальциевых каналов: частота и частота отмены — метаанализ рандомизированных исследований
,J Hypertens
,2011
, vol.29
(стр.1270
—1280
) 22,,.Сравнение эффективности и побочных эффектов комбинированной терапии ингибитором ангиотензинпревращающего фермента (беназеприл) с антагонистом кальция (нифедипином или амлодипином) с монотерапией высокими дозами антагониста кальция при системной гипертензии
,Am J Cardiol
,2000
, т.86
(стр.1182
—1187
) 23,,,.Исследовательская группа регионального отделения Итальянского общества гипертонии
Улучшенная переносимость дигидропиридинового антагониста кальциевых каналов лерканидипина: испытание лерканидипином с провокационным воздействием
,Blood Press Suppl
,2003
, vol.1
(стр.14
—21
) 24,,,,,.COHORT Study Group
Переносимость длительного лечения лерканидипином по сравнению с амлодипином и лацидипином у пожилых гипертоников
,Am J Hypertens
,2002
, vol.15
(стр.932
—940
) 25,.Эффективность и переносимость лерканидипина у пациентов с артериальной гипертензией: результаты исследования IV фазы в общей практике
,Expert Opin Pharmacother
,2007
, vol.8
(стр.2215
—2223
) 26,,,,,,.Упорство на лечении и контроль артериального давления с помощью различных антигипертензивных препаратов первой линии: проспективная оценка
,Clin Exp Hypertens
,2007
, vol.29
(стр.553
—562
) 27,.Роль комбинации фиксированных доз лерканидипин-эналаприл в защите почек
,J Нефрол
,2011
, vol.24
(стр.428
—437
) 28,,,.Эффективность и безопасность комбинации фиксированных доз лерканидипина и эналаприла в повседневной практике. Сравнение офисного, самостоятельного измерения и амбулаторного артериального давления
,Expert Opin Pharmacother
,2011
, vol.12
(стр.2771
—2779
) 29,.Полвека гидрохлоротиазида: факты, фантазии, выдумки и глупости
,Am J Med
,2011
, vol.124
(стр.896
—899
) 30Профилактика инсульта с помощью антигипертензивной лекарственной терапии у пожилых людей с изолированной систолической гипертензией. Окончательные результаты программы «Систолическая гипертензия у пожилых людей» (SHEP). SHEP Cooperative Research Group
,JAMA
,1991
, т.265
(стр.3255
—3264
) 31,,,,,,,,,,,,,.HYVET Study Group
Лечение гипертонии у пациентов в возрасте 80 лет и старше
,N Engl J Med
,2008
, vol.358
(стр.1887
—1898
) 32,,,.Метаанализ зависимости доза-ответ гидрохлоротиазида, хлорталидона и бендрофлуметиазида от артериального давления, калия в сыворотке и уратов
,Гипертония
,2012
, vol.59
(стр.1104
—1109
) 33,,.Хлорталидон в сравнении с гидрохлоротиазидом в снижении сердечно-сосудистых событий: систематический обзор и сетевой метаанализ
,Гипертензия.
,2012
, т.59
(стр.1110
—1117
) 34,,,,,,,.Антигипертензивная эффективность гидрохлоротиазида по сравнению с хлорталидоном в сочетании с азилсартаном медоксомилом
,Am J Med
,2012
, vol.125
(стр.1229.e1
—1229.e10
) 35,,,,,,,.Азилсартан медоксомил плюс хлорталидон снижает артериальное давление более эффективно, чем олмесартан плюс гидрохлоротиазид, при систолической гипертензии 2 стадии
,Гипертония
,2012
, vol.60
(стр.310
—318
) 36,,,,,,,.Дифференциальное влияние небиволола и метопролола на центральное давление в аорте и толщину стенки левого желудочка
,Гипертония
,2011
, vol.57
(стр.1122
—1128
) 37,,,,,,,,,,.GEMINI Investigators
Метаболические эффекты карведилола по сравнению с метопрололом у пациентов с сахарным диабетом 2 типа и гипертонией: рандомизированное контролируемое исследование
,JAMA
,2004
, vol.292
(стр.2227
—2236
) 38,.Антагонисты рецепторов эндотелина: место в лечении гипертонической болезни?
,Циферблат нефрола
,2012
, т.27
(стр.865
—868
) 39,,.Двойное нейрогормональное вмешательство при сердечно-сосудистых заболеваниях: ингибирование рецептора ангиотензина и неприлизина
,Экспертное заключение, исследуемое лекарство
,2013
, vol.22
(стр.915
—925
) 40,,,,,.Снижение артериального давления с помощью LCZ696, нового ингибитора двойного действия рецептора ангиотензина II и неприлизина: рандомизированное, двойное слепое, плацебо-контролируемое, активное исследование сравнения
,Lancet
,2010
, vol.375
(стр.1255
—1266
) 41,,,,.Последовательное сравнение ингибирования альдостерон-синтазы и минералокортикоидной блокады у пациентов с первичным альдостеронизмом
,J Hypertens
,2013
, vol.31
(стр.624
—629
) 42.Возможные преимущества ингибирования ро-киназы при артериальной гипертензии
,Curr Hypertens Rep
,2013
, vol.15
(стр.506
—513
) 43,,,.Измерение, анализ и контроль соблюдения режима лечения при резистентной гипертензии
,Гипертония
,2013
, vol.62
(стр.218
—225
) 44,,,,.Соблюдение назначенных антигипертензивных препаратов: продольное исследование электронных историй дозирования
,BMJ
,2008
, vol.336
(стр.1114
—1117
) 45,,.Приверженность к лекарствам, предотвращающим сердечно-сосудистые заболевания: метаанализ на 376 162 пациентах
,Am J Med
,2012
, vol.125
(стр.882
—887
)Издается от имени Европейского общества кардиологов. Все права защищены. © Автор, 2013. Для получения разрешений обращайтесь по электронной почте: [email protected]
Несколько препаратов, содержащих лозартан, добровольно отозваны из-за потенциальной примеси нитрозаминов
9 марта 2019 г.
Для немедленного выпуска
ОТТАВА — Министерство здравоохранения Канады сообщает канадцам, что несколько партий препаратов, содержащих лозартан, добровольно отзываются Teva Canada, Apotex Inc., Pharmascience Inc. и Pro Doc Limitée из-за потенциальной примеси нитрозамина, N-нитрозо-N-метил-4-аминомасляной кислоты (NMBA).
NMBA потенциально является канцерогеном для человека, а это означает, что длительное воздействие может увеличить потенциальный риск рака.
Teva Canada добровольно отзывает две партии комбинированных таблеток лозартан / гидрохлоротиазид (HCTZ) после тестирования одной партии, выявившей уровни NMBA, превышающие разумно безопасные, если препарат принимался в течение всей жизни.Apotex Inc., Pharmascience Inc. и Pro Doc Limitée добровольно отзывают несколько партий продуктов, содержащих лозартан, в качестве меры предосторожности.
Активный фармацевтический ингредиент лозартана (API) во всех отозванных продуктах производится компанией Hetero Labs Ltd. Unit 1 в Индии. Эти отзывы относятся ко всем партиям лекарств, распространяемых в Канаде, которые содержат Лозартан API, произведенные в Hetero Labs Ltd. Unit 1.
Лозартан — препарат, блокирующий рецепторы ангиотензина (БРА), также известный как «сартан».«Сартаны — это класс лекарств, используемых для лечения пациентов с высоким кровяным давлением, чтобы предотвратить сердечные приступы и инсульт. Они также используются у пациентов, перенесших сердечную недостаточность или недавно перенесший сердечный приступ. С июля 2018 года в Канаде и за рубежом неоднократно отзывались продукты, содержащие еще один сартан, валсартан, из-за примесей нитрозаминов (дополнительную информацию см. По ссылкам ниже).
Как и в случае с предыдущими отзывами, связанными с примесями нитрозаминов, Министерство здравоохранения Канады сообщает, что нет непосредственного риска для пациентов, принимающих эти лекарства, поскольку потенциальный риск рака связан с долгосрочным воздействием примесей.Пациентам не следует прекращать прием лекарств, если это не рекомендовано их лечащим врачом.
В настоящее время на канадском рынке доступны альтернативные продукты. Министерство здравоохранения Канады продолжает следить за ситуацией с поставками. Министерство здравоохранения Канады рекомендует канадцам посетить сайт drugshortagescanada.ca для получения информации о нехватке и прекращении приема лекарств. Пациенты, у которых есть вопросы или опасения по поводу любого лекарства, которое они принимают, в том числе о том, что делать, если это лекарство недоступно, должны поговорить со своим лечащим врачом.
Канадцы с вопросами об отзывах могут обращаться по телефону:
Apotex Inc. через Stericyle Inc. по бесплатному телефону 1-877-492-4795;
Pharmascience Inc., позвонив по бесплатному телефону 1-800-340-9735;
Pro Doc Limitée, позвонив по бесплатному телефону 1-800-361-8559 или по электронной почте [email protected]; или
Teva Canada по бесплатному телефону 1-800-268-4129 или по электронной почте [email protected].
Министерство здравоохранения Канады призывает потребителей сообщать в Департамент о любых побочных эффектах или жалобах, связанных с продуктами для здоровья.
Затронутые продукты
Отзыв следующих продуктов, содержащих лозартан, производства Hetero Labs Ltd. Unit 1. Министерство здравоохранения Канады ведет полный список препаратов сартана, которые были отозваны из-за примесей нитрозаминов, на своем веб-сайте.
| Название продукта / активный фармацевтический ингредиент (API) | DIN | Прочность | Лот | Срок годности |
|---|---|---|---|---|
| АПО-ЛОСАРТАН | 02379058 | 25 мг | NL1453 | 08/2019 |
| АПО-ЛОСАРТАН | 02379058 | 25 мг | NL1452 | 08/2019 |
| АПО-ЛОСАРТАН | 02353504 | 50 мг | NK1254 | 08/2019 |
| АПО-ЛОСАРТАН | 02353504 | 50 мг | NK1253 | 08/2019 |
| АПО-ЛОСАРТАН | 02353512 | 100 мг | NL1461 | 08/2019 |
| АПО-ЛОСАРТАН | 02353512 | 100 мг | NG2092 | 04/2019 |
| АПО-ЛОСАРТАН | 02353512 | 100 мг | NH5932 | 06/2019 |
| АПО-ЛОСАРТАН | 02353512 | 100 мг | NH5933 | 06/2019 |
| АПО-ЛОСАРТАН | 02353512 | 100 мг | NL1460 | 08/2019 |
| АПО-ЛОСАРТАН | 02353512 | 100 мг | NH5934 | 06/2019 |
| APO-LOSARTAN / HCTZ | 02371235 | 50/12.5 мг | NL1441 | 08/2019 |
| APO-LOSARTAN / HCTZ | 02371235 | 50 / 12,5 мг | NZ8848 | 05/2020 |
| APO-LOSARTAN / HCTZ | 02371235 | 50 / 12,5 мг | NL1445 | 08/2019 |
| APO-LOSARTAN / HCTZ | 02371235 | 50/12.5 мг | NZ8849 | 05/2020 |
| APO-LOSARTAN / HCTZ | 02371235 | 50 / 12,5 мг | NZ8860 | 05/2020 |
| APO-LOSARTAN / HCTZ | 02371243 | 100 / 12,5 мг | NG2087 | 04/2019 |
| APO-LOSARTAN / HCTZ | 02371243 | 100/12.5 мг | NL1421 | 10/2019 |
| APO-LOSARTAN / HCTZ | 02371243 | 100 / 12,5 мг | NG2086 | 04/2019 |
| APO-LOSARTAN / HCTZ | 02371243 | 100 / 12,5 мг | NL1422 | 10/2019 |
| APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NL1429 | 08/2019 |
| APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NZ8846 | 05/2020 |
| APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NZ8847 | 05/2020 |
| APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NZ8845 | 05/2020 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394367 | 25 мг | 498292 | 03/2019 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394367 | 25 мг | 605344 | 02/2020 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 498779 | 03/2019 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 600046 | 06/2019 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 603903 | 11/2019 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 498284 | 03/2019 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 603895 | 11/2019 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394383 | 100 мг | 499008 | 03/2019 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394383 | 100 мг | 605299 | 01/2020 |
| ЛОСАРТАН (PRO DOC LIMITEE) | 02394383 | 100 мг | 605297 | 01/2020 |
| ПМС-ЛОСАРТАН | 02309750 | 25 мг | 498294 | 03/2019 |
| ПМС-ЛОСАРТАН | 02309750 | 25 мг | 605342 | 02/2020 |
| ПМС-ЛОСАРТАН | 02309750 | 25 мг | 611944 | 01/2021 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 498285 | 03/2019 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 600047 | 06/2019 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 600091 | 06/2019 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 603894 | 11/2019 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 612025 | 01/2021 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 612031 | 01/2021 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 612679 | 01/2021 |
| ПМС-ЛОСАРТАН | 02309769 | 50 мг | 616743 | 08/2021 |
| ПМС-ЛОСАРТАН | 02309777 | 100 мг | 498864 | 03/2019 |
| ПМС-ЛОСАРТАН | 02309777 | 100 мг | 602668 | 09/2019 |
| ПМС-ЛОСАРТАН | 02309777 | 100 мг | 603816 | 09/2019 |
| ПМС-ЛОСАРТАН | 02309777 | 100 мг | 605298 | 01/2020 |
| ПМС-ЛОСАРТАН | 02309777 | 100 мг | 605300 | 01/2020 |
| ПМС-ЛОСАРТАН | 02309777 | 100 мг | 613935 | 03/2021 |
| ПМС-ЛОСАРТАН | 02309777 | 100 мг | 613936 | 03/2021 |
| TEVA-LOSARTAN / HCTZ | 02358263 | 50/12.5 мг | 35349397A | 09/2019 |
| TEVA-LOSARTAN / HCTZ | 02358263 | 50 / 12,5 мг | 35344801A | 09/2020 |
Оценка продолжается
Министерство здравоохранения Канады продолжает работать с компаниями и международными регулирующими партнерами, включая Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и Европейское агентство по лекарственным средствам, чтобы оценить проблему примесей нитрозамина в некоторых сартановых препаратах, ее первопричины и меры по смягчению последствий.Оценка Министерства здравоохранения Канады на данный момент предполагает, что нитрозамины могут образовываться при наличии определенных химических веществ и условий реакции в процессе производства АФИ лекарственного средства. Они также могут возникать в результате повторного использования материалов, таких как растворители или исходные материалы, загрязненных примесями.
АФИ — это активный ингредиент лекарственного средства, оказывающего действие на организм. АФИ используются при производстве готовых лекарств в виде «лекарственных форм» (таких как пилюли, капсулы или таблетки).
В декабре 2018 года Министерство здравоохранения Канады обратилось ко всем компаниям, продающим сартаны в Канаде, с просьбой протестировать продукты, уже представленные на рынке, и те, которые будут выпущены в Канаде, на содержание N-нитрозодиметиламина (NDMA) и N-нитрозодиэтиламина (NDEA). Министерство здравоохранения Канады также рекомендовало компаниям рассмотреть возможность использования производственных методов, исключающих образование и присутствие всех примесей нитрозаминов. Министерство здравоохранения Канады протестировало более 50 образцов сартановых препаратов и продолжит публиковать результаты любых новых образцов на своем веб-сайте.
Министерство здравоохранения Канады по-прежнему возлагает на компании ответственность за безопасность и эффективность лекарств, продаваемых в Канаде, и ожидает, что производители предпримут все необходимые действия для предотвращения образования примесей нитрозаминов. Департамент предпримет дальнейшие шаги по мере необходимости, чтобы подтвердить, что приняты надлежащие и своевременные меры для защиты здоровья и безопасности канадцев.
Производители отозванных API сартана
На основе обзора информации от U.S. Инспекция FDA Министерства здравоохранения Канады обнаружила, что Hetero Labs Ltd. Unit 1 не соответствует требованиям надлежащей производственной практики (GMP). Рейтинг несоответствия означает, что канадские компании больше не могут импортировать лекарства, содержащие API-интерфейсы, с этого сайта, если они не являются необходимыми с медицинской точки зрения.
Как сообщалось ранее, Министерство здравоохранения Канады также обнаружило, что филиал Zhejiang Huahai Pharmaceuticals (ZHP) в Китае в Чуаннане не соответствует требованиям GMP. На этом предприятии производился валсартан, который, как было обнаружено, содержал примеси нитрозаминов.Все препараты, содержащие валсартан, производимые ZHP, отозваны в Канаде.
GMP — это международно признанные стандарты, которые помогают гарантировать, что лекарства производятся, тестируются, хранятся и распространяются в соответствии с высокими стандартами безопасности и качества Канады. Рейтинг несоответствия не обязательно указывает на проблему безопасности продукта. Это означает, что Департамент выявил проблемы с тем, как компания соблюдает надлежащие производственные процессы и процедуры.Министерство здравоохранения Канады регулярно проверяет объекты или оценивает результаты проверок, проводимых надежными международными партнерами по регулированию, чтобы убедиться, что они соответствуют этим стандартам, и ведет базу данных с результатами проверок. Министерство здравоохранения Канады обычно не сообщает заранее об этих рейтингах, но в настоящее время обновляет информацию для канадцев в рамках своих обязательств по информированию о своей деятельности, связанной с примесями нитрозаминов в сартанах.
Министерство здравоохранения Канады продолжает сотрудничать с международными регулирующими органами в проведении инспекций иностранных производителей сартанов и при необходимости будет принимать меры и информировать канадцев.
Что делать
Канадцы с вопросами об отзывах могут обращаться по телефону:
- Apotex Inc. через Stericyle Inc. по бесплатному телефону 1-877-492-4795;
- Pharmascience Inc., позвонив по бесплатному телефону 1-800-340-9735;
- Pro Doc Limitée, позвонив по бесплатному телефону 1-800-361-8559 или по электронной почте [email protected]; или
- Teva Canada по бесплатному телефону 1-800-268-4129 или по электронной почте у клиента[email protected].
Министерство здравоохранения Канады призывает потребителей сообщать в Департамент о любых побочных эффектах или жалобах, связанных с продуктами для здоровья.
Министерство здравоохранения Канады
(613) 957-2983
[email protected]
Общественные запросы
(613) 957-2991
1-866 225-0709
Для получения дополнительной информации
- Дополнительная информация, включая полный список отозванных продуктов, связанных с этой проблемой, а также результаты лабораторных тестов Министерства здравоохранения Канады и метод тестирования.
достигнет 27,2 миллиарда долларов США к 2026 году из-за воздействия COVID-19 — QY Research Report 2020
Согласно QY Research, вероятный сценарий, как ожидается, вырастет на -3,4% в 2020 году, а выручка будет 25,0 млрд долларов США в 2020 году по сравнению с 25,9 млрд долларов США в 2019 году.Объем рынка сартанов достигнет 27,2 млрд долларов США в 2026 году, а среднегодовой темп роста составит 1,2% в период с 2020 по 2026 год.
Сартаны — это антигипертензивные препараты последнего поколения, обладающие хорошим антигипертензивным действием и лекарственной переносимостью, меньшим количеством побочных реакций и защитным действием на органы-мишени, поэтому они широко используются в клинике.В мире более 1 миллиарда пациентов с гипертонией.
Долгосрочное лечение стимулирует спрос на сартаны и промежуточные продукты. Из-за нехватки ключевых промежуточных продуктов, ужесточения защиты окружающей среды и появления примесей Sartan, поставки продуктов Sartan ограничены, а цена продолжает расти.
Сартаны можно разделить на пять категорий: валсартан, ирбесартан, телмисартан, лозартан и другие.
Запросить образец отчета @ https: // www.qyresearch.com/sample-form/form/1546587/global-sartans-market
После вспышки вируса COVID-19 в декабре 2019 года болезнь распространилась почти на 100 стран по всему миру, и Всемирная организация здравоохранения объявила ее чрезвычайной ситуацией в области общественного здравоохранения. Глобальные последствия коронавирусной болезни 2019 года (COVID-19) уже начинают ощущаться и существенно повлияют на рынок Sartans в 2020 году.
COVID-19 может повлиять на мировую экономику тремя основными способами: напрямую влияя на производство и спрос, создавая нарушения цепочки поставок и рынка, а также оказывая финансовое воздействие на фирмы и финансовые рынки.
Вспышка COVID-19 повлияла на многие аспекты, например на отмену рейсов; запреты на поездки и карантин; рестораны закрыты; все внутренние мероприятия ограничены; в более чем сорока странах объявлено чрезвычайное положение; массовое замедление цепочки поставок; волатильность фондового рынка; падение деловой уверенности, растущая паника среди населения и неуверенность в завтрашнем дне.
В этом отчете также анализируется влияние коронавируса COVID-19 на индустрию сартанов.
По типу продукта рынок в основном делится на
- Валсартан
- Телмисартан
- Лосартан
- Ирбесартан
- Азилсартан
- Ольмесартан
По конечным пользователям / приложениям этот отчет охватывает следующие сегменты
- Гипертония
- Сердечно-сосудистые заболевания
- Болезни почек
- Другое
К основным производителям Sartans на этом рынке относятся:
- Pfizer
- Новартис
- Мерк
- Астра Зенека
- Джонсон и Джонсон
- Эли Лилли
- Санофи
- Бристоль-Майерс Сквибб
- Байер
- ГСК
- Teva Pharmaceutical
Купить сейчас полный отчет за 3350 долларов США по адресу https: // www.qyresearch.com/settlement/pre/8acf4c95ba5484
Контакты:
Рахул Сингх — директор по продажам и маркетингу
Контакт: +91 7028 920 828
Эл. Почта: [email protected]
Зарегистрированный офис в США : QY Research, INC.
17890 Castleton, Suite 218,
Промышленный город, Калифорния —
Электронная почта — [email protected]
Интернет — www.qyresearch.com
Обновление информации — Несколько препаратов, содержащих лозартан, добровольно отозваны из-за потенциальной примеси нитрозамина
OTTAWA, 9 марта 2019 г. / CNW / — Министерство здравоохранения Канады сообщает канадцам, что Teva Canada , Apotex Inc. добровольно отозвали несколько партий препаратов, содержащих лозартан., Pharmascience Inc. и Pro Doc Limitée из-за потенциальной примеси нитрозамина, N-нитрозо-N-метил-4-аминомасляной кислоты (NMBA).
NMBA потенциально является канцерогеном для человека, а это означает, что длительное воздействие может увеличить потенциальный риск рака.
Teva Canada добровольно отзывает две партии комбинированных таблеток лозартан / гидрохлоротиазид (HCTZ) после тестирования одной партии, выявившей уровни NMBA, превышающие разумно безопасные, если препарат принимался в течение всей жизни. Apotex Inc ., Pharmascience Inc . И Pro Doc Limitée добровольно отзывают несколько партий продуктов, содержащих лозартан, в качестве меры предосторожности.
Активный фармацевтический ингредиент (API) лозартана во всех отозванных продуктах производится компанией Hetero Labs Ltd. Unit 1 в Индии. Эти отзывы относятся ко всем партиям лекарств, распространяемых в Канаде, которые содержат Лозартан API, произведенные в Hetero Labs Ltd. Unit 1.
Лозартан — препарат, блокирующий рецепторы ангиотензина (БРА), также известный как «сартан».«Сартаны — это класс лекарств, используемых для лечения пациентов с высоким кровяным давлением, чтобы предотвратить сердечные приступы и инсульт. Они также используются у пациентов, перенесших сердечную недостаточность или недавний сердечный приступ. Было несколько отзывов продуктов, содержащих еще один сартан. , валсартан, в Канаде и на международном уровне с июля 2018 года из-за примесей нитрозаминов (дополнительную информацию см. по ссылкам ниже).
Как и в случае с предыдущими отзывами, касающимися примесей нитрозаминов, Министерство здравоохранения Канады сообщает, что нет непосредственного риска для пациентов, принимающих эти лекарства, поскольку потенциальный риск рака связан с долгосрочным воздействием примесей.Пациентам не следует прекращать прием лекарств, если это не рекомендовано их лечащим врачом.
В настоящее время на канадском рынке доступны альтернативные продукты. Министерство здравоохранения Канады продолжает следить за ситуацией с поставками. Министерство здравоохранения Канады рекомендует канадцам посетить сайт drugshortagescanada.ca для получения информации о нехватке и прекращении приема лекарств. Пациенты, у которых есть вопросы или опасения по поводу любого лекарства, которое они принимают, в том числе о том, что делать, если это лекарство недоступно, должны поговорить со своим лечащим врачом.
Канадцы с вопросами об отзывах могут обращаться:
- Apotex Inc. через Stericyle Inc. по бесплатному телефону 1-877-492-4795;
- Pharmascience Inc., позвонив по бесплатному телефону 1-800-340-9735;
- Pro Doc Limitée, позвонив по бесплатному телефону 1-800-361-8559 или по электронной почте [email protected]; или
- Teva Canada по бесплатному телефону 1-800-268-4129 или по электронной почте [email protected].
Министерство здравоохранения Канады призывает потребителей сообщать в Департамент о любых побочных эффектах или жалобах, связанных с продуктами для здоровья.
Затронутые продукты
Отзыв следующих продуктов, содержащих лозартан, производства Hetero Labs Ltd. Unit 1. Министерство здравоохранения Канады ведет полный список препаратов сартана, которые были отозваны из-за примесей нитрозаминов, на своем веб-сайте.
Название продукта / Активный фармацевтический ингредиент (API) | DIN | Прочность | Лот | Срок действия |
АПО-ЛОСАРТАН | 02379058 | 25 мг | NL1453 | 08/2019 |
АПО-ЛОСАРТАН | 02379058 | 25 мг | NL1452 | 08/2019 |
АПО-ЛОСАРТАН | 02353504 | 50 мг | NK1254 | 08/2019 |
АПО-ЛОСАРТАН | 02353504 | 50 мг | NK1253 | 08/2019 |
АПО-ЛОСАРТАН | 02353512 | 100 мг | NL1461 | 08/2019 |
АПО-ЛОСАРТАН | 02353512 | 100 мг | NG2092 | 04/2019 |
АПО-ЛОСАРТАН | 02353512 | 100 мг | NH5932 | 06/2019 |
АПО-ЛОСАРТАН | 02353512 | 100 мг | NH5933 | 06/2019 |
АПО-ЛОСАРТАН | 02353512 | 100 мг | NL1460 | 08/2019 |
АПО-ЛОСАРТАН | 02353512 | 100 мг | NH5934 | 06/2019 |
APO-LOSARTAN / HCTZ | 02371235 | 50/12.5 мг | NL1441 | 08/2019 |
APO-LOSARTAN / HCTZ | 02371235 | 50 / 12,5 мг | NZ8848 | 05/2020 |
APO-LOSARTAN / HCTZ | 02371235 | 50/12.5 мг | NL1445 | 08/2019 |
APO-LOSARTAN / HCTZ | 02371235 | 50 / 12,5 мг | NZ8849 | 05/2020 |
APO-LOSARTAN / HCTZ | 02371235 | 50/12.5 мг | NZ8860 | 05/2020 |
APO-LOSARTAN / HCTZ | 02371243 | 100 / 12,5 мг | NG2087 | 04/2019 |
APO-LOSARTAN / HCTZ | 02371243 | 100/12.5 мг | NL1421 | 10/2019 |
APO-LOSARTAN / HCTZ | 02371243 | 100 / 12,5 мг | NG2086 | 04/2019 |
APO-LOSARTAN / HCTZ | 02371243 | 100/12.5 мг | NL1422 | 10/2019 |
APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NL1429 | 08/2019 |
APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NZ8846 | 05/2020 |
APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NZ8847 | 05/2020 |
APO-LOSARTAN / HCTZ | 02371251 | 100/25 мг | NZ8845 | 05/2020 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394367 | 25 мг | 498292 | 03/2019 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394367 | 25 мг | 605344 | 02/2020 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 498779 | 03/2019 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 600046 | 06/2019 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 603903 | 11/2019 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 498284 | 03/2019 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394375 | 50 мг | 603895 | 11/2019 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394383 | 100 мг | 499008 | 03/2019 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394383 | 100 мг | 605299 | 01/2020 |
ЛОСАРТАН (PRO DOC LIMITEE) | 02394383 | 100 мг | 605297 | 01/2020 |
ПМС-ЛОСАРТАН | 02309750 | 25 мг | 498294 | 03/2019 |
ПМС-ЛОСАРТАН | 02309750 | 25 мг | 605342 | 02/2020 |
ПМС-ЛОСАРТАН | 02309750 | 25 мг | 611944 | 01/2021 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 498285 | 03/2019 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 600047 | 06/2019 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 600091 | 06/2019 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 603894 | 11/2019 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 612025 | 01/2021 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 612031 | 01/2021 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 612679 | 01/2021 |
ПМС-ЛОСАРТАН | 02309769 | 50 мг | 616743 | 08/2021 |
ПМС-ЛОСАРТАН | 02309777 | 100 мг | 498864 | 03/2019 |
ПМС-ЛОСАРТАН | 02309777 | 100 мг | 602668 | 09/2019 |
ПМС-ЛОСАРТАН | 02309777 | 100 мг | 603816 | 09/2019 |
ПМС-ЛОСАРТАН | 02309777 | 100 мг | 605298 | 01/2020 |
ПМС-ЛОСАРТАН | 02309777 | 100 мг | 605300 | 01/2020 |
ПМС-ЛОСАРТАН | 02309777 | 100 мг | 613935 | 03/2021 |
ПМС-ЛОСАРТАН | 02309777 | 100 мг | 613936 | 03/2021 |
TEVA-LOSARTAN / HCTZ | 02358263 | 50/12.5 мг | 35349397A | 09/2019 |
TEVA-LOSARTAN / HCTZ | 02358263 | 50 / 12,5 мг | 35344801A | 09/2020 |
Оценка продолжается
Министерство здравоохранения Канады продолжает сотрудничать с компаниями и международными партнерами в сфере регулирования, включая U.S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) и Европейское агентство по лекарственным средствам, чтобы оценить проблему примесей нитрозамина в некоторых сартановых препаратах, ее основные причины и меры по смягчению. Оценка Министерства здравоохранения Канады на данный момент предполагает, что нитрозамины могут образовываться при наличии определенных химических веществ и условий реакции в процессе производства АФИ лекарственного средства. Они также могут возникать в результате повторного использования материалов, таких как растворители или исходные материалы, загрязненных примесями.
АФИ — это активный ингредиент лекарственного средства, оказывающего действие на организм. АФИ используются при производстве готовых лекарств в виде «лекарственных форм» (таких как пилюли, капсулы или таблетки).
В декабре 2018 года Министерство здравоохранения Канады обратилось ко всем компаниям, продающим сартаны в Канаде, с просьбой протестировать продукты, уже представленные на рынке, и те, которые будут выпущены в Канаде, на содержание N-нитрозодиметиламина (NDMA) и N-нитрозодиэтиламина (NDEA). Министерство здравоохранения Канады также рекомендовало компаниям рассмотреть возможность использования производственных методов, исключающих образование и присутствие всех примесей нитрозаминов.Министерство здравоохранения Канады протестировало более 50 образцов сартановых препаратов и продолжит публиковать результаты любых новых образцов на своем веб-сайте.
Health Canada продолжает возлагать на компании ответственность за безопасность и эффективность лекарств, продаваемых в Канаде, и ожидает, что производители предпримут все необходимые действия для предотвращения образования примесей нитрозаминов. Департамент предпримет дальнейшие шаги по мере необходимости, чтобы подтвердить, что приняты надлежащие и своевременные меры для защиты здоровья и безопасности канадцев.
Производители отозванных API сартана
На основе анализа информации инспекции FDA США Министерство здравоохранения Канады обнаружило, что Hetero Labs Ltd. Unit 1 не соответствует требованиям надлежащей производственной практики (GMP). Рейтинг несоответствия означает, что канадские компании больше не могут импортировать лекарства, содержащие API-интерфейсы, с этого сайта, если они не являются необходимыми с медицинской точки зрения.
Как сообщалось ранее, Министерство здравоохранения Канады также обнаружило, что предприятие Zhejiang Huahai Pharmaceuticals (ZHP) в Китае не соответствует требованиям GMP.На этом предприятии производился валсартан, который, как было обнаружено, содержал примеси нитрозаминов. Все препараты, содержащие валсартан, производимые ZHP, отозваны в Канаде.
GMP — это международно признанные стандарты, которые помогают гарантировать, что лекарства постоянно производятся, тестируются, хранятся и распространяются в соответствии с высокими стандартами безопасности и качества Канады. Рейтинг несоответствия не обязательно указывает на проблему безопасности продукта. Это означает, что Департамент выявил проблемы с тем, как компания соблюдает надлежащие производственные процессы и процедуры.Министерство здравоохранения Канады регулярно проверяет объекты или оценивает результаты проверок, проводимых надежными международными партнерами по регулированию, чтобы убедиться, что они соответствуют этим стандартам, и ведет базу данных с результатами проверок. Министерство здравоохранения Канады обычно не сообщает заранее об этих рейтингах, но в настоящее время обновляет информацию для канадцев в рамках своих обязательств по информированию о своей деятельности, связанной с примесями нитрозаминов в сартанах.
Министерство здравоохранения Канады продолжает сотрудничать с международными регулирующими органами в области инспекций иностранных производителей сартанов и при необходимости будет принимать меры и информировать канадцев.
Ссылки по теме
- Дополнительная информация, включая полный список отозванных продуктов, связанных с этой проблемой, а также результаты лабораторных тестов Министерства здравоохранения Канады и метод тестирования.

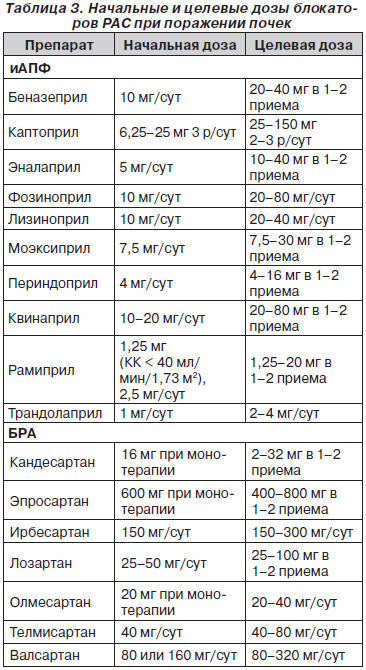
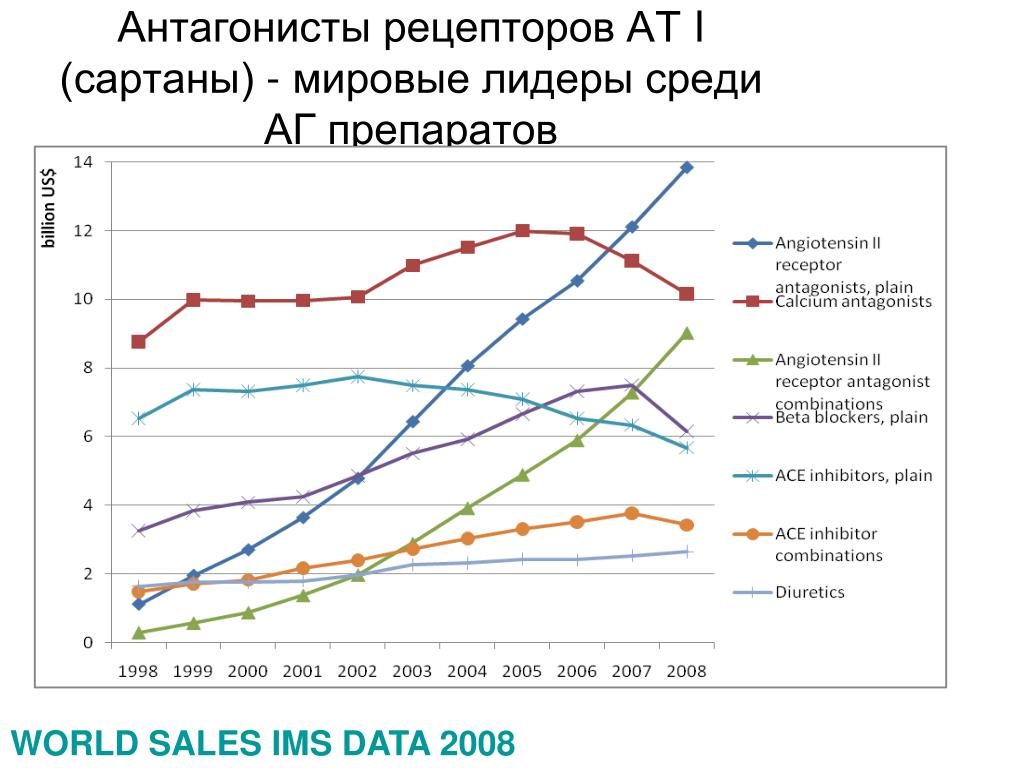
 ncbi.nlm.nih.gov/pubmed/21570954
ncbi.nlm.nih.gov/pubmed/21570954 ncbi.nlm.nih.gov/pubmed/19120129
ncbi.nlm.nih.gov/pubmed/19120129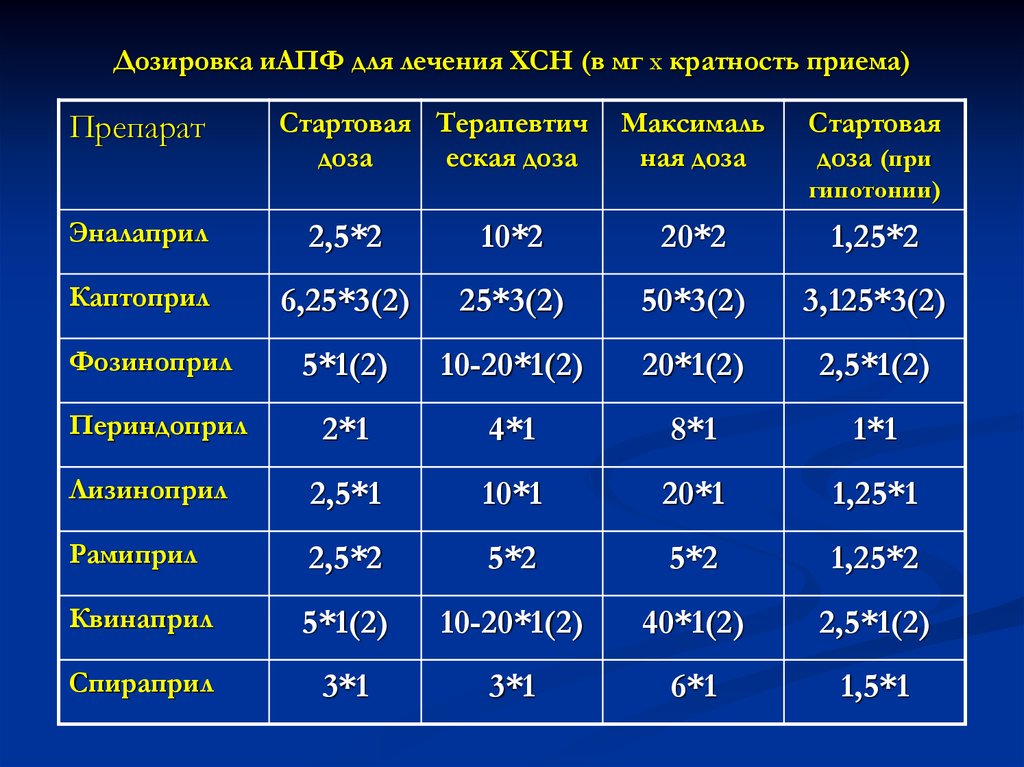 wiley.com/doi/10.1002/acn3.161/abstract
wiley.com/doi/10.1002/acn3.161/abstract ncbi.nlm.nih.gov/pmc/articles/PMC3108350/
ncbi.nlm.nih.gov/pmc/articles/PMC3108350/ ncbi.nlm.nih.gov/pubmed/17004092
ncbi.nlm.nih.gov/pubmed/17004092_575.gif) ncbi.nlm.nih.gov/pubmed/17456026
ncbi.nlm.nih.gov/pubmed/17456026