Болезнь Паркинсона — Википедия
Боле́знь Паркинсо́на (синонимы: идиопатический синдром паркинсонизма, дрожательный паралич) — медленно прогрессирующее хроническое неврологическое заболевание, характерное для лиц старшей возрастной группы[3]. Относится к дегенеративным заболеваниям экстрапирамидной моторной системы. Вызвано прогрессирующим разрушением и гибелью нейронов, вырабатывающих нейромедиатор дофамин[4], — прежде всего в чёрной субстанции, а также и в других отделах центральной нервной системы. Недостаточная выработка дофамина ведёт к активирующему влиянию базальных ганглиев на кору головного мозга. Ведущими симптомами (иначе: основные или кардинальные симптомы) являются:
Современная медицина пока не может излечить заболевание (этиологическая или патогенетическая терапия), однако существующие методы консервативного и оперативного лечения позволяют значительно улучшить качество жизни больных и замедлить прогрессирование болезни[5].
Термин «паркинсонизм» является общим понятием для ряда заболеваний и состояний с вышеназванными ведущими симптомами. Однако наиболее значимой из форм паркинсонизма является болезнь Паркинсона — идиопатическое заболевание (что означает болезнь самостоятельную, не вызванную генетическими нарушениями или другими заболеваниями).
Своим названием болезнь Паркинсона обязана французскому неврологу Жану Шарко. Он предложил назвать её в честь британского врача и автора «Эссе о дрожательном параличе» Джеймса Паркинсона, чей труд не был должным образом оценён при жизни[6].
Первая страница «Эссе о дрожательном параличе» Джеймса Паркинсона Жан Шарко — французский невролог, предложивший называть заболевание болезнью Паркинсона
Рисунок человека с болезнью Паркинсона, сделанный Жаном Шарко
Жан Шарко — французский невролог, предложивший называть заболевание болезнью Паркинсона
Рисунок человека с болезнью Паркинсона, сделанный Жаном ШаркоПроявления болезни Паркинсона были описаны за несколько тысячелетий до опубликования в 1817 году Джеймсом Паркинсоном «Эссе о дрожательном параличе» (англ. An Essay on the Shaking Palsy).
В египетском папирусе XII столетия до н. э. у одного из фараонов отмечены характерные для заболевания симптомы. В Библии описаны люди с тремором[6][7]. В текстах Аюрведы заболевание, проявляющееся тремором, ограничением движений, слюнотечением и другими характерными симптомами, рекомендовано лечить некоторыми видами бобовых. Знаменитый древнеримский врач Гален, по всей видимости, ещё во II столетии н. э. описал болезнь Паркинсона, указав на её симптомы — тремор покоя (дрожь покоящихся частей тела), постуральную неустойчивость и мышечную ригидность[7][8].
После Галена симптомы паркинсонизма вновь были описаны лишь в XVII столетии[7]. Голландский врач и анатом Франциск Сильвий отметил отличие тремора покоя от других видов дрожания, немец Иероним Гобий[en] выделил симптомы характерной для паркинсонизма походки
В 1817 году английский врач Джеймс Паркинсон опубликовал «Эссе о дрожательном параличе»[6]. В нём он описал шестерых больных людей, подробно остановившись на таких характерных симптомах заболевания, как тремор покоя, патологическая походка и постуральная неустойчивость, мышечная ригидность и другие. Также он оценил их динамику при прогрессировании заболевания[6][11]. Работа оставалась незамеченной в течение 40 лет после опубликования[11]. Классические исследования неврологов У. Говерса, С. Вильсона, В. Эрба и Ж. Шарко в 1868—1881 годах позволили выделить болезнь Паркинсона как самостоятельное заболевание. По предложению знаменитого французского невролога Шарко заболевание получило имя британского врача Паркинсона, чей труд не был должным образом оценён при жизни [6].
После определения болезни Паркинсона как самостоятельного заболевания возник вопрос о том, поражение каких структур приводит к его симптомам. Французский невролог Эдуард Бриссо в конце XIX столетия предположил, что за развитие заболевания ответственны субталамическое ядро и ножки мозга (отдел среднего мозга)[6]. В 1912 году Фредерик Леви обнаружил специфические клеточные включения в клетках ствола мозга, характерные для болезни Паркинсона, впоследствии названные тельцами Леви[6]. В 1919 году русский невролог К. Н. Третьяков определил, что основные патологические изменения при заболевании возникают в чёрной субстанции[12]. Предположения К. Н. Третьякова не признавались медицинским сообществом до их подтверждения немецким патологоанатомом Рольфом Хасслером[en] в 1948 году[6][13].
Биохимические изменения, которые лежат в основе заболевания, стали изучать в 1950-х годах. За исследования нейротрансмиттера дофамина, играющего важную роль в развитии заболевания, шведский фармаколог Арвид Карлссон получил Нобелевскую премию по физиологии и медицине
Вместе с исследованиями природы заболевания развивались методы его лечения. Неврологи конца XIX — начала XX столетий отмечали положительный эффект алкалоидов группы атропина белладонны. В 1939 году была предпринята попытка хирургического лечения — деструкция базальных ганглиев. Эти методики были усовершенствованы за последующие 20 лет[8]. До внедрения в клиническую практику леводопы антихолинергические препараты и хирургическое разрушение базальных ядер оставались основными методами лечения болезни Паркинсона[14][16]. В конце 1980-х годов стимуляция глубинных структур мозга электрическими импульсами была признана возможным методом лечения заболевания[17].
Болезнь Паркинсона составляет 70—80 % случаев синдрома паркинсонизма. Она является наиболее частым нейродегенеративным заболеванием после болезни Альцгеймера [18][19]. Заболевание встречается повсеместно. Его частота колеблется от 60 до 140 человек на 100 тысяч населения, число больных значительно увеличивается среди представителей старшей возрастной группы. Удельный вес людей с болезнью Паркинсона в возрастной группе старше 60 лет составляет 1 %[3], а старше 85 лет — от 2,6 %[4] до 4 %[18]. Чаще всего первые симптомы заболевания появляются в 55—60 лет. Однако в ряде случаев болезнь может развиться и в возрасте до 40 (болезнь Паркинсона с ранним началом) или до 20 лет (ювенильная форма заболевания)[4].
Мужчины болеют несколько чаще, чем женщины. Существенных расовых различий в структуре заболеваемости не выявлено[4].
Этиология болезни Паркинсона на вторую половину 2011 года окончательно не выяснена. Этиологическими факторами риска считаются старение, генетическая предрасположенность, воздействие факторов окружающей среды
Около 15 % людей с болезнью Паркинсона имеют семейный анамнез данного заболевания. Однако гены, ответственные за развитие болезни Паркинсона, не идентифицированы[4].
Причинами паркинсоноподобных проявлений также могут быть воздействие факторов окружающей среды (пестициды, гербициды, соли тяжёлых металлов)[22], хроническая цереброваскулярная недостаточность или употребление лекарств, вызывающих экстрапирамидные побочные эффекты [23].
Экологические факторы[править | править код]
Установлено, что после инъекции вещества 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МФТП) развивается паркинсонизм[4]. МФТП проникает через ГЭБ и под действием МАО-B окисляется до 1-метил-4-фенилпиридина (МФП+). МФП+ проникает в митохондрии и ингибирует комплекс I дыхательной цепи. Сходство химического строения МФТП и некоторых пестицидов (например, ротенон, паракват) и гербицидов (например, Агент Оранж) позволило предположить, что МФТП-подобные токсины окружающей среды способствуют развитию болезни Паркинсона[24][25][26]. К факторам риска относят также проживание в сельской местности и близость промышленных предприятий и карьеров[26].
Риск развития болезни Паркинсона у курильщиков в 3 раза ниже, чем у некурильщиков[24]. Предполагают, что это связано с дофамин-стимулирующим эффектом никотина
Окислительная гипотеза[править | править код]
Окислительная гипотеза предполагает, что свободные радикалы, образующиеся при окислительном метаболизме дофамина, играют важную роль в развитии и прогрессировании болезни Паркинсона. Содержание веществ, которые могут служить донором электронов, в чёрном веществе увеличивается, что способствует образованию свободных радикалов[4]. Кроме того, при окислении дофамина под действием МАО образуется пероксид водорода. Если пероксид водорода не связывается с глутатионом, то происходит накопление весьма реактивных гидроксильных радикалов, которые вступают в реакцию с липидами клеточных мембран, вызывая перекисное окисление липидов и гибель клеток.
Патологическая анатомия[править | править код]


При болезни Паркинсона поражаются структуры экстрапирамидной системы — базальные ядра и чёрное вещество, голубое пятно и другие[29]. Наиболее выраженные изменения отмечают в передних отделах чёрной субстанции. Характерные для болезни Паркинсона симптомы возникают при гибели 60—80 % нейронов этого анатомического образования[21][30].
Макроскопические изменения характеризуются депигментацией содержащих меланин областей чёрного вещества и голубого пятна[18][31]. При микроскопическом исследовании поражённых областей выявляют уменьшение числа нервных клеток. В них определяется наличие телец Леви. Также происходит гибель астроцитов (разновидности глиальных клеток) и активация микроглии. Тельца Леви образуются вследствие скопления в цитоплазме белка α-синуклеина
Тельца Леви обнаруживают также и при других нейродегенеративных заболеваниях. В связи с этим они не считаются специфическим маркером болезни Паркинсона. Кроме того, при данном заболевании в чёрной субстанции и голубом пятне обнаружены «бледные тельца» — внутриклеточные гранулярные включения, которые замещают распадающийся меланин[32].
Согласно предложенной Брааком и соавторами классификации, в асимптоматической стадии болезни Паркинсона тельца Леви появляются в нервных клетках обонятельной луковицы, продолговатого мозга и варолиевого моста. С прогрессированием заболевания наличие данных патологических телец отмечается в нейронах чёрной субстанции, среднего мозга, базальных ганглиев и на конечных этапах в клетках коры головного мозга[30].
Патологическая физиология[править | править код]
Тесная взаимосвязь между составляющими экстрапирамидной системы — паллидумом и стриатумом — обеспечивается многочисленными пучками нервных волокон. Благодаря связям между таламусом и стриопаллидарной системой образуются рефлекторные дуги, обеспечивающие выполнение многочисленных стереотипных и автоматизированных движений (например, ходьба, бег, плаванье, езда на велосипеде и др.). Тесная связь стриопаллидарной системы с ядрами гипоталамуса определяет её роль в механизмах эмоциональных реакций[33].
В норме экстрапирамидная система посылает импульсы к периферическим двигательным нейронам. Эти сигналы играют важную роль в обеспечении миостатики путём готовности мышц к произвольным движениям. От деятельности данного отдела центральной нервной системы зависит способность человека принимать оптимальную для намеченного действия позу, достигается необходимое соотношение тонуса мышц-агонистов и мышц-антагонистов, а также плавность и соразмерность произвольных движений во времени и пространстве[33].
Характер клинических проявлений болезни зависит от того, какая часть стриопаллидарной системы поражена — стриатум или паллидум. Если чрезмерно тормозящее влияние стриатума, возникает гипокинезия — бедность движений, амимия. Гипофункция стриатума приводит к возникновению избыточных непроизвольных движений — гиперкинезов[33]. Паллидум оказывает тормозящее воздействие на структуры стриатума. Для болезни Паркинсона характерно снижение тормозящего влияния паллидума на стриатум. Повреждение паллидума приводит к «торможению торможения» периферических двигательных нейронов[34].
Открытие роли нейромедиаторов позволило объяснить функции экстрапирамидной системы, а также причины возникновения клинических проявлений болезни Паркинсона и паркинсонизма. В мозге существует несколько дофаминергических систем. Одна из них начинается в нейронах чёрной субстанции, аксоны которых через ножку мозга, внутреннюю капсулу, бледный шар доходят до полосатого тела (лат. corpus striatum). Терминальные отделы этих аксонов содержат большое количество дофамина и его производных. Дегенерация данного нигростриарного дофаминергического пути является основным причинным фактором развития болезни Паркинсона. Вторая восходящая дофаминергическая система — мезолимбический путь. Он начинается от клеток интерпедункулярного ядра среднего мозга и заканчивается в гипоталамусе и лобных долях головного мозга. Этот путь принимает участие в контроле настроения, поведении и контролирует начало двигательного акта и движений аффективной реакции (движений, которые сопровождают эмоции)[34].
Основу всех форм паркинсонизма составляет резкое уменьшение количества дофамина в чёрной субстанции и полосатом теле[4] и соответственно нарушение функционирования дофаминергических проводящих путей головного мозга.
Для болезни Паркинсона характерны 4 двигательных нарушения: тремор, гипокинезия, мышечная ригидность, постуральная неустойчивость, — а также вегетативные и психические расстройства[20].
Тремор (дрожание) — наиболее очевидный и легко выявляемый симптом[35]. Для паркинсонизма характерен тремор, возникающий в покое, хотя редко возможны и другие типы (постуральный, интенционный)[20]. Его частота 4—6 Гц (движений в секунду). Он обычно начинается в дистальном отделе одной руки, при прогрессировании заболевания распространяясь на противоположную руку и на ноги[4]. Разнонаправленные движения большого и других пальцев внешне напоминают счёт монет или скатывание пилюль (схожесть с ручной техникой создания пилюль в фармацевтике)[36][37]. Иногда также отмечается дрожание головы по типу «да-да» или «нет-нет», дрожание век, языка, нижней челюсти. В редких случаях оно охватывает всё тело. Тремор усиливается при волнении и стихает во время сна и произвольных движений[38]. В отличие от мозжечкового тремора, который появляется при движении и отсутствует в покое, при болезни Паркинсона типично его наличие в покое и уменьшение или исчезновение при движениях[39].
Почерк при болезни Паркинсона. На рисунке (масштаб не соблюдён) видны рваные движения там, где предполагаются плавные линииГипокинезия — снижение спонтанной двигательной активности. Больной может застывать, часами сохраняя неподвижность. Характерна общая скованность. Активные движения возникают после некоторого промедления, темп их замедлен — брадикинезия[39]. Больной ходит мелкими шагами, ступни при этом располагаются параллельно друг другу — кукольная походка[38]. Лицо маскообразное (амимия), взгляд застывший, мигания редкие. Улыбка, гримаса плача возникают с запозданием и так же медленно исчезают[39].
«Поза манекена» характерная для болезни ПаркинсонаРечь лишена выразительности, монотонна и имеет тенденцию к затуханию. В результате характерного для болезни Паркинсона уменьшения амплитуды движений почерк становится мелким — микрография[37][38].
Одним из проявлений олигокинезии (уменьшение количества движений) является отсутствие физиологических синкинезий (содружественных движений). При ходьбе руки не совершают обычных размашистых движений, они остаются прижатыми к туловищу (ахейрокинез). При взгляде вверх не отмечается наморщивания лба. Сжатие пальцев в кулак не сопровождается разгибанием кисти. Больной не может выполнять несколько целенаправленных движений одновременно. Все действия напоминают автоматические[37][38][39].
Мышечная ригидность — равномерное повышение тонуса мышц по пластическому типу. Конечности при их сгибании и разгибании застывают в приданном им положении. Такая форма повышения мышечного тонуса называется «пластической восковой гибкостью». Преобладание ригидности в определённых группах мышц приводит к формированию характерной позы просителя[37] (также называют «поза манекена»[38][39]): больной сутулится, голова наклонена вперёд, полусогнутые в локтевых суставах руки прижаты к телу, ноги также слегка согнуты в тазобедренных и коленных суставах. При пассивном сгибании-разгибании предплечья, головы, круговых движениях в лучезапястном суставе можно ощутить своеобразную прерывистость, ступенчатость напряжения мышц — «симптом зубчатого колеса»[37][39].
Изменения мышечного тонуса ведут к нарушению тенденции конечности к возвращению в исходную позицию после совершённого движения. Например, после резкого пассивного тыльного сгибания стопы она некоторое время сохраняет приданную ей позицию — феномен Вестфаля[38].
Постуральная неустойчивость развивается на поздних стадиях заболевания[4]. У больного отмечаются затрудения преодоления как инерции покоя, так и инерции движения. Больному сложно начать движение, а начав его, трудно остановиться. Возникают явления пропульсии (лат. propulsio — проталкивание вперёд), латеропульсии и ретропульсии. Они выражаются в том, что, начав движение вперёд, в сторону или назад, туловище обычно как бы опережает ноги, в результате чего нарушается положение центра тяжести. Человек теряет устойчивость и падает[38]. Иногда у больных определяют «парадоксальные кинезии», когда вследствие эмоциональных переживаний, после сна либо вследствие других факторов человек начинает свободно передвигаться, пропадают характерные для заболевания симптомы. Через несколько часов симптоматика возвращается[37].
Вегетативные и психические расстройства. Кроме нарушений двигательной сферы, при болезни Паркинсона отмечаются вегетативные расстройства, а также нарушения обмена веществ. Следствием может быть либо истощение (кахексия), либо ожирение. Секреторные расстройства проявляются сальностью кожных покровов, особенно лица, повышенным слюноотделением, избыточной потливостью[37][38].
Психические расстройства при болезни Паркинсона могут быть обусловлены как самим заболеванием, так и антипаркинсоническими препаратами. Начальные признаки психоза (страх, растерянность, бессонница, галлюцинаторно-параноидное состояние с нарушением ориентировки) отмечают у 20 % амбулаторных и двух третей больных с тяжёлой формой паркинсонизма. Слабоумие выражено слабее, чем при сенильной деменции. У 47 % наблюдают депрессии, у 40 % — расстройства сна и патологическую утомляемость[40]. Больные безынициативны, вялы, а также назойливы, склонны к повторению одних и тех же вопросов[37][38].
Различают несколько клинических форм заболевания — ригидно-брадикинетическую, дрожательно-ригидную и дрожательную[41]:
- Ригидно-брадикинетическая форма характеризуется повышением тонуса мышц по пластическому типу, прогрессирующим замедлением активных движений вплоть до обездвиженности. Появляются мышечные контрактуры. Характерна «поза манекена» («поза просителя»).
- Дрожательно-ригидная форма характеризуется тремором конечностей, преимущественно их дистальных отделов, к которому присоединяется скованность произвольных движений.
- Для дрожательной формы характерно наличие постоянного или почти постоянного средне- и крупноамплитудного тремора конечностей, языка, головы, нижней челюсти. Тонус мышц нормальный или несколько повышен. Темп произвольных движений сохранён.
Диагностика и дифференциальный диагноз. Другие виды паркинсонизма[править | править код]
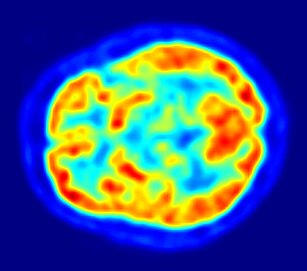 Томография мозга мужчины (56 лет) с диагнозом Паркинсона
Томография мозга мужчины (56 лет) с диагнозом ПаркинсонаДиагностика болезни Паркинсона в большинстве случаев не вызывает затруднений — достаточно наличия у пациента гипокинезии и одного из симптомов: тремора покоя, ригидности, постуральных нарушений в сочетании с положительным эффектом от приёма леводопы[35]. На начальных этапах заболевания, когда проявления заболевания не выражены либо выражены слабо, правильной диагностике может способствовать выявление постуральных рефлексов (рефлексов положения). К ним относится описанный выше феномен Вестфаля, а также феномен Фуа—Тевенара (либо феномен голени). Данные рефлексы возникают вследствие повышения пластического тонуса мышц. Феномен голени проявляется тем, что максимально согнутая в коленном суставе нога больного, который лежит на животе, опускается медленно и обычно разгибается не полностью[38].
Дифференциальный диагноз болезни Паркинсона с другими патологиями проходит в два этапа. Следует исключить состояния и процессы, при которых имеются схожие с паркинсонизмом симптомы. При наличии у больного паркинсонизма необходимо учитывать, что данный синдром характерен для ряда заболеваний.
Патогномоничные для паркинсонизма симптомы наблюдаются при следующих расстройствах[4]:
Паркинсонизм также может быть вызван целым рядом заболеваний. В большинстве случаев (~80 %) он вызван поражением нигростриарной системы вследствие болезни Паркинсона. При поражениях соответствующих отделов центральной нервной системы другой этиологии будут возникать токсический, лекарственный, постэнцефалитический, сосудистый, посттравматический и другие паркинсонизмы[4].
При многих заболеваниях развивается синдром паркинсонизма в сочетании с симптомами поражения других отделов центральной нервной системы. Для обозначения данной группы заболеваний используют термин «паркинсон-плюс»[4].
Классификация паркинсонизма и частота встречаемости его отдельных форм*[19]| Тип | Форма | Частота, % |
|---|---|---|
| Первичный (идиопатический) паркинсонизм | Болезнь Паркинсона | 80,2 |
| * | ||
| Вторичный паркинсонизм | Постэнцефалитический | 0,5 |
| Лекарственный | 3,9 | |
| Сосудистый | 2,1 | |
| Токсический | * | |
| Травматический | * | |
| Паркинсонизм, связанный с тиреоидными нарушениями, гипотиреоидизмом, гепатоцеребральной дегенерацией, опухолью мозга, гидроцефалией, сирингомезенцефалией | * | |
| Паркинсонический синдром при мультисистемной дегенерации — «паркинсонизм-плюс» | Прогрессирующий супрануклеарный паралич (синдром Стила—Ричардсона) | 7,4 |
| Синдром Шая—Драйжера | 1,7 | |
| Стриато-нигральная дегенерация | 0,4 | |
| Комплекс паркинсонизм—деменция—боковой амиотрофический склероз | 0,2 | |
| Кортико-базальная дегенерация | 0,5 | |
| Болезнь диффузных телец Леви | 1,2 | |
| Болезнь Галлервордена—Шварца | 0,3 | |
| Оливо-понто-церебральная дегенерация | * |
* Формы паркинсонизма, частота встречаемости которых не указана, диагностируют редко, и в сумме они составляют 2,2 %.
В соответствии с последними соглашениями Европейской ассоциации болезни Паркинсона[42] синдром паркинсонизма подразделяется на четыре группы:
- идиопатический паркинсонизм
- генетические формы паркинсонизма, семейный синдром паркинсонизма — наследственная форма, обозначается локализацией гена (например, PARK1)
- паркинсонизм в рамках других нейродегенеративных заболеваний (атипичные формы паркинсонизма, иногда называемые благодаря дополнительным симптомам «синдром паркинсонизм плюс»)
- симптоматические синдромы Паркинсона — например, как следствие некоторых медикаментов, амфетаминов, травм, опухолей, действия токсических веществ, эндокринно-метаболических нарушений, воспалительно-инфекционных заболеваний
Идиопатический и атипичный паркинсонизм могут в качестве проявлений нейродегенеративных заболеваний классифицироваться как синуклеинопатии (англ.)русск. (идиопатический паркинсонизм, мультисистемная атрофия, деменция с тельцами леви) или таупатии (прогрессирующий супрануклеарный парез взора, кортико-базальная деменция).
В 1992 году британский врач Хьюз предложил критерии диагностики болезни Паркинсона, позволяющие установить диагноз с точностью до 93 % (согласно данным аутопсий)[43]:
- Наличие гипокинезии и как минимум одного из следующих симптомов: ригидность, тремор покоя 4—6 Гц, постуральные нарушения.
- Асимметричный дебют заболевания (стадия гемипаркинсонизма).
- Прогрессирующее течение.
- Отсутствие в анамнезе возможных этиологических факторов вторичного паркинсонизма (приём нейролептиков, достоверно перенесённый энцефалит, острые нарушения мозгового кровообращения, повторные или тяжёлые черепно-мозговые травмы).
- Отсутствие следующих симптомов:
- a) на всех стадиях заболевания
- отчётливой мозжечковой и/или пирамидной симптоматики
- надъядерного паралича взора
- окулогирных кризов
- b) на ранних стадиях заболевания
- грубых постуральных расстройств
- грубой прогрессирующей вегетативной недостаточности
- грубой деменции
Эти критерии должны соблюдаться лишь при отборе больных для научных исследований. Для предварительного диагноза достаточно выполнение лишь первых двух пунктов[35].
Стадии паркинсонизма по Хён и Яру (Hoehn, Yahr, 1967)[править | править код]
Наиболее часто применяемой в медицине является классификация стадий паркинсонизма по Хён и Яру[44][45]. Впервые она была опубликована в 1967 году в журнале Neurology Маргарет Хён (англ. Hoehn) и Мелвином Яром (англ. Yahr). Изначально она описывала 5 стадий прогрессирования болезни Паркинсона (1 — 5)[46]. Впоследствии шкалу модифицировали, дополнив её стадиями 0, 1,5 и 2,5[47].
- Стадия 0 — нет признаков заболевания.
- Стадия 1 — симптомы проявляются на одной из конечностей.
- Стадия 1,5 — симптоматика проявляется на одной из конечностей и туловище.
- Стадия 2 — двусторонние проявления без постуральной неустойчивости.
- Стадия 2,5 — двусторонние проявления с постуральной неустойчивостью. Больной способен преодолевать инерцию движения, вызванную толчком.
- Стадия 3 — двусторонние проявления. Постуральная неустойчивость. Больной способен к самообслуживанию.
- Стадия 4 — обездвиженность, потребность в посторонней помощи. При этом больной способен ходить и/или стоять без поддержки.
- Стадия 5 — больной прикован к креслу или кровати. Тяжёлая инвалидизация.
 Молекула дофамина, недостаток которого вызывает болезнь Паркинсона
Молекула дофамина, недостаток которого вызывает болезнь ПаркинсонаКонсервативное лечение[править | править код]
В настоящее время болезнь Паркинсона является неизлечимой, все существующие методы лечения направлены на облегчение её симптомов (симптоматическое лечение). Основные препараты, устраняющие двигательные нарушения: леводопа (чаще в комбинации с периферическими ингибиторами ДОФА-декарбоксилазы или реже с ингибиторами КОМТ), агонисты дофаминовых рецепторов[en] и ингибиторы МАО-Б[5].
Дофаминергические препараты[править | править код]
Диоксифенилаланин (сокращённо допа, или дофа) — биогенное вещество, которое образуется в организме из тирозина и является предшественником дофамина, в свою очередь являющегося предшественником норадреналина. В связи с тем, что при болезни Паркинсона содержание дофамина в головном мозге значительно снижено, для лечения заболевания целесообразно применение веществ, повышающих его содержание в ЦНС. Сам дофамин не может быть использован для этой цели, так как он плохо проникает через гемато-энцефалический барьер[48].
Леводопа[править | править код]
В качестве лекарственного препарата широко применяют синтетический левовращающий изомер диоксифенилаланина (сокращённо L-дофа), который значительно активнее правовращающего. Леводопа хорошо всасывается при приёме внутрь. Бо́льшая часть препарата попадает в печень и превращается в дофамин, который не проникает через гемато-энцефалический барьер. Для уменьшения декарбоксилирования препарат рекомендуют применять с ингибиторами дофа-декарбоксилазы (бенсеразидом,
Паркинсонизм — Википедия
Материал из Википедии — свободной энциклопедии
Паркинсони́зм — неврологический синдром, который характеризуется рядом симптомов: тремором, мышечной ригидностью (устойчивое повышение мышечного тонуса, равномерное сопротивление мышц во всех фазах пассивного движения, одинаково выраженное в сгибателях и разгибателях), постуральной неустойчивостью (неспособность удерживать равновесие, трудности ходьбы, падения) и брадикинезией (замедленный темп движений, трудность начальных движений, трудность поворотов)[1]. Ядро клинической картины паркинсонизма представляет собой акинетико-ригидный синдром[2].
Встречается при целом ряде заболеваний. Наиболее частой причиной является болезнь Паркинсона.
- Первичный (идиопатический) паркинсонизм (болезнь Паркинсона) встречается в большинстве случаев.
- Вторичный, симптоматический паркинсонизм:
Лекарственный паркинсонизм является одним из самых частых форм вторичного паркинсонизма и составляет от 4 до 10 % всех случаев возникновения паркинсонических симптомов. Чаще всего он связан с применением нейролептиков, его распространённость наиболее высока среди пациентов психиатрических клиник и амбулаторных психиатрических учреждений[3]. Именно лекарственный паркинсонизм необходимо в первую очередь исключить врачу при обследовании пациента с недавно развившимися гипокинезией, ригидностью или тремором[4]. Главным фактором риска развития лекарственного паркинсонизма является пожилой возраст[5][6][7].
Нейролептические экстрапирамидные расстройства, в том числе нейролептический паркинсонизм, появились после 1952 года, когда во врачебную практику были внедрены нейролептики (антипсихотики). Впервые лекарственный паркинсонизм был описан в 1954 году — он был выявлен у больного, которого лечили нейролептиками фенотиазинового ряда и резерпином[8].
Приблизительно в 50 % случаев[9] лекарственный паркинсонизм возникает из-за приёма лекарственных средств, не относящихся к антипсихотикам. Это могут быть[3]:
Исследователями отмечались отдельные случаи паркинсонизма, связанные с приёмом α-интерферона, амоксапина, амлодипина, амиодарона, амфотерицина В, диазепама, дилтиазема, дисульфирама, дифенина, индометацина, каптоприла, клопамида, ловастатина, тразодона, фенелзина, циклоспорина, циметидина, цитозин-арабинозида, высоких доз морфина, а также после введения контрастирующих средств. Механизм развития экстрапирамидных нарушений в этих случаях остаётся неизвестным. Возможно усиление паркинсонизма при приёме холиномиметиков, в том числе пиридостигмина, донепезила[4].
Сообщалось и о случаях возникновения паркинсонизма при приёме трициклических антидепрессантов и препаратов лития, но анализ этих публикаций показывает, что речь в них идёт не столько о паркинсонизме как таковом, сколько о треморе постурального или постурально-кинетического характера, иногда довольно грубом и сопровождающемся феноменом «зубчатого колеса»[4].
Общим признаком заболеваний с атипичным паркинсонизмом является быстрое течение, неполный или кратковременный эффект от лечения леводопой, клинические признаки, нетипичные для болезни Паркинсона — по крайней мере, в её ранней стадии: например, постуральные нарушения, автономные дисфунции, отчётливое аксональное доминирование гипокинетически-ригидного синдрома (не на конечностях, а на теле), пирамидные знаки, миоклонии, мозжечковые симптомы, нарушения окуломоторики и когнитивных функциий — прежде всего лобных. Эти заболевания возникают, как правило, спорадически. К наследственным формам относятся некоторые формы спиноцеребеллярных атаксий и фронтотемпоральных деменций, болезнь Вильсона-Коновалова, а также ювенильная форма болезни Хантингтона. Диагностика атипичных форм паркинсонизма важна для планирования, так как здесь возникают особые проблемы, требующие специального лечения. Кроме того, знание атипичных форм паркинсонизма поможет избежать неэффективного или даже рискованного лечения. Например, пациенты с прогрессирующим супрануклеарным парезом взора или мультисистемной атрофией не реагируют на глубокую стимуляцию мозга.
- ↑ Aminoff M. J., Greenberg D. A., Simon R. P. Clinical Neurology (неопр.). — 6th. — Lange: McGraw-Hill Medical, 2005. — С. 241—245. — ISBN 0071423605.
- ↑ 24.2.2. Болезнь Паркинсона // Гусев Е.И., Коновалов А.Н., Бурд Г.С. Неврология и нейрохирургия: учебник. — 2004.
- ↑ 1 2 Луцкий И. С., Евтушенко С. К., Симонян В. А. Симпозиум «Болезнь Паркинсона (клиника, диагностика, принципы терапии)» // Последипломное образование. — 2011. — № 5 (43).
- ↑ 1 2 3 4 Левин О. С., Шиндряева Н. Н., Аникина М. А. Лекарственный паркинсонизм // Журнал неврологии и психиатрии им. С. С. Корсакова. — 2012. — № 8. — С. 69—74.
- ↑ Avorn J et al. Neuroleptic drug exposure and treatment of parkinsonism in the elderly: a case-control study (англ.) // The American Journal of Medicine (англ.)русск. : journal. — 1995. — July (vol. 99, no. 1). — P. 48—54. — PMID 7598142.
- ↑ Susatia F., Fernandez HH. Drug induced parkinsonism (неопр.) // Curr Treat Options Neurol. — 2009. — Т. 11. — С. 162—169. — PMID 19364450.
- ↑ B Thanvi, S Treadwell. Drug induced parkinsonism: a common cause of parkinsonism in older people (англ.) // Postgraduate Medical Journal (англ.)русск. : journal. — 2009. — Vol. 85. — P. 322—326. — doi:10.1136/pgmj.2008.073312.
- ↑ Достоверность гипотезы Иди и Сазерленда. Нейролептический синдром — лекарственный паркинсонизм
- ↑ Bondon-Guitton E et al. Drug-induced parkinsonism: A review of 17 years’ experience in a regional pharmacovigilance center in France (англ.) // Movement Disorders : journal. — 2011. — October (vol. 26, no. 12). — P. 2226—2231.
- ↑ Manfred Hauben, Lester Reich. Valproate-induced parkinsonism: Use of a newer pharmacovigilance tool to investigate the reporting of an unanticipated adverse event with an “old” drug (англ.) // Movement Disorders : journal. — 2005. — March (vol. 20, no. 3). — P. 387.
- ↑ C. Armon et al. «Reversible parkinsonism and cognitive impairment with chronic valproate use» Neurology 1996; 47: 626—635
- Neurologie compact für Klinik und Praxis, herausgegeben von Andreas Hufschmidt 6. Auflage 2013
- Thomas Brandt «Therapie und Verlauf neurologischer Erkrankungen 6. Auflage 2013 Kapitel «Atypische Parkinson-Syndrome» von A. Münchau und G.K. Wenning
- Левин О.С. Как лечить паркинсонизм не при болезни Паркинсона? // Трудный пациент. — 2008. — № 5—6. Архивировано 7 февраля 2013 года.
- Экстрапирамидные расстройства: Руководство по диагностике и лечению / Под ред. В.Н. Штока, И.А. Ивановой-Смоленской, О.С. Левина. — Москва: МЕДпресс-информ, 2002. — 608 с. — ISBN 5-901712-29-3.
что это такое, первые признаки и симптомы, лечение
Болезнь Паркинсона – отражение нейродегенеративных процессов с прогрессирующим течением, которые сопровождаются характерными симптомами лишь на поздних этапах, что затрудняет раннюю диагностику и лечение. Распространенность патологии составляет 1% населения в возрасте старше 55 лет. С увеличением возраста цифры повышаются. В популяции старше 65 лет заболевание встречается с частотой 5% случаев. Проявления паркинсонизма включают тремор покоя, брадикинезию (замедление согласованных движений) на фоне ригидности мышц, постуральную нестабильность (неспособность удерживать равновесие).


Характеристика заболевания
Простыми словами болезнь Паркинсона – это такая патология, которая проявляется характерными изменениями мозгового вещества, что на поздних стадиях отчетливо наблюдается в ходе нейровизуализации. Повреждение нервной ткани протекает в несколько стадий. Патоморфологическое исследование мозгового вещества свидетельствует о вовлечении в патологический процесс многих структур мозга.
Болезнь Паркинсона начинается с поражения дорсального (заднего) ядра (скопление многоугольных и веретенообразных клеток серого вещества) блуждающего нерва, откуда отходят нервные волокна в ганглии вегетативной системы, затем повреждения затрагивают такую структуру, как обонятельная луковица (часть обонятельного мозга).
Следующие отделы, которые подвергаются патологическим изменениям – голубое пятно (часть ретикулярной формации, ядро, расположенное на уровне моста, отвечающее за физиологическую реакцию в ответ на напряжение и чувство тревоги) и другие отделы ретикулярной формации (образование, расположенное вдоль оси ствола, контролирующее функции спинного мозга и коры полушарий головного мозга).
Следующий этап течения заболевания Паркинсона наступает спустя 2-4 года, характеризуется поражением нервного вещества черной субстанции – отдел экстрапирамидной системы, который регулирует мышечный тонус, моторные и статокинетические функции. Черное вещество участвует в вегетативной деятельности, управляя работой сердечной мышцы, тонусом сосудистой стенки, системой дыхания.
При развитии болезни Паркинсона повреждаются нейроны полосатого тела (отдел конечного мозга, отвечающий за уменьшение мышечного тонуса, регуляцию работы внутренних органов, формирование поведенческих реакций). На фоне поражения вещества полосатого тела происходят патологические изменения:
- Гипертонус (стойкое повышение тонуса) скелетных мышц.
- Нарушение способности выполнять сложные движения.
- Сокращение выработки дофамина – нейромедиатора, который отвечает за когнитивные способности, двигательную активность, мотивацию и эмоциональные реакции.
Болезнь Паркинсона опасна тем, что выраженная моторная дисфункция появляется, когда уровень стриарного (взаимодействующего с полосатым телом) дофамина понижается на 60-80%, а число нигростриарных нейронов уменьшается почти вдвое, чем обусловлено нарушение передачи импульсов по нигростриарному пути. При болезни Паркинсона важна ранняя (до момента развития моторной дисфункции) диагностика – это поможет эффективно лечить болезнь, что улучшает прогноз.
Описание клинических случаев болезни Паркинсона указывает на частую ошибочную постановку диагноза, когда такие симптомы, как гипокинезия и мышечная ригидность списываются на последствия перенесенного острого нарушения мозгового кровотока, что приводит к назначению некорректной терапии. Лечащий врач часто связывает синдром Паркинсона у таких пациентов с сосудистыми патологиями, это ассоциируется с неоправданной, длительной терапией ноотропными и вазоактивными препаратами, что не приносит желаемого лечебного эффекта.
При постановке дифференциального диагноза между болезнью Паркинсона и паркинсонизмом сосудистой этиологии учитывают характер течения. Паркинсонизм на фоне патологии сосудов, питающих мозговую ткань, протекает остро, значительно прогрессируя в течение первых 6 месяцев после перенесенного эпизода острого нарушения мозгового кровотока (инсульт).


Течение сосудистого паркинсонизма прерывистое с чередующимися периодами декомпенсации (мозговая дисфункция вследствие исчерпания физиологических возможностей и приспособительных механизмов), стабилизации, внезапного регресса симптоматики. В ходе инструментальной диагностики (нейровизуализация) выявляются многочисленные очаги повреждения мозговой ткани ишемической и геморрагической природы.
Ишемические и геморрагические очаги выявляются преимущественно в лобной области, таламусе, переднем (бледный шар) и среднем мозге. Одновременно обнаруживается лейкоареоз (диффузное поражение белого вещества) перивентрикулярной (в области желудочковой системы) и субкортикальной (подкорковая зона) локализации.
Для синдрома паркинсонизма сосудистой этиологии характерны признаки: преимущественное нарушение функций нижних конечностей, симметричная симптоматика, патологическое изменение походки и утрата способности удерживать равновесие на начальных стадиях развития патологии. В неврологии ошибочно ставят диагноз болезнь Паркинсона на основании такого признака, как тремор, не учитывая отсутствие всех других симптомов.
Дрожание кистей и пальцев рук, головы может возникать как симптом эссенциального тремора – наследственная форма доброкачественного дрожания невыясненной причины. Эссенциальный тремор – наследственное заболевание семейного типа. Для патологии характерен тремор действия, когда дрожание появляется (усиливается) при попытке совершить целенаправленное движение или удержать статическую позу.
Формы и стадии патологии
Первичная форма болезни Паркинсона встречается с частотой около 80% случаев. В остальных 20% случаев синдром паркинсонизма спровоцирован первичным заболеванием. Вторичные формы паркинсонизма ассоциируются с сосудистыми патологиями, черепно-мозговыми травмами, приемом некоторых лекарств (антипсихотики), интоксикациями, последствиями энцефалита. Классификация болезни Паркинсона предполагает выделение стадий течения:
- Стадия 0. Признаки патологии не наблюдаются.
- Стадия 1. Симптомы болезни Паркинсона как постоянные, так и кратковременные, проявляются в зоне одной конечности. Позже нарушения затрагивают туловище.
- Стадия 2. Двигательные нарушения выявляются в обеих половинах тела. При этом сохраняется способность удерживать равновесие. Позже развивается постуральная нестабильность.
- Стадия 3. Усугубление симптоматики с сохранением способности больного к самообслуживанию.
- Стадия 4. Частичная или полная утрата двигательной активности, потребность в постоянном медицинском наблюдении и уходе. Сохраняется способность стоять или ходить.
- Стадия 5. Тяжелая степень инвалидности (полная обездвиженность).

С учетом клинической картины (преобладающий симптом) различают дрожательную (преобладает тремор), акинетико-ригидную (преобладают двигательные нарушения) и смешанную формы. Распознать развитие болезни Паркинсона на ранней стадии практически невозможно, потому что выраженная симптоматика появляется после разрушения 40% нигростриарных нейронов, которые передают импульсы по нигростриарному пути от структуры, известной как черная субстанция, до полосатого тела.
В силу того, что болезнь Паркинсона прогрессирует, рано или поздно развивается стадия декомпенсации, которая проявляется, как быстро нарастающая симптоматика (усугубление симптомов на протяжении более суток) на фоне привычного приема антипаркинсонических препаратов. Осложнения в стадии декомпенсации ассоциируются с резким ухудшением двигательной активности. Самостоятельная отмена лекарств может спровоцировать декомпенсацию или акинетический криз. Признаки акинетического криза:
- Дисфагия (нарушение функции глотания).
- Дизартрия (расстройство речи на фоне нарушения иннервации речевого аппарата).
- Акинезия (частичная или полная утрата способности совершать произвольные движения).
- Дисфония (уменьшение силы, изменение тембра голоса).
- Помрачение, спутанность сознания, бред.
При акинетическом кризе наблюдаются признаки сбоев в работе вегетативной системы, в том числе тахикардия (нарушение сердечного ритма), артериальная гипотония (низкие значения артериального давления), гипергидроз (избыточное потоотделение), гипертермия (накопление тепла, перегревание тела), энурез (недержание мочи).
На этой стадии болезни Паркинсона неэффективна терапия антипиретиками (жаропонижающие лекарства), что в сочетании с нарушением функции глотания приводит к обезвоживанию организма, изменению реологических характеристик крови, расстройству микроциркуляции в системе кровоснабжения мозга и других органов.
Отсутствие в этот период корректной терапии приводит к летальному исходу, который происходит по причине развития пневмонии (воспаление легких), тромбоэмболии (закупорка сосуда тромбом), нарушения водно-электролитного баланса.
Причины появления
Болезнь Паркинсона относится к нейродегенеративным заболеваниям, причины возникновения коррелируют с гибелью нервных клеток, повреждением структуры мозгового вещества, атрофией нервной ткани. Современные врачи затрудняются точно ответить на вопрос, откуда берется заболевание. В 95% случаев патология развивается спорадически (без очевидных причин), в 5% случаев – носит семейный характер (раньше выявлены случаи заболевания среди родственников).
Определить от чего появляется болезнь Паркинсона невозможно, однако выделяют провоцирующие факторы, такие как генетическая предрасположенность, физиологическое старение, неблагоприятное влияние внешней среды (интоксикации пестицидами, гербицидами). Спровоцировать синдром паркинсонизма может систематическое употребление героина или его аналога МФТП (наркотическая зависимость).


Симптомы и признаки
Первые признаки болезни Паркинсона чаще неспецифические, что затрудняет постановку диагноза на ранней стадии, несмотря на наличие неврологических симптомов:
- Повышенная утомляемость.
- Общая и мышечная слабость.
- Нарушения двигательной координации легкой степени.
- Расстройство мелкой моторики, к примеру, трудности при выведении письменных знаков.
Нередко выраженным двигательным расстройствам предшествуют болезненные ощущения в области костных структур позвоночника и мышц шеи, которые ошибочно истолковываются, как признаки остеохондроза шейного и поясничного отделов, остеоартроза (разрушение внутрисуставного хряща), периартрита (болезненная скованность мышц, окружающих сустав) плечевой и лопаточной зоны.
Систематические боли безрезультатно лечатся разными способами, которые включают физиотерапевтические процедуры, классический и точечный массаж, мануальную терапию. Длительность фазы, предшествующей появлению двигательных нарушений, составляет в среднем 2-4 года.
Симптомы и ранние признаки болезни Паркинсона у молодых людей включают запоры, гипосмию (ухудшение обоняния), расстройство ночного сна с эпизодами сильной сонливости в дневное время. Начальные признаки и симптомы болезни Паркинсона, которые выявляются преимущественно у женщин: депрессия, тревожное расстройство. Симптомы и признаки болезни Паркинсона у мужчин и женщин делятся на группы:
- Основные. Гипокинезия (ограничение объема и темпа движений), тремор (дрожание конечностей), возникающий спонтанно без совершения произвольных движений, ригидность, неподатливость, твердость мышц, неспособность пребывать в состоянии равновесия.
- Дополнительные. Повышенная тревожность, брадифрения (заторможенность мыслительной деятельности), деменция, депрессивное состояние, расстройство сна.
- Черепные. Дизартрия (нарушение артикуляции), дисфагия (расстройство функции глотания), блефароспазм (непроизвольное стойкое сокращение круговой глазной мышцы), гипосмия (ухудшение обоняния, больной практически не различает запахи), сиалорея (усиленная продукция слюны). У больного слабо выражена мимика, лицо напоминает застывшую маску.
- Мышечно-скелетные. Нейропатия (поражение периферических нервов, проявляющееся расстройством чувствительности – онемением, покалыванием) компрессионного типа, деформация костных структур кистей рук и стоп ног, кифосколиоз (искривление позвоночника), отеки на периферических участках тела (руки, ноги). Нередко наблюдается дистония (судороги, спазматическое сокращение мышц).
- Вегетативные. Ортостатическая гипотензия (резкое понижение значений артериального давления при переходе из сидячей или лежачей позиции в положение стоя), гипергидроз (избыточное потоотделение), запоры и другие диспепсические явления, расстройства сексуальной сферы, нарушение мочеиспускания.
- Сенсорные. Крампи (внезапные сокращения группы мышц, сопровождающиеся болью), боли, парестезии (расстройство чувствительности), комплекс симптомов «беспокойных ног», характеризующийся появлением в положении покоя неприятных ощущений в области чаще нижних, редко верхних конечностей, когда человек постоянно совершает движения, чтобы облегчить состояние.
Болезнь Паркинсона может проявляться себореей – усиленной продукцией секрета сальных желез, вследствие чего появляется болезненный зуд в области кожных покровов. Себорея возникает как результат нарушения нейроэндокринной регуляции деятельности сальных желез.


Диагностика
С высокой вероятностью прижизненно выявить болезнь Паркинсона можно, опираясь на клиническую картину. Достоверно диагностировать патологию удается после смерти больного посредством патоморфологического изучения мозгового вещества. В ходе аутопсии выявляются признаки: гибель нейронов, формирующих черную субстанцию, депигментация мозговой ткани, глиоз, присутствие телец Леви. Диагностика болезни Паркинсона предполагает выполнение последовательных действий:
- Выявление синдрома паркинсонизма с типичными признаками (тремор в состоянии покоя, брадикинезия, постуральная нестабильность).
- Дифференциация от других патологий с похожей симптоматикой. На этом этапе применяют критерии исключения – семейный характер неврологических нарушений, отсутствие признаков прогрессирования на протяжении 3 лет, односторонняя или симметричная симптоматика в течение длительного периода, продолжительная ремиссия, отсутствие терапевтического эффекта после приема препаратов Леводопы.
- Сопоставление подтверждающих диагноз критериев. К ним относят одностороннюю симптоматику в начале заболевания, сохранение ассиметричного проявления симптомов на фоне их усугубления, прогрессирующее течение, многолетний период болезни, выраженное терапевтическое действие лекарств на основе Леводопы (уменьшение симптомов на 70-100%), сохранение ответа на прием Леводопы на протяжении 5 и более лет.
Подтверждением диагноза считается появление дискинезии (внезапные, непроизвольные движения группой мышц), спровоцированной приемом Леводопы. Чтобы правильно диагностировать болезнь Паркинсона, необходимо исключить такие патологии, как инсульт, опухоль мозга, гидроцефалия, повторные травмы в области головы.
Усомниться в диагнозе болезнь Паркинсона опытного врача заставят признаки поражения мозжечка и пирамидных путей, парез взора, окулогирные кризы (согласованное отклонение глаз), ранняя деменция, выраженная вегетативная симптоматика (ортостатическая гипотензия, расстройство мочеиспускания). Синдром паркинсонизма может развиться на фоне длительного приема нейролептиков (препараты, подавляющие психическую нервную деятельность).
Методы лечения
Болезнь Паркинсона лечит врач-невролог в зависимости от того, в какой стадии и форме она протекает. Чтобы эффективно бороться с болезнью Паркинсона, врач принимает решение, чем лечить пациента (выбор препаратов, схемы приема и дозировок), учитывая возраст, преобладающую симптоматику, характер течения. Болезнь Паркинсона лечится препаратами, устраняющими симптомы. Патогенетическая терапия, направленная на предотвращение гибели нейронов черной субстанции, не разработана.
Другое направление – нейропротекторная терапия. Лекарства нормализуют биохимический дисбаланс, затронувший область базальных ганглиев с последующим развитием таких эффектов, как снижение уровня дофамина и подавление деятельности глутаматергической, холинергической системы. Подбирая подходящие препараты, врач учитывает стадию заболевания, выраженность происходящих изменений, наличие соматических болезней, возраст и сферу профессиональной деятельности больного.
Чтобы вылечить болезнь Паркинсона, пациентам молодого возраста назначают такие препараты, как агонисты (усиливают биологический отклик) дофаминовых рецепторов, лекарства на основе вещества Амантадина (оказывает дофаминэргическое действие), ингибиторы фермента моноаминоксидазы (замедляют выработку фермента, препятствуя разрушению дофамина).

Лекарства на основе Карбидопы или Леводопы назначают, когда нужно бороться с такими проявлениями болезни Паркинсона, как двигательные нарушения. Обычно препараты Леводопы назначают на 2-3 стадии течения, если моторная дисфункция ограничивает двигательную активность пациента и ухудшает качество жизни. В 98% случаев даже небольшие дозы (200 мг/сутки) лекарства существенно уменьшают симптоматику.
Терапия Карбидопой или Леводопой эффективна на протяжении 4-6 лет. После длительного приема препаратов бывают побочные явления, которые осложняют состояние больного, усиливая дезадаптацию. При выявлении симптомов и признаков болезни Паркинсона у пожилых пациентов сразу проводится терапия Леводопой в комбинации с другими лекарствами, обладающими противопаркинсоническим действием.
Если в клинической картине преобладает симптом тремор в состоянии покоя, врач может назначить антихолинергические средства (Акинетон, Циклодол). Хирургические методы терапии показаны при выраженных двигательных нарушениях и сильных побочных эффектах после приема Леводопы, что делает невозможным увеличение дозы.
Для коррекции нарушений проводятся стереотаксические операции (прицельная деструкция участков мозгового вещества, ответственных за двигательную активность и мышечный тонус) и трансплантация нервной ткани, продуцирующей дофамин, в область базальных ганглиев. Альтернативный метод воздействия – криоталамотомия, когда под прицельным действием низких температур разрушаются мозговые структуры, по которым передаются патологические импульсы.
Чтобы остановить прогрессирование болезни Паркинсона в молодом возрасте, применяют различные методики. В числе передовых разработок в сфере медицины – пересадка стволовых клеток. Полное восстановление двигательной активности невозможно, но борьба с заболеванием эффективно ведется при помощи новейших методов лечения болезни Паркинсона, к которым относят стимуляцию мозговых структур в области субталамуса (отдел промежуточного мозга).
Новый подход к эффективному лечению болезни Паркинсона заключается в назначении комплексной терапии, где определенные препараты сочетаются с сеансами психотерапии и методами нейрохирургии. Лечение синдрома Паркинсона проводится с учетом первичного заболевания, которое спровоцировало появление характерной симптоматики. Акинетические кризы, возникшие на фоне болезни Паркинсона, лечат как любое угрожающее жизни состояние. Проводятся мероприятия:
- Искусственная (аппаратная) вентиляция легких (в случае нарушения дыхательной функции).
- Установка назогастрального зонда для обеспечения питания и введения фармацевтических средств.
- Введение Амантадина сульфата (капельно, внутривенно) курсом 10 дней (дозировка 500 мл).
Параллельно назначают препараты Гепарина (с целью профилактики тромбоза вен), антибактериальные средства (для предотвращения развития пневмонии гипостатического типа), лекарства, стабилизирующие водно-электролитный баланс.

Прогноз
Ответ на вопрос, можно ли вылечить болезнь Паркинсона, отрицательный. Болезнь Паркинсона неизлечима, что обуславливает относительно неблагоприятный прогноз для жизни. Статистика показывает, 25% пациентов в течение 5 лет после дебюта заболевания пребывают в состоянии тяжелой инвалидности. Смерть наступает в 65% случаев в период следующих 5 лет. Описаны истории болезни, когда пациенты жили с диагнозом дольше 15 лет.
Чтобы жить дольше с болезнью Паркинсона, необходимо выполнять предписания врача, в первую очередь такие, как регулярный прием антипаркинсонических препаратов и стимуляция двигательной активности (массаж, гимнастика). Прогноз, сколько проживет человек с подобным диагнозом, составляется индивидуально с учетом возраста больного, общего состояния здоровья, клинической картины. Реабилитация при болезни Паркинсона включает сеансы психотерапии, занятия лечебной гимнастикой, физиотерапевтические процедуры.
Профилактика
Программа специфической профилактики заболевания не разработана. Учитывая серьезные последствия болезни Паркинсона, важно при первых признаках патологии обратиться к врачу с целью ранней диагностики и назначения корректного лечения.
Болезнь Паркинсона возникает на фоне нейродегенеративных процессов, проявляется тремором в состоянии покоя, постуральной неустойчивостью, ригидностью мышц, замедлением и ограничением объема целенаправленных движений при сохранении асимметрии в проявлении симптоматики. Ранняя диагностика и корректная терапия относятся к благоприятным прогностическим факторам.
Просмотров: 250
почему возникает и как лечат – Зожник

Врач-невролог, кандидат медицинских наук, паркинсолог Юсуповской больницы Георгий Романович Попов поведал Зожнику о болезни Паркинсона – распространенной и пока неизлечимой.
Болезнь Паркинсона – самое частое нейродегенеративное заболевание после болезни Альцгеймера.
На 100 тысяч человек – от 120 до 180 случаев, причем, чем старше возрастная группа, чем чаще встречается заболевание. После 60 лет болезнью страдает уже 1% человек, среди людей старше 85 лет – от 2,6 до 4%. Но иногда болезнь может развиться и до 40 и даже до 20 лет.
Болезнь Паркинсона была диагностирована у многих известных людей. Среди них: Иоанн Павел II, Мао Цзедун, Ясир Арафат, испанский вождь Франко, художник Сальвадор Дали, поэт Андрей Вознесенский, боксер Мохаммед Али, актеры Робин Уильямс и Майкл Джей Фокс (ему была проведена таламотомия, но об этом – ниже).

Мохаммед Али и Майкл Джей Фокс – жертвы болезни Паркинсона.
Болезнь Паркинсона: причина науке неизвестна
Болезнь Паркинсона также называется идиопатическим паркинсонизмом («идиопатический» – возникающий по неизвестной причине). Собственно, современная наука пока затрудняется назвать точные причины возникновения болезни.
В настоящее время причины ищут, в основном, по генетическим факторам (мутирование генов) и среди малоизученных факторов внутренней и внешней среды, взаимодействие которых приводит к болезни Паркинсона.
Впрочем, эксперты сомневаются о весомом вкладе экологии именно в развитие болезни Паркинсона. Первые описания болезни были еще у Гиппократа и в аюрведе, тогда экология была хорошей, а люди всё равно болели. другой аргумент против экологии – заболевают чаще сельчане, где экология лучше, чем в городе.
Патологические гены чаще винят, когда дебют заболевания приходится на 4-й десяток жизни и раньше – когда паркинсонизм проявляется на 2-м десятке жизни.
Малоизученные факторы окружающей среды имеют большее значение, когда болезнь Паркинсона приходит в пожилом возрасте, а генетические факторы наоборот – отходят на второй план.

Есть и другие, более редкие причины паркинсонизма и соответствующие им типы паркинсонизма:
- нейролептический паркинсонизм,
- постгипоксический,
- инфекционный (энцефалит Экономо),
- посттравматический,
- интоксикационный (марганец, бензин, сероуглерод, угарный газ и др.),
- паркинсонизм при гидроцефалии или опухоли головного мозга
- сосудистый паркинсонизм
и другие варианты происхождения этого синдрома – по причине возникновения болезни.
Передается ли болезнь Паркинсона по наследству?
Ученые изучали однояйцевых близнецов, носящих абсолютно одинаковый генотип, при этом заболевает только один из близнецов, а другого болезнь обходит стороной.
Генетическая связь прослеживается, но случаи наследования болезни Паркинсона от родителей к детям не превышают 10%, при этом даже эта цифра, как показывает практика, явно завышена.
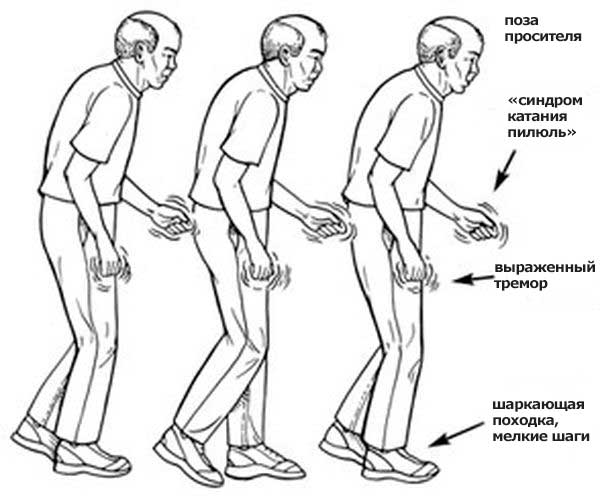
Некоторые симптомы болезни Паркинсона.
Как проявляется болезнь Паркинсона?
Двигательные симптомы болезни Паркинсона собственно формируют синдром паркинсонизма, который включает как минимум первый и еще один из трёх следующих признаков:
- Повышение мышечного тонуса по пластическому типу (когда сопротивление мышц на всех этапах пассивного движения как при сгибании, так и при разгибании – то есть сопротивляются и напряжены и мышцы-антагонисты, и мышцы-агонисты)
- Тремор покоя,
- Постуральная неустойчивость (нарушение способности удерживать равновесие).
Паркинсонизм на ранних стадиях: как определить и вовремя начать лечение
Ранние стадии болезни – это то золотое время, когда можно реально приостановить прогрессирование заболевания своевременным приемом противопаркинсонических препаратов. По горькому опыту отечественных врачей, больные чаще всего обращаются уже на развёрнутых стадиях, они просто не знают, как распознавать первые симптомы болезни.
Болезнь всегда начинается с одной стороны: появляется лёгкое подволакивание одной ноги, руки не двигаются содружественно при ходьбе. Нужно обращать внимание на изменение почерка (он может стать мельче), очень знаковый симптом – дрожание в покоящейся конечности, некоторые больные замечают неловкость в мелкоточечных движениях: шнуровке, застёгивании пуговиц.
Очень часто развиваются запоры, а курящие люди с лёгкостью бросают курение, часто больные испытывают непонятного происхождения боли в мышцах или в области плеча, беспричинно развивается тоска и тревога.
Если вы обнаружили у себя эти симптомы – надо сразу же обратиться к специалисту по болезни Паркинсона и расстройствам движений. Врач установит диагноз, поскольку очень многие состояния имитируют паркинсонизм.
Если вы нашли у себя перечисленные симптомы – проверьтесь у специалиста, Во-первых, это может быть не болезнь Паркинсона, во-вторых, сли все же она – чем раньше начнете лечение, тем дольше будете на ногах.
Лечение будет включать обязательное применение медикаментов, не менее важное значение имеет физкультура: упражнения на растяжку, мелкую моторику, очень полезны длительные пешие прогулки и плавание, которые способствуют выработке эндогенных нейротрофических факторов.
Многие пациенты отмечают, что при беге не чувствуют симптомов болезни. В общем, главное правило – неукоснительно принимать назначенные медикаменты и заниматься физкультурой.
Адинамия крайне вредна для течения болезни Паркинсона. Прочие медицинские мероприятия типа массажа, физиопроцедур, иглоукалывания также важны, но всё-таки отходят на второй план.
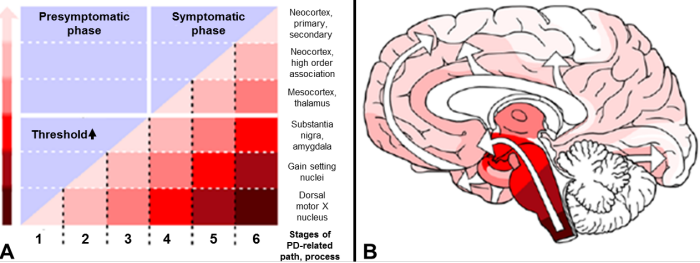
Стадии развития болезни Паркинсона: симптомы проявляются уже в середине развития болезни.
Сопутствующие паркинсонизму заболевания
Синдром паркинсонизма – спутник других заболеваний. Паркинсонизм встречается в группе нейродегенеративных заболеваний, также с неизвестной причиной происхождения как и болезнь Паркинсона, например мультисистемная атрофия, прогрессирующий надъядерный паралич, болезнь диффузных телец Леви, болезнь Альцгеймера, кортикобазальная дененерация, но в этих случаях синдром паркинсонизма не является доминирующим в клинической картине.
Какие типы паркинсонизма излечимы
В подавляющем большинстве случаев паркинсонизм прогрессирует и мало поддаётся лечению, исключение пока составляют:
- лекарственный паркинсонизм (чаще всего нейролептический) – когда причина возникновения – прием тех или иных лекарств,
- паркинсонизм при опухолях или иных внутричерепных объёмных образованиях, гидроцефалии,
- паркинсонизм при редком дисметаболическом заболевании, связанном с накоплением меди – болезни Вильсона.
В этих случаях устранение причины: отмена нейролептика, удаление опухоли и своевременно начатая терапия болезни Вильсона-Коновалова D-пеницилламином приводит к постепенному регрессу паркинсонизма.
Как лечат болезнь Паркинсона
Пока самые эффективные и распространённые методы лечения паркинсонизма – консервативные.
Драматический прорыв в терапии болезни Паркинсона возник с изобретением леводопы полвека назад и эффективность леводопы пока ничем не превзойдена.

Эффективность леводопы в лечении паркинсонизма пока никакие препараты не превзошли.
Из 6 классов противопаркинсонических препаратов леводопа остаётся «золотым стандартом» лечения болезни Паркинсона.
Сначала, на заре её применения, назначались максимально переносимые дозы, однако временная эйфория сменилась разочарованием: практически все пациенты стали испытывать укорочение действия принятой дозы, а с течением времени это явление прогрессировало, появлялись неясные насильственные движения и эти состояния только усугублялись.
Через несколько лет леводопу модернизировали. Добавление к леводопе периферических ингибиторов дофадекарбоксилазы (карбидопы или бенсеразида), которые не проникают в мозг, эффективно предотвращало побочные действия дофамина и его метаболитов на периферии, повышало биодоступность леводопы, но не решило проблему поздних двигательных осложнений – главной проблемы лечения паркинсонизма леводопой.
Вся последующая эволюция медикаментозного лечения болезни Паркинсона в общем-то была направлена на профилактику и коррекцию этих двигательных осложнений.
С течением времени появились пролонгированные формы леводопы, появились так называемые агонисты дофаминовых рецепторов, стали активнее применяться препараты амантадина, у которых был обнаружен антидискинетический эффект, постепенно стали появляться препараты, блокирующие распад леводопы и её главного активного метаболита – дофамина (Ингибиторы КОМТ и МАО-Б).
Но тем не менее: со временем двигательные осложнения лечения леводопой нарастают и в крайних случаях применяется хирургическое вмешательство.
Операции применяются при дискинезиях и треморе, резистентном к медикаментозной терапии.
Хирургические методы лечения паркинсонизма
Наиболее ранними являются так называемые деструктивные операции: разрушение с одной стороны мозга определённых ядер приводило к исчезновению дискинезий и тремора на противоположной стороне, попытки двусторонней деструкции приводили к крайне неприятным последствиям – нарушению глотания, потери голоса и нередко к тяжёлой депрессии, впоследствии техники деструктивных операций усовершенствовались, появился неинвазивный метод операций – гамма нож, основанный на радиологическом фокусе точки-мишени в головном мозге.
Менее опасный и более эффективный метод хирургических операций – стимуляция глубинных структур головного мозга (DBS). Но это дорогостоящее вмешательство может также привести к ряду побочных эффектов.
Следует добавить, что любое хирургическое вмешательство не позволяет отменить противопаркинсонические средства и имеет свои строгие показания и противопоказания.
Инвазивные методы лечения паркинсонизма
Альтернативные и относительно новые методы лечения – инвазивные методы.
Один из методов – парентеральное введение дуодопы (леводопы/карбидопы в виде геля) непосредственно в 12-перстную кишку. До этого момента проходит испытательный период (от суток до 3-х), когда подбирается оптимальная доза через установленный назогастральный зонд, после чего проводится операция по внедрению канюли в 12-перстную кишку через желудок, которая фиксируется на коже. К ней подключается картридж с дуодопой, обеспечивающий непрерывное поступление дуодопы в кишечник, картридж меняется ежедневно. Метод уникальный, во многом безальтернативный, но имеющий некоторые недостатки, связанные, как правило, с очень чётким выполнением инструкций по применению пациентами, к тому же с течением времени у больных может развиться полинейропатия, связанная с дефицитом витаминов В6 и В12.
Последней разновидностью леводопосодержащих препаратов является форма, высвобождаемая крайне медленно и равномерно, требующая трёхкратного приёма в определённые часы. Но препарат в нашей стране не зарегистрирован, и хотя в США и некоторых странах он появился на рынке под торговым названием Rytary, пока ещё продолжаются его клинические испытания. (по информации drugs.com препарат стоит $280-350 за 100 капсул в зависимости от дозировок действующих препаратов)
Еще одно современное средство, схожее по структуре с леводопой – её метиловый эфир (L-DOPA methylester hydrochloride), который легко проникает через слизистые оболочки и гематоэнцефалический барьер и вызывает быстрое «включение» у пациентов с моторными флуктуациями. Препарат проходит последние стадии клинических исследований, но когда он появится на российском рынке пока неизвестно.
Другой современный инвазивный метод (условно инвазивный, поскольку препарат вводится подкожно) – применение апоморфиновых помп, которые автоматически через определённые промежутки времени вводят препарат. Апоморфин – один из давно открытых препаратов группы агонистов дофаминовых рецепторов, действие его наступает гораздо быстрее, чем у стандартных и быстродействующих форм леводопы, и едва ли не превосходит по противопаркинсоническому действию леводопe. Но препарат вызывает массу нежелательных явлений, для предотвращения которых требуется приём других медикаментов.
Опыт западных коллег подсказывает, что помпы лучше заменить эпизодическим подкалыванием препарата больными самостоятельно для быстрого выхода из состояния «выключения», т.е. обездвиженности. Апоморфин пока не зарегистрирован в нашей стране как противопаркинсонический препарат.
Лечение паркинсонизма с помощью плацебо
Во многих клинических исследованиях на первых порах плацебо оказывалось эффективным среди примерно 4% пациентов, поэтому данный эффект начисто пропадал, что в общем-то характерно для всех органических поражениях головного мозга.
Терапия болезни Паркинсона – симптоматическая
Практически все вышеописанные способы лечения паркинсонизма – по сути, симптоматические, но своевременно начатая и адекватная терапия помогает сохранить мобильность пациентов и положительно сказывается в отдалённой перспективе.
Взгляды на назначение препаратов леводопы менялись: от немедленного назначения с момента постановки диагноза – до максимальной отсрочки её назначения.
Сейчас утвердилось мнение, что леводопу следует назначать не слишком рано и не слишком поздно, только тогда, когда другие противопаркинсонические средства становятся недостаточно эффективными.
Это правило не распространяется на больных старше 70 лет, так как парадоксальным образом моторные осложнения в этой возрастной категории если и развиваются, то протекают мягче и, к тому же чем выше возраст, тем больше хронических заболеваний, выше риск ятрогенных психозов, а препараты леводопы являются наиболее переносимыми, помимо наибольшей эффективности.
Неэффективные методики лечения болезни Паркинсона
В прошлом были попытки терапии болезни Паркинсона антиоксидантами, но исследования показали их неэффективность.
То же можно сказать и о внедрении в организм стволовых клеток, когда эффект оказывался кратковременным и наступало обвальное ухудшение состояния, тем не менее генно-инженерные стволовые клетки пока не полностью себя дискредитировали, но требуется ещё много усилий для доведения этого способа до надежного и эффективного.
Существующие в настоящее время методики со стволовыми клетками можно считать еще и неэтичными, поскольку для этого способа часто используется так называемый «абортивный материал».
Болезнь Паркинсона: перспективы лечения
Увы, прогнозы на излечение болезни, как правило, дают шарлатаны, которых немало в интернете. Серьёзные исследователи, в общем-то, пока не наполнены оптимизмом.
Тем не менее – любая болезнь потенциально излечима, и если найдётся способ излечения болезни Паркинсона, то это будет величайший прорыв в неврологии, сопоставимый с изобретением антибиотиков. Возможно, способ излечения от болезни Паркинсона окажется универсальным для всех нейродегенеративных заболеваний, и это будет новая эра в медицине.
В настоящее время на уровне пробирки исследуется эффективность некоторых антибиотиков в предотвращении агрегации белка ᾱ-синуклеина, конгломераты которого оказывают цитотоксическое действие.
Попытки внедрения нейротрофических факторов в организм для восстановления частично поражённых клеток пока не увенчались успехом, поскольку нейротрофические факторы оказывают своё действие не в поражённых клетках мозга, а в соседних глиальных клетках. Способ адресной доставки пока разрабатывается.
В качестве потенциального средства для лечения болезни Паркинсона также разрабатываются препараты, способствующие выработке эндогенных белков – шаперонов, которые способствуют правильной укладке синтезируемых белков в нейронах.
Автор: врач-невролог, кандидат медицинских наук, паркинсолог Юсуповской больницы Георгий Романович Попов
Читайте также на Зожнике:
Наука о пользе тайцзи
Откуда берется облысение и опасно ли оно для здоровья?
Шкала развода на диагноз: 5 главных признаков псевдодиагностики
Плацебо и ноцебо: правила самоизлечения
Онколог Илья Фоминцев: «Люди, которые заболеют раком через 10 лет, смогут его не бояться»
Расскажите друзьям:
Болезнь Паркинсона | ЕвразияМед
Что такое болезнь Паркинсона
Паркинсонизм или болезнь Паркинсона (дрожательный паралич) – хроническое прогрессирующее заболевание головного мозга, впервые описанное в 1817 г. английским врачом Дж. Паркинсоном. Больные паркинсонизмом часто страдают от непроизвольного дрожания конечностей (тремора), мышечной ригидности (жесткости), нарушения координации и речи, а также испытывают затруднения с передвижением. Эти симптомы обычно развиваются после 60 лет, хотя известны случаи заболевания паркинсонизмом в возрасте младше 50 лет.
Болезнь Паркинсона – прогрессирующее заболевание, т.е. его симптомы и проявления с течением времени обостряются и ухудшаются. Однако, несмотря на то, что в конечном итоге болезнь Паркинсона приводит к инвалидности и потере дееспособности, заболевание прогрессирует медленно, и даже после постановки диагноза большинство больных еще долгие годы может вести полноценную жизнь.
Симптомы болезни Паркинсона
Первые симптомы болезни Паркинсона сложно заметить – как, например, неподвижность рук при ходьбе, легкий тремор (дрожание) в пальцах рук или незначительные нарушения речи. Больные чувствуют опустошение, упадок сил, подвержены депрессии или страдают от бессонницы. Кроме того, привычные занятия (душ, бритье, приготовление пищи и т.п.) требуют больших усилий и занимают больше времени:
- Тремор. Тремор часто начинается с легкого дрожания рук или даже отдельных пальцев. Иногда дрожание рук сопровождается неравномерным движением большого и среднего пальцев, напоминающим перекатывание невидимых. Тремор особенно проявляется, когда больной находится в состоянии стресса.
- Замедленность движения.
- Потеря равновесия.
- Потеря автоматизма движений.
- Многие больные паркинсонизмом также страдают от нарушения речи – она может стать слабо модулированной, неразборчивой. Голос теряет интонации и становится монотонным и тихим.
- Нарушение глотания и слюноотделения. Этот симптом появляется на поздних стадиях развития болезни.
- Слабоумие. Незначительный процент больных паркинсонизмом страдает от слабоумия – неспособности мыслить, понимать и запоминать. Этот симптом также появляется на поздних стадиях заболевания.
Причины болезни Паркинсона
Сегодня известно, что многие симптомы и проявления болезни Паркинсона развиваются вследствие повреждения или разрушения определенных нервных окончаний (нейронов), расположенных в черном веществе головного мозга. В нормальном состоянии эти нервные клетки вырабатывают дофамин. Функция дофамина заключается в плавной передаче импульсов для обеспечения нормальных движений.
При болезни Паркинсона уменьшается продукция дофамина, нарушается нормальная передача нервных импульсов и появляются основные симптомы паркинсонизма.
В процессе старения все люди лишаются некоторой части вырабатывающих дофамин нейронов. Но больные паркинсонизмом теряют более половины нейронов, расположенных в черном веществе. Хотя происходит вырождение и других клеток головного мозга, именно клетки, вырабатывающие дофамин, необходимы для движения, поэтому их потеря катастрофична. Причины повреждения или разрушения этих клеток до сих пор является объектом многих исследований.
По мнению ученых, болезнь Паркинсона может развиваться вследствие неблагоприятного сочетания генетических и внешних факторов. Определенные лекарства, болезни и токсические вещества также могут создавать клиническую картину, характерную для паркинсонизма.
Вторичный паркинсонизм также может быть обусловлен инфекционным, травматическим поражением головного мозга, инфекционными или лекарственными воздействиями, а так же сосудистыми или опухолевыми заболеваниями.
Лечение паркинсонизма
На данный момент не существует методов лечения, которые могли бы устранить причину болезни Паркинсона, затормозить вызывающие её процессы в головном мозге.
Современные лекарства хорошо снимают симптомы заболевания. Это таблетки, которые нужно пить каждый день. В зависимости от стадии болезни и эффективности лечения, врач при повторных осмотрах меняет дозы препаратов, добавляет и отменяет лекарственные средства.
Наиболее эффективны препараты леводопы, восполняющие дефицит дофамина в головном мозге. Подбор схемы лечения должен проводить врач-невролог, имеющий специальную подготовку и опыт ведения таких больных.
Справиться с симптомами и повысить качество жизни пациента помогает лечебная физкультура: тренировка ходьбы и равновесия, мелких движений под контролем инструктора. В последнее время в качестве упражнений широко используется скандинавская ходьба.
Требуется особое внимание, если человеку с болезнью Паркинсона проводится операция или назначается лечение в связи с другими заболеваниями. Это может повлиять на эффективность противопаркинсонической терапии, вызвать осложнения. Чтобы избежать отрицательных последствий, необходимо обсуждать любые предстоящие вмешательства с лечащим врачом-неврологом.
причины, симптомы, лечение и знаменитости с диагнозом
Болезнь Паркинсона — это медленно развивающееся заболевание нервной системы, проявляющееся в дрожании с состоянии покоя, замедленности движений и нарушении рефлексов. Болезнь хроническая, прогрессирующая и неизлечимая. Наиболее характерна для людей старшей возрастной группы.
Причины болезни Паркинсона
Болезнь Паркинсона развивается из-за постепенного разрушения нейронов, вырабатывающих один из важнейших нейромедиаторов в организме — дофамин.
Дофамин служит важной частью системы вознаграждения в мозге, отвечает за формирование чувства любви, участвует в процессах обучения и мыслительной деятельности.
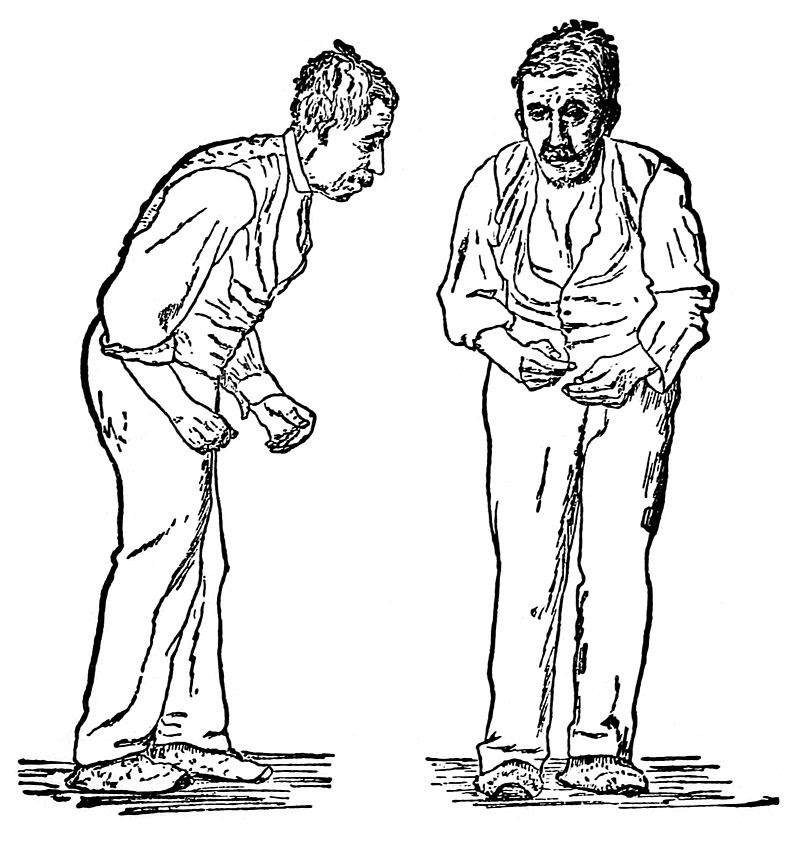 wikipedia.org / William Richard Gowers
wikipedia.org / William Richard Gowers
Причины, по которым возникает болезнь Паркинсона и начинают стремительно гибнуть нервные клетки, до сих пор не выявлены. Известны факторы риска — это старение, генетическая предрасположенность, негативное воздействие факторов окружающей среды.
Около 15% заболевших Паркинсоном имеют в семейном анамнезе это заболевание. Но какие гены отвечают за развитие болезни, также не установлено.
Обычное старение тоже сопровождается уменьшением числа нейронов и дофаминовых рецепторов. Но при болезни Паркинсона темпы этого процесса намного выше.
Болезнь Паркинсона в 80% случаев развивается без каких-либо предпосылок. В оставшихся 20% паркинсонизм может быть осложнением других заболеваний: энцефалита, опухоли мозга, инсульта, черепно-мозговой травмы и некоторых других. Иногда к паркинсонизму может привести отравление токсичными веществами (угарный газ, этанол), прием наркотиков и нейролептиков.
Болезнь Паркинсона у пожилых, мужчин и женщин
Число больных Паркинсоном значительно увеличивается среди взрослых людей. Чаще всего первые симптомы заболевания появляются в 55-60 лет.
Но порой болезнь может развиться и до 40. Есть и так называемая ювенильная форма, когда заболевание проявляется в 20 лет.
Мужчины болеют несколько чаще, чем женщины. Существенных различий в зависимости от расовой принадлежности не выявлено.
Признаки и симптомы
Одним из главных признаков болезни является дрожание в состоянии покоя. Это ритмическое подергивание пальца руки, напоминающее скатывания хлебного шарика. Реже симптом проявляется на ногах. Также наблюдается дрожание челюсти, языка, век.
К тому же наблюдается замедление и снижение количества движений. Больные могут надолго замирать в одной позе, лицо становится как маска с открытым ртом, возникает шаркающая семенящая походка, руки при ходьбе не движутся в такт.
Также появляется мышечная ригидность (повышенный тонус мышц). Из-за постоянного напряжения человек становится сгорбленным, с согнутыми руками и ногами, вытянутой вперед головой.
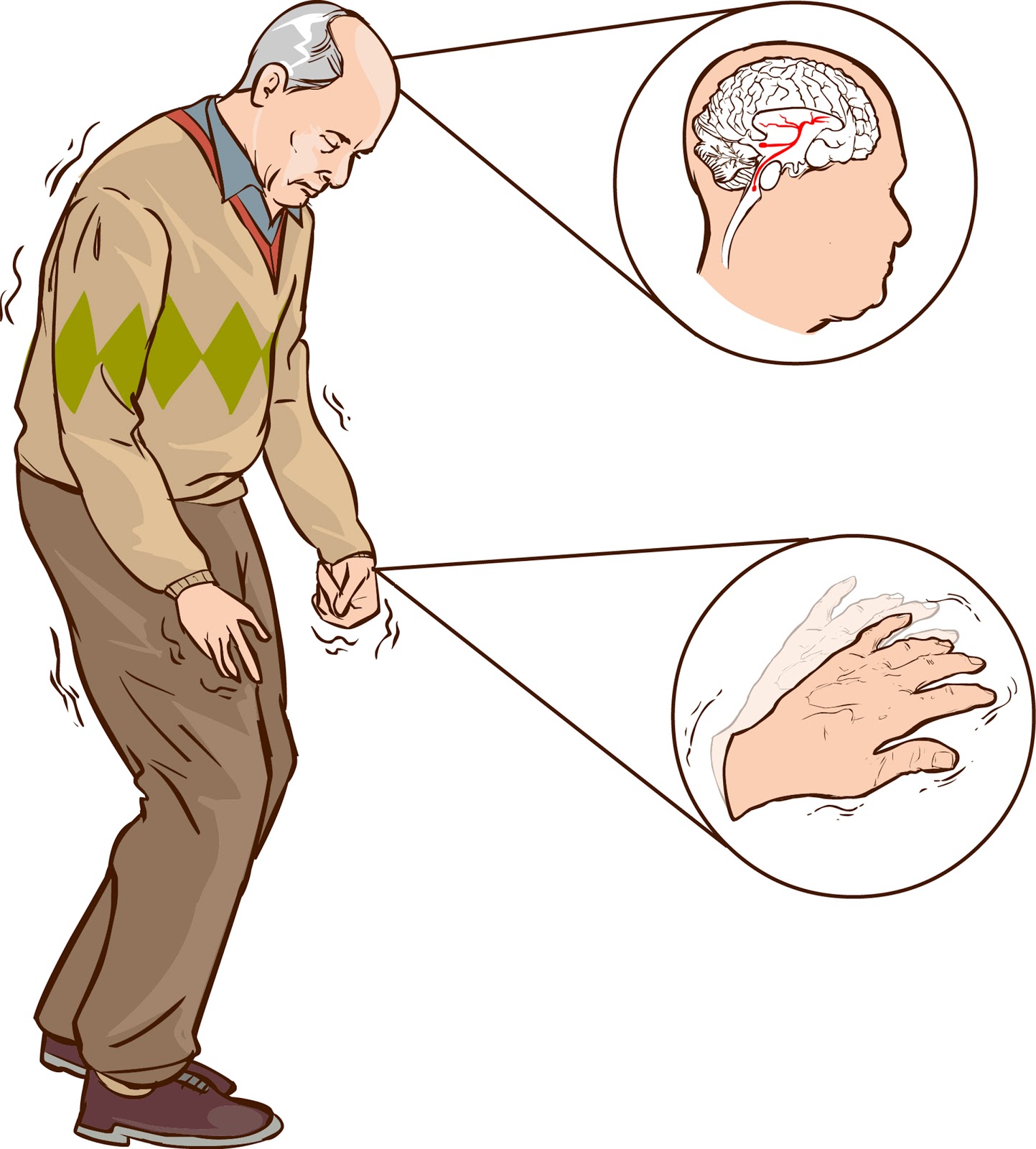 Фото: depositphotos
Фото: depositphotos
На поздних стадиях развивается постуральная неустойчивость: больному трудно начать движение или остановиться. Человек постепенно теряет контроль над своим телом, ему становится сложно удерживать равновесие.
Речь делается замедленной, невыразительной, малопонятной, тихой и с запинками. Пропадает интонация.
К тому же могут возникнуть себорея (избыточная выработка кожного сала), запоры, недержание, снижение артериального давления, половая дисфункция.
Слабоумие развивается у половины больных, чаще при начале заболевания с двусторонним поражением. Но даже у пациентов, сохранивших рассудок, замедляются мыслительные процессы и ухудшается память, возникает равнодушие к себе и миру, снижается настроение.
Стадии болезни
При болезни Паркинсона выделяют пять основных стадий и еще несколько дополнительных:
Стадия 0 — отсутствие признаков заболевания.
Стадия 1 — симптомы проявляются на одной из конечностей.
Стадия 1,5 — симптоматика проявляется на одной из конечностей и туловище.
Стадия 2 — двусторонние проявления без постуральной неустойчивости.
Стадия 2,5 — двусторонние проявления с постуральной неустойчивостью.
Стадия 3 — двусторонние проявления. Постуральная неустойчивость. Больной способен к самообслуживанию.
Стадия 4 — больной не может совершать сложных движений и нуждается в посторонней помощи, но способен ходить и/или стоять без поддержки.
Стадия 5 — больной прикован к креслу или кровати. Тяжелая инвалидизация.
Методы лечения
Вылечить болезнь Паркинсона полностью нельзя. Но можно бороться с ее симптомами, облегчая жизнь пациента.
Для сохранения двигательной активности разрабатывают индивидуальную программу физических упражнений, а также назначают лекарства с леводопой и агонисты дофаминовых рецепторов (имитируют действие дофамина). Также применяются лекарства с веществами, способными повышать содержание дофамина в ЦНС.
 Пациент с болезнью Паркинсона выполняет физические упражнения. Фото: Reuters
Пациент с болезнью Паркинсона выполняет физические упражнения. Фото: Reuters
При неэффективности такого лечения и сильном проявлении тремора или двигательных расстройств возможно проведение операции. Но при этом высок риск осложнений.
Сейчас используют и малоинвазивную хирургию, вживляя в мозг пациента электроды, которые соединяют с имплантируемым подкожно нейростимулятором.
Болезнь Паркинсона у знаменитостей
Неизлечимым недугом страдали многие известные личности. В последние годы жизни болезнь развилась у китайского лидера Мао Цзэдуна. От нее страдал палестинский политик Ясир Арафат. Был неутешительный диагноз и у Адольфа Гитлера.
У испанского живописца Сальвадора Дали болезнь диагностировали за восемь лет до смерти. Поэт Андрей Вознесенский после 15 лет заболевания умер от его осложнений. НА протяжении 35 лет с недугом боролся боксер Мохаммед Али, который был вынужден завершить свою спортивную карьеру из-за диагноза.
В недавнем интервью Британский рок-музыкант Оззи Осборн рассказал, что у него также болезнь Паркинсона. Уже год он проходит тяжелый курс лечения.
 Фото: instagram / ozzyosbourne
Фото: instagram / ozzyosbourne
Болезнь Паркинсона — причины, симптомы, диагностика и лечение
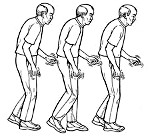
Болезнь Паркинсона — медленно прогрессирующее дегенеративное заболевание центральной нервной системы, основными проявлениями которого являются такие двигательные нарушения, как гипокинезия, ригидность мышц, тремор покоя, постуральные расстройства. Кроме этого при болезни Паркинсона развиваются вегетативные, аффективные и другие расстройства. Различают истинный паркинсонизм (болезнь Паркинсона) и синдром паркинсонизма, который может сопровождать многие неврологические заболевания (ЧМТ, опухоли головного мозга, инсульты, энцефалиты и пр.). При подозрении на болезнь Паркинсона пациенту необходимо пройти электроэнцефалографию, реоэнцефалографию, МРТ головного мозга.
Общие сведения
Болезнь Паркинсона — медленно прогрессирующее дегенеративное заболевание центральной нервной системы, основными проявлениями которого являются такие двигательные нарушения, как гипокинезия, ригидность мышц, тремор покоя, постуральные расстройства. Кроме этого при болезни Паркинсона развиваются вегетативные, аффективные и другие расстройства.
Классификация болезни Паркинсона
Классификация болезни Паркинсона основывается на возрасте начала болезни:
Также известны различные классификации синдрома паркинсонизма:
- дрожательные
- дрожательно-ригидные
- ригидно-дрожательные
- акинетико-ригидные
- смешанные
Однако данные классификации болезни Паркинсона и синдрома паркинсонизма не считаются безупречными. Поэтому на сегодня общепринятого подхода в этом вопросе не существует.
Этиология и патогенез болезни Паркинсона
Современной медициной достигнут определенный прогресс в понимании молекулярных и биохимических механизмов болезни Паркинсона. Не смотря на это, остается неизвестной истинная этиология спорадических форм этого заболевания. Большое значение имеют генетическая предрасположенность и факторы внешней среды. Сочетание и взаимодействие этих двух факторов инициируют процесс дегенерации в пигментсодержащих, а впоследствии и других нейронах ствола головного мозга. Такой процесс, однажды возникнув, становится необратимым и начинает экспансивное распространение по всему мозгу. Более других белковых субстанций нервной системы наибольшему разрушению подвергается альфа-синуклеин. На клеточном уровне механизм этого процесса выглядит как недостаточность дыхательных функций митохондрий, а также окислительный стресс — основная причина апоптоза нейронов. Однако в патогенезе болезни Паркинсона принимают участие и другие факторы, функции которых остаются не раскрытыми до сих пор.
Клиническая картина болезни Паркинсона
Существует тетрада двигательных симптомов болезни Паркинсона: тремор, ригидность, гипокинезия, нарушения постуральной регуляции. Тремор — самый очевидный и легковыявляемый симптом. Наиболее типичен для паркинсонизма тремор покоя, однако возможны и другие виды тремора, например: постуральный тремор или интенционный тремор. Мышечная ригидность может быть малозаметной на начальных стадиях, чаще при дрожательной форме болезни Паркинсона, но очевидной при выраженном синдроме паркинсонизма. Большое значение имеет ранее выявление минимальной асимметрии тонуса в конечностях, так как асимметрия симптомов — характерный признак всех стадий болезни Паркинсона.
Гипокинезия является облигатным симптомом паркинсонизма любой этиологии. На начальных стадиях болезни Паркинсона выявление гипокинезии может затруднено, поэтому прибегают к демонстративным приемам (например, быстро сжать и разжать кулак). Ранние проявления гипокинезии можно наблюдать в элементарных действиях, направленных на самообслуживание (бритье, чистка зубов, застегивание мелких пуговиц и др.). Гипокинезия — это брадикинезия (замедленность движений), олигокинезия (уменьшение кол-ва движений), а также уменьшение амплитуды движений и снижение их скорости. По причине гипокинезии при болезни Паркинсона нарушается индивидуальный «язык тела», в том числе жесты, мимика, речь и пластичность моторики.
Постуральные нарушения при болезни Паркинсона проявляются довольно рано (например, ассиметрия вытянутых вперед рук). Однако чаще всего они привлекают внимание врачей уже в дезадаптационной своей стадии (III стадия). Объяснением этому может служить тот факт, что постуральные нарушения в сравнении с другими симптомами болезни Паркинсона менее специфичны для нее.
Кроме вышеупомянутых основных проявлений паркинсонизма, болезни Паркинсона сопутствуют и другие симптомы, которые в некоторых случаях могут выходить на первый план клинической картины. Причем степень дезадаптации пациента в таких случаях ничуть не меньше. Перечислим только некоторые из них: слюнотечение, дизартрия и/или дисфагия, запор, деменция, депрессия, нарушения сна, дизурические расстройства, синдром беспокойных ног и другие.
Различают пять стадий болезни Паркинсона, каждая из которых отражает степень тяжести заболевания. Наибольшее распространение получила классификация, предложенная в 1967 году Хеном и Яром:
- 0 стадия — двигательные проявления отсутствуют
- I стадия — односторонние проявления заболевания
- II стадия — двусторонние симптомы без постуральных нарушений
- III стадия — умеренная постуральная неустойчивость, но пациент не нуждается в посторонней помощи
- IV стадия — значительная утрата двигательной активности, но пациент в состоянии стоять и передвигаться без поддержки
- V стадия — в отсутствие посторонней помощи пациент прикован к креслу или постели
Диагноз болезни Паркинсона
Клиническая диагностика болезни Паркинсона проходит в три этапа.
1-ый этап
Распознавание синдрома паркинсонизма и его синдромальная дифференциация от своих неврологических и психопатологических синдромов, так или иначе схожих с истинным паркинсонизмом. Истинный паркинсонизм — это гипокинезия в сочетании с одним из следующих симптомов: тремор покоя (4-6 Гц), мышечная ригидность, постуральная неустойчивость, не связанная с первичными вестибулярными, зрительными и мозжечковыми нарушениями.
2-ой этап
Исключение иных заболеваний, которые могут проявляться синдромом паркинсонизма. Существует несколько критериев исключения болезни Паркинсона:
- окулогирные кризы
- терапия нейролептиками перед дебютом заболевания
- наличие в анамнезе повторных инсультов со ступенеобразным прогрессированием симптомов паркинсонизма, достоверный энцефалит или повторные ЧМТ
- продолжительная ремиссия
- исключительно односторонние проявления в течение более 3 лет
- мозжечковые симптомы
- надъядерный паралич взора
- ранее яркое проявление деменции
- ранее яркое проявление вегетативной недостаточности
- симптом Бабинского
- опухоль головного мозга или открытая гидроцефалия
- неэффективность больших доз леводопы
- интоксикация МФТП
3-й этап
Выявление симптомов, подтверждающих болезнь Паркинсона. Для этого необходимо наличие как минимум трех из нижеперечисленных критериев:
- односторонние проявления в дебюте болезни
- наличие тремора покоя
- асимметрия симптомов (с большей степенью выраженности на стороне тела, с которой началось заболевание)
- 70-100%-реакция на терапию леводопой
- прогрессирующее течение заболевания
- эффективность леводопы в течение 5 лет и более
- продолжительность заболевания 10 лет и более
Для обследования пациентов с подозрением на болезнь Паркинсона применяют реоэнцефалографию, ЭЭГ, методы нейровизуализации: КТ головного мозга и МРТ.
Дифференциальный диагноз
Болезнь Паркинсона необходимо дифференцировать от всех заболеваний, которые сопровождаются синдромом паркинсонизма: вторичный паркинсонизм, псевдопаркинсонизм, «паркинсонизм плюс». Около 80% случаев синдрома паркинсонизма приходится на болезнь Паркинсона.
Следует помнить об определенных клинических особенностях паркинсонизма, которые должны вызывать сомнения в диагнозе болезнь Паркинсона, например: неэффективность леводопы, отсутствие тремора, симметричность двигательных нарушений, ранние проявления признаков периферической вегетативной недостаточности.
Лечение болезни Паркинсона
Пути лечения болезни Паркинсона существенно различаются на ранних и поздних стадиях заболевания, поэтому их стоит рассматривать раздельно.
Лечение болезни Паркинсона на ранних стадиях.
Ранее диагностирование болезни Паркинсона не всегда означает незамедлительное начало какой-либо лекарственной терапии. Для определения сроков начала лекарственного лечения необходимо учитывать тяжесть заболевания, продолжительность заболевания, темп его прогрессирования, любые сопутствующие заболевания, а также «личные факторы» (профессиональное, социальное и семейное положение пациента, психическое состояние, особенности личности и т. д.). Цель такой терапии — восстановление (достаточный регресс) нарушенных функций посредством минимально возможных доз.
Лекарственная терапия на ранней стадии болезни Паркинсона подразумевает использование препаратов, увеличивающих синтез дофамина в мозге, стимулирующих его выброс и блокирующих обратное его поглощение, угнетающих распад дофамина, стимулирующих дофаминовые рецепторы и препятствующие гибели нейронов. К таким препаратам относятся амантадин, селективные ингибиторы МАО-В (селегилин и др.), агонисты дофаминовых рецепторов (пирибедил, прамипексол и др.). Допускается применение вышеуказанных препаратов как в виде монотерапии (чаще), так и в различных комбинациях.
Вышеперечисленные препараты значительно уступают по эффективности препаратам леводопы, однако для лечения болезни Паркинсона на ранних стадиях они вполне подходят. Теоретически на ранних стадиях болезни Паркинсона агонисты дофаминовых рецепторов способны отсрочить назначение леводопы, а на поздних стадиях — снизить ее дозу. Однако не в их пользу говорит большое количество побочных эффектов (язва желудка, ортостатическая гипотензия, психические нарушения, эритромелалгия, ретроперитонеальный фиброз и др.) и способность снижать чувствительность постсинаптических дофаминовых рецепторов.
Четкие критерии, определяющие оптимальное время начала лечения препаратами леводопы, отсутствуют. Тем не менее, следует учитывать возраст пациента (по возможности после 60-70 лет), избегать раннего назначения леводопы, при подборе дозы ориентироваться на «откликаемость» пациента на препарат, улучшений в его профессиональной и социальной деятельности.
Лечение болезни Паркинсона на поздних стадиях.
В независимости от характера течения болезни Паркинсона обязательно происходит постепенная трансформация клинической картины заболевания. Со временем прогрессируют уже присутствующие нарушения и появляются новые, большинство из которых с трудом поддается терапии, оказывая тем самым сильное стрессорное воздействие на пациента. Кроме этого, меняется привычный эффект от леводопы — снижается эффективность препарата, нарастают лекарственные дискинезии (как результат гиперчувствительности дофаминовых рецепторов).
Снижение эффективности терапии проявляется снижением срока лечебного действия каждой лозы леводопы. Формируется феномен «включения-выключения», единственным способом борьбы с которым становится постепенное повышение дозы леводопы, а это в свою очередь запускает порочный круг, порождающий новые проблемы, бороться с которыми становится все тяжелее. Реальная помощь в данном случае может быть оказана двумя способами: назначением дополнительной дозы леводопы в целях сокращения интервалов между приемами; добавлением в схему лечения ингибитора КОМТ и переводом пациента на терапию комбинированным препаратом леводопы и энтакапона.
Побочные эффекты терапии леводопой. Одно из проявлений снижения порога чувствительности к некоторым побочным эффектам — тенденция к появлению оральных (или иных) гиперкинезов на фоне симптомов гиперкинезии. Таким образом, в клинической картине болезни Паркинсона парадоксальным образом сочетаются симптомы избытка дофамина (оральные гиперкинезы) и его дефицита (гипокинезия). Снижение дозы леводопы в такой ситуации дает только временное устранение гиперкинеза, через некоторое время он появляется вновь. Ортостатическая артериальная гипотензия при болезни Паркинсона проявляется обычно относительно резким снижением артериального давления вскоре после приема леводопы. Таким побочным эффектом обладают и леводопа, и агонисты дофаминовых рецепторов, поэтому после определения причины побочного эффекта необходимо уменьшить дозу соответствующего препарата.
Психические нарушения при болезни Паркинсона могут проявляться в виде депрессии, тревоги, апатии, зрительных галлюцинаций, ажитации. Кроме того, типично появление запоминающихся, ярких сновидений. Со временем все вышеперечисленные нарушения прогрессируют и рано или поздно проявляются и в состоянии бодрствования. Терапию таких психических нарушений необходимо проводить совместно с психиатром. Иногда достаточно избавить пациента от тревоги и страха, так как именно они провоцируют более грубые психические нарушения. Большинство лекарственных дискинезий проявляется на пике действия препарата. Наиболее надежный способ их устранения — уменьшение разовой дозы леводопы с сохранением суточной дозы препарата. Поэтому дробный прием малых доз леводопы — наилучший способ предотвращения дискинезий такого типа.
В терминальной стадии болезни Паркинсона основные сложности связаны с кахексией, утратой способности к стоянию, ходьбе и самообслуживанию. В это время необходимо проведение целого комплекса реабилитационных мероприятий, направленных на обеспечение оптимальных условий для повседневной бытовой деятельности пациента. Следует помнить, что на поздних стадиях болезнь Паркинсона становится тяжелым бременем не только для самого пациента, но и для его семьи, членам которой может потребоваться не только терапевтическая, но иногда и специализированная помощь.
Хирургическое лечение болезни Паркинсона заключается в проведении стереотаксической деструкции вентролатерального ядра таламуса и субталамического ядра, а также глубокой стимуляции мозга. В случае выраженного акинетико-ригидного синдрома рекомендована паллидотомия, а также глубокая электростимуляция бледного шара и субталамического ядра.
Прогноз
Для болезни Паркинсона характерно неуклонное нарастание выраженной симптоматики. В 25% случаев в течение первых пяти лет заболевания наступает инвалидизации или смерть. У 89% пациентов, переживших 15 лет течения болезни Паркинсона, неизбежно наступает тяжелая степень инвалидности или смерть. Отмечено снижение уровня смертности пациентов с болезнью Паркинсона в связи с началом применения леводопы, а также рост продолжительности жизни.
