«Летающие мушки»
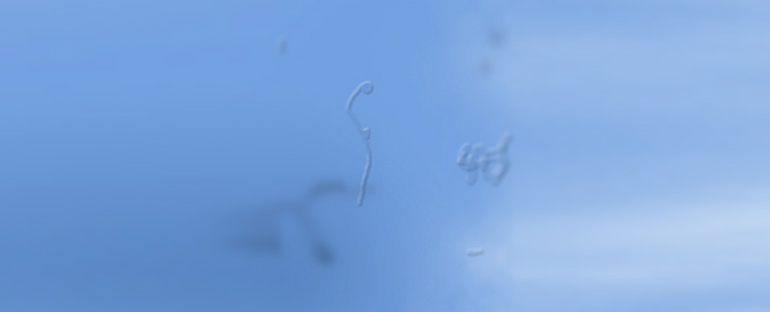
Многим людям знакомо внезапное появления «точек», «полос», «червячков» перед глазами.
Лучше всего помутнения заметны при взгляде на чистую яркую поверхность (чистое небо, белый потолок, снег и т.д). В условиях слабого освещения окружающей среды помутнения, как правило, не видны.
Почему возникает подобный визуальный эффект и что с этим делать?
Чаще всего такие жалобы как «мушки перед глазами» связаны с развитием инволюционных (то есть возрастных) изменений стекловидного тела глаза. Данное явление принято называть деструкцией стекловидного тела.
А что же такое стекловидное тело? Представлено оно в виде бессосудистого прозрачного студенистого вещества, которое заполняет полость глазного яблоко между хрусталиком и сетчаткой. Его наличие обеспечивает сохранение правильной формы глазного яблока, компенсирует перепады внутриглазного давления, осуществляет проведение световых импульсов к сетчатке глаза.
У здорового человека стекловидное тело полностью прозрачно и не содержит каких-либо включений.
Помимо характерных для деструкции стекловидного тела глаза «мушек» в поле зрения возникают «молнии» либо «вспышки», что свидетельствует о наличии в глазном яблоке «оптических полостей». Таким образом, мозг воспринимает аномальную реакцию зрительного нерва на присутствие пустот. Рассмотреть мутные частицы сложно, поскольку они движутся вслед за движением глаз.
Деструкция стекловидного тела может проявляться в форме «золотого» либо «серебряного дождя». Характерно для людей пожилого возраста, страдающих нарушением холестеринового обмена, а также сахарным диабетом.
Причины помутнений в стекловидном теле:
1. общие заболевания организма (Сахарный диабет; заболевания сердечно-сосудистой системы; сдавливание артериальных сосудов при наличии шейного остеохондроза; гормональные изменения, проявляющиеся во время беременности, климактерического периода, при назначении гормональной терапии; физическое истощение; психоэмоциональные стрессы),
2.
 заболевания органа зрения (близорукость, хронические воспалительные процессы в глазу, глазная мигрень),
заболевания органа зрения (близорукость, хронические воспалительные процессы в глазу, глазная мигрень),3. частые и длительные зрительные нагрузки, авитаминоз.
Как правило, это состояние не приводит к изменениям остроты зрения и не несет за собой серьезных последствий. Однако, за маской безобидного явления могут скрываться опасные для зрения состояния. Возникновение «летающих мушек» может свидетельствовать о начале процесса отслоения сетчатки, что в конечном итоге может привести к полной потере зрения. Поэтому обязательно необходим осмотр специалиста.
• проверка остроты зрения;
• составление анамнеза;
• осмотр с применением щелевой лампы
• офтальмоскопия (осмотр глазного дна)
Данные, полученные в процессе обследования, позволяют сделать вывод о наличии либо отсутствии возрастных процессов в стекловидном теле глазного яблока.
Лечение деструкции стекловидного тела глаза в большинстве случаев малоэффективно.
 Иногда незначительные помутнения и мелкие волокна могут рассосаться самостоятельно, однако крупные образования остаются до конца жизни.
Иногда незначительные помутнения и мелкие волокна могут рассосаться самостоятельно, однако крупные образования остаются до конца жизни.Вопросы о том, как лечить деструкцию стекловидного тела глаза и нужно ли это делать, решаются в каждом случае индивидуально. Необходимость и эффективность терапии зависит от степени нарушений зрительных функций, площади поражения стекловидного тела, а также влияния данных патологических факторов на состояние человека и его трудоспособность.
В настоящее время методы специфического лечения деструкции стекловидного тела, которые позволяют эффективно и безопасно устранять массивные образования, не разработаны. Основные лечебные мероприятия направлены на устранение причин, вызвавших возникновение заболевания, снижение зрительных нагрузок и применение симптоматической медикаментозной терапии.
Лечение деструкции стекловидного тела на начальных стадиях заключается в коррекции образа жизни и лечении сопутствующего общего заболевания. Рекомендовано избегать длительных зрительных нагрузок, при работе за компьютером каждый час необходимо делать перерывы, во время которых выполнять специальные упражнения для глаз.
 Для предотвращения прогрессирования патологии необходимо соблюдать режим дня, регулярно бывать на свежем воздухе, придерживаться принципов правильного питания. Стоит отметить, что при деструкции стекловидного тела можно заниматься спортом, однако предпочтение лучше отдавать видам, не требующим существенной физической активности и нагрузки.
Для предотвращения прогрессирования патологии необходимо соблюдать режим дня, регулярно бывать на свежем воздухе, придерживаться принципов правильного питания. Стоит отметить, что при деструкции стекловидного тела можно заниматься спортом, однако предпочтение лучше отдавать видам, не требующим существенной физической активности и нагрузки.• витреолизис – расщепление имеющихся в стекловидном теле помутнений с помощью YAG-лазера;
• витрэктомия – частичная либо полная замена стекловидного тела на искусственную среду (силиконовое масло, газовые пузырьки).
Использование хирургических операций в качестве способа лечения деструкции стекловидного тела имеет неоднозначный прогноз, поскольку имеется большой риск возникновения серьезных осложнений (катаракта, гипотония, отслойка сетчатки, кровоизлияния). Зачастую использование таких методов неоправданно, в первую очередь для пожилых людей, в связи с прогрессированием возрастных изменений в глазах.
Прогноз развития заболевания в большинстве случаев благоприятный. Помутнения относительно быстро стабилизируются после возникновения и развития заболевания. Проявление ослаблений данного симптома в ходе возрастных процессов наблюдается крайне редко, и плавающие помутнения остаются в полости глазного яблока.
Деструкция стекловидного тела глаза, проявляемая в легкой форме, не оказывает заметного влияния на трудоспособность человека и не является причиной возникновения серьезных осложнений. Однако развитие тяжелых форм недуга может существенно ухудшить качество жизни.
В основной массе случаев помутнения стекловидного тела не представляют опасности для зрения. Но для исключения серьезных заболеваний стекловидного тела необходим осмотр специалиста 1 раз в год.
Материал подготовлен:
врач- офтальмолог Родичкина Наталия Александровна
Лечение деструкции стекловидного тела.
 Список клиник, рейтинг, отзывы, цены
Список клиник, рейтинг, отзывы, ценыО заболевании
Деструкция стекловидного тела (отслойка стекловидного тела) – дегенеративный процесс, при котором мембрана стекловидного тела отделяется от сетчатки. Как правило, причинами развития данного заболевания являются старение или близорукость (миопия). Иногда эта патология может вызывать повреждения глазного яблока или нарушение метаболических процессов в организме. В детстве стекловидное тело прикреплено к сетчатке глаза, но с возрастом оно может отделяться от сетчатки и вызывать проблемы со зрением. Стекловидное тело представляет собой желеобразное вещество, расположенное между сетчаткой и хрусталиком глаза. Отслойка стекловидного тела возникает из-за отслойки волокнистой части сетчатки, которая состоит из связанных молекул белка. Самым распространенным осложнением данного заболевания является образование периферического разрыва сетчатки (8-15% всех случаев), отслойка стекловидного тела (редко), расслоение сетчатки (15%), кровоизлияние в стекловидное тело (13-19%, но большинство из этих осложнений не вызывают серьезного ухудшения зрения). Самым опасным осложнением является образование макулярного разрыва сетчатки.
Самым опасным осложнением является образование макулярного разрыва сетчатки.
На развитие осложнений отслойки стекловидного тела невозможно повлиять. Единственная рекомендация – поддерживать прямую связь с Вашим врачом. Таким образом, он сможет следить за процессом развития заболевания, а также сможет предпринять своевременное лечение. В 53% случаев деструкция стекловидного тела возникает у людей в возрасте старше 50 лет, а в 65% — в возрасте старше 65 лет.
Симптомы
Деструкция стекловидного тела сопровождается такими симптомами:
- Пелена перед глазами
- Черные пятна перед глазами
- Непродолжительные яркие вспышки света. Эти вспышки усиливаются, когда человек смотрит на яркие предметы
- Расплывчатое зрение, которое возникает из-за разрыва сетчатки
- Закрывая глаза, человек видит яркие плавающие предметы
- Общая раздражительность
Симптомы могут обостряться, когда человек вращает головой или резко вскакивает с кровати. Все эти симптомы свидетельствуют о том, что нужно обратиться к офтальмологу.
Все эти симптомы свидетельствуют о том, что нужно обратиться к офтальмологу.
Диагностика
Если человек видит вспышки или странную пелену перед глазами, ему нужно проконсультироваться у офтальмолога. Для осмотра стекловидного тела врач может воспользоваться каплями, которые расширяют зрачки, а для осмотра сетчатки глаза – офтальмоскопом и щелевой лампой со специальной линзой. После принятия таких капель несколько часов зрение может быть нечетким, но уже через пару часов это пройдет.
Виды лечения
- Медикаментозное лечение заключается в принятии комплексных витаминов и биостимуляторов, которые защищают глаза от последствий внутренних и внешних воздействий, а также способствуют общему улучшению состояния зрительного аппарата человека. Если в стекловидно теле из-за разрыва кровеносных сосудов скапливается или выделяется кровь, пациенту приписывают капли, которые абсорбируют кровь. Во время такого вида лечения больному назначается постельный режим на протяжении 3-4 дней, а также ему следует избегать больших физических нагрузок.

- Если деструкция стекловидного тела сопровождается отслойкой сетчатки глаза, стекловидное тело нужно полностью удалить хирургическим путем и заменить его специальным газом. Такая операция по удалению стекловидного тела называется витрэктомией. Со временем этот газ заменяется внутриглазной жидкостью. Другие вещества, которые могут заменить стекловидную мембрану, могут быть введены в глаз лишь на несколько дней или несколько лет. Такое вещество-заменитель должно обладать значительной вязкостью, высокой прозрачностью, долгосрочной резорбцией, а также не должно вызывать аллергических или воспалительных реакций. Возможно, человеку надо будет попробовать несколько веществ-заменителей, чтобы найти самое подходящее для него.
Автор: Доктор Вадим Жилюк
Причины деструкции стекловидного тела — ответ специалиста онлайн
Причины деструкции стекловидного тела
Question — answer
Может ли к деструкции стекловидного тела (летающие мушки) привести свечение яркого света в глаза? Могут ли офтальмологические исследования ухудшить ситуацию? 1)Свечение ярким светом в глаза при расширенном зрачке для исследования глазного дна. 2)УЗИ глаза. 3)ОКТ глаза (макулярной области). Может ли препарат Мильдронат также ухудшить ситуацию? Есть ли хоть какой-то способ остановить процесс деструкции?
2)УЗИ глаза. 3)ОКТ глаза (макулярной области). Может ли препарат Мильдронат также ухудшить ситуацию? Есть ли хоть какой-то способ остановить процесс деструкции?
Все исследования, названные Вами, имеют конкретные показания и противопоказания при их применении, проходят соответствующую сертификацию. Применяются только для уточнения диагноза и определения правильной тактики и динамики лечения. Милдронат считается эффективным при сосудистой и дистрофической патологии глазного дна и привести к ухудшению стекловидного тела не может. Его нельзя применять при повышении внутричерепного давления (в т.ч. при нарушении венозного оттока, внутричерепных опухолях). «Летающие мушки» — это нежные помутнения в стекловидном теле (его измененные и склеенные волокна), которые при ярком освещении отбрасывают тень на сетчатку и воспринимаются глазом как плавающие перед ним темные образования различной величины и формы (волнистые линии, пятнышки). Они наиболее четко видны при взгляде на равномерно освещенную белую поверхность (снег, светлое небо, белая стена и т.

3 December 2021, 8:55
Влияние витреоретинала на функцию хрусталика и катаракту
Philos Trans R Soc Lond B Biol Sci. 2011 Apr 27; 366 (1568): 1293–1300.
Дэвид К. Биб
1 Департамент офтальмологии и визуальных наук, Вашингтонский университет, Сент-Луис, Миссури, 63110, США
2 Департамент клеточной биологии и физиологии, Вашингтонский университет, Сент-Луис, Миссури 63110, США
Нэнси М.
 Холекамп
Холекамп2 Департамент клеточной биологии и физиологии Вашингтонского университета, Сент-Луис, Миссури, 63110, США
3 Barnes Retina Institute, Вашингтонский университет, Сент-Луис, Миссури 63110, США
Карла Зигфрид
1 Кафедра офтальмологии и визуальных наук, Вашингтонский университет, Сент-Луис, штат Миссури, 63110, США
Ин-Бо Шуй
1 Кафедра офтальмологии и визуальных наук, Вашингтонский университет, Сент-Луис, Миссури 63110, США
1 Департамент офтальмологии и визуальных наук, Вашингтонский университет, Сент-Луис, штат Миссури, 63110, США
2 Депар Центр клеточной биологии и физиологии, Вашингтонский университет, Сент-Луис, штат Миссури, 63110, США
3 Институт сетчатки Барнса, Вашингтонский университет, Сент-Луис, штат Миссури, США
Авторские права на этот журнал принадлежат © Королевское общество, 2011 другими статьями в PMC.
Abstract
Хрусталик состоит из тонкого метаболически активного внешнего слоя, состоящего из клеток эпителия и поверхностных волокон. Внутри этой внешней оболочки находятся терминально дифференцированные, метаболически неактивные клеточные волокна, которые делятся на внешнюю кору и центральное ядро. Зрелые клеточные волокна содержат очень высокую концентрацию белка, который важен для прозрачности и преломляющей силы хрусталика. Эти белки защищены от окисления восстанавливающими веществами, такими как глутатион, и средой с низким содержанием кислорода вокруг хрусталика.Глутатион достигает зрелых волоконных клеток, диффундируя из метаболически активных клеток на поверхности хрусталика. С возрастом цитоплазма ядра становится более жесткой, что снижает скорость диффузии и делает ядерные белки более восприимчивыми к окислению. Низкое pO 2 поддерживается на задней поверхности хрусталика за счет физических и физиологических свойств стекловидного тела, когда гель заполняет пространство между хрусталиком и сетчаткой. Разрушение или дегенерация стекловидного тела увеличивает воздействие кислорода сетчатки на хрусталик.Кислород достигает ядра хрусталика, увеличивая окисление и агрегацию белков и приводя к ядерной катаракте. Мы предполагаем, что поддержание низкого pO 2 вокруг хрусталика должно предотвратить образование ядерной катаракты.
Разрушение или дегенерация стекловидного тела увеличивает воздействие кислорода сетчатки на хрусталик.Кислород достигает ядра хрусталика, увеличивая окисление и агрегацию белков и приводя к ядерной катаракте. Мы предполагаем, что поддержание низкого pO 2 вокруг хрусталика должно предотвратить образование ядерной катаракты.
Ключевые слова: ядерная катаракта, окисление, кислород, стекловидное тело, аскорбиновая кислота, глутатион
1. Структура линзы и метаболизм
Хрусталик представляет собой необычную структуру, полностью состоящую из специализированных эпителиальных клеток, окруженных толстой гибкой капсулой .Тонкие фибриллы, зонулы, подвешивают хрусталик в глазу. Зонулы возникают из ресничного эпителия и вставляются в капсулу на экваторе хрусталика. Под капсулой со стороны линзы, обращенной к роговице, лежит простой кубовидный эпителий. На экваторе эти эпителиальные клетки выходят из клеточного цикла, а затем сильно удлиняются, образуя волокнистые клетки. Во время своего удлинения базальные концы волоконных клеток перемещаются по внутренней поверхности задней капсулы, а их апикальные концы проходят под передним эпителием.Удлинение приближает концы волоконных ячеек к центральной оси линзы, где они встречаются с волоконными ячейками, проходящими с противоположной стороны. У человека апикальный и базальный концы волоконных клеток встречаются вдоль трех или более плоскостей швов [1]. Во время жизни плода плоскости швов пересекаются, образуя вертикальную букву «Y» на переднем полюсе хрусталика и перевернутую букву «Y» на заднем полюсе. После рождения кончики швов раздваиваются, образуя в общей сложности шесть плоскостей швов. Позже кончик каждого шва снова раздваивается, образуя 12 швов в хрусталике взрослого человека.После того, как клетки волокна достигают швов, они перестают удлиняться и вытесняются с поверхности хрусталика клетками волокна, которые образовались сразу после них. Этот процесс, который продолжается на протяжении всей жизни, заставляет зародившиеся ранее клеточные волокна глубоко погружаться в хрусталик, при этом удлиняющиеся клеточные волокна образуют тонкую оболочку на поверхности волокнистой массы.
Во время своего удлинения базальные концы волоконных клеток перемещаются по внутренней поверхности задней капсулы, а их апикальные концы проходят под передним эпителием.Удлинение приближает концы волоконных ячеек к центральной оси линзы, где они встречаются с волоконными ячейками, проходящими с противоположной стороны. У человека апикальный и базальный концы волоконных клеток встречаются вдоль трех или более плоскостей швов [1]. Во время жизни плода плоскости швов пересекаются, образуя вертикальную букву «Y» на переднем полюсе хрусталика и перевернутую букву «Y» на заднем полюсе. После рождения кончики швов раздваиваются, образуя в общей сложности шесть плоскостей швов. Позже кончик каждого шва снова раздваивается, образуя 12 швов в хрусталике взрослого человека.После того, как клетки волокна достигают швов, они перестают удлиняться и вытесняются с поверхности хрусталика клетками волокна, которые образовались сразу после них. Этот процесс, который продолжается на протяжении всей жизни, заставляет зародившиеся ранее клеточные волокна глубоко погружаться в хрусталик, при этом удлиняющиеся клеточные волокна образуют тонкую оболочку на поверхности волокнистой массы. Вскоре после того, как они отсоединяются от капсулы, клеточные волокна завершают свою дифференцировку, разрушая все мембраносвязанные внутриклеточные органеллы, включая митохондрии и ядра [2].В этом состоянии они остаются на всю оставшуюся жизнь человека. В результате этого процесса волокнистые клетки, сформированные во время жизни плода, располагаются в середине хрусталика, составляя область, известную как ядро. Волокнистые клетки, которые дифференцируются после рождения, образуют внешнюю оболочку хрусталика взрослого человека, называемую корой.
Вскоре после того, как они отсоединяются от капсулы, клеточные волокна завершают свою дифференцировку, разрушая все мембраносвязанные внутриклеточные органеллы, включая митохондрии и ядра [2].В этом состоянии они остаются на всю оставшуюся жизнь человека. В результате этого процесса волокнистые клетки, сформированные во время жизни плода, располагаются в середине хрусталика, составляя область, известную как ядро. Волокнистые клетки, которые дифференцируются после рождения, образуют внешнюю оболочку хрусталика взрослого человека, называемую корой.
Вместе с эпителием тонкий слой ядерных волоконных клеток у поверхности хрусталика взрослого человека отвечает за большую часть его метаболической активности. Как только ядра и другие мембраносвязанные органеллы теряются в клетках волокон, их способность синтезировать белки, осуществлять окислительный метаболизм и синтезировать новые мембраны прекращается.Сообщалось, что активность лактатдегидрогеназы (ЛДГ), последнего фермента гликолитического пути, прекращается вскоре после распада органелл [3]. Если это верно, гликолитический метаболизм также прекращается вскоре после разложения органелл, поскольку ЛДГ требуется для производства NAD + , необходимого на «предшествующих» стадиях гликолиза. Даже если это не точное описание судьбы активности ЛДГ, для гликолитического метаболизма требуется согласованная активность 10 ферментов. Следовательно, можно ожидать, что гликолитическая активность будет довольно быстро снижаться в отсутствие продолжающегося синтеза белка.Таким образом, большая часть физиологических потребностей зрелых клеток коркового вещества и ядерных волокон удовлетворяется за счет тонкой оболочки поверхностных клеток с ядросодержащими волокнами. Эти потребности скромные, но критичные для прозрачности объектива. Зрелые клеточные волокна тесно связаны с метаболически активными клетками поверхностных волокон обширной сетью щелевых соединений. Небольшие молекулы, образующиеся в поверхностных клетках, могут достигать самых старых клеток ядерных волокон, распространяясь от клетки к клетке через сеть щелевых соединений.
Если это верно, гликолитический метаболизм также прекращается вскоре после разложения органелл, поскольку ЛДГ требуется для производства NAD + , необходимого на «предшествующих» стадиях гликолиза. Даже если это не точное описание судьбы активности ЛДГ, для гликолитического метаболизма требуется согласованная активность 10 ферментов. Следовательно, можно ожидать, что гликолитическая активность будет довольно быстро снижаться в отсутствие продолжающегося синтеза белка.Таким образом, большая часть физиологических потребностей зрелых клеток коркового вещества и ядерных волокон удовлетворяется за счет тонкой оболочки поверхностных клеток с ядросодержащими волокнами. Эти потребности скромные, но критичные для прозрачности объектива. Зрелые клеточные волокна тесно связаны с метаболически активными клетками поверхностных волокон обширной сетью щелевых соединений. Небольшие молекулы, образующиеся в поверхностных клетках, могут достигать самых старых клеток ядерных волокон, распространяясь от клетки к клетке через сеть щелевых соединений. Одним из наиболее важных метаболитов является глутатион-антиоксидант.
Одним из наиболее важных метаболитов является глутатион-антиоксидант.
Уровни глутатиона в клетках поверхностных волокон чрезвычайно высоки, достигая 10 мМ или более у некоторых видов [4]. Экспериментальное истощение глутатиона в интактном хрусталике приводит к быстрому образованию катаракты [5]. Градиент глутатиона присутствует в хрусталике взрослого человека с самой высокой концентрацией на поверхности хрусталика и самой низкой в ядре. Когда меченый цистеин, предшественник глутатиона, добавляется в культивируемые линзы, большая часть меченой аминокислоты попадает в линзу около экватора, а затем постепенно диффундирует в радиальном направлении к ядру [6].С возрастом уровень глутатиона снижается в ядре, но не на периферии хрусталика. Воздействие на линзы гипербарического кислорода, окислительного стресса, мало влияет на уровни глутатиона в коре головного мозга, но заметно снижает уровни глутатиона в ядре. Эти наблюдения показывают, что глутатион синтезируется в клетках поверхностных волокон и достигает ядра путем диффузии через щелевые соединения, которые соединяют соседние клетки волокон (). Воздействие на хрусталик повышенного содержания кислорода истощает глутатион в ядре, который затем должен восполняться за счет диффузии из поверхностных клеток.
Воздействие на хрусталик повышенного содержания кислорода истощает глутатион в ядре, который затем должен восполняться за счет диффузии из поверхностных клеток.
Схема, показывающая расположение зоны активного метаболизма в хрусталике (заштрихована серым). Стрелки указывают направление диффузии глутатиона (GSH) от этих активных клеток к метаболически неактивным клеткам ядра хрусталика. Когда глутатион окисляется до GSSG в ядре хрусталика, он диффундирует вниз по градиенту концентрации в противоположном направлении, к поверхности хрусталика.
Возрастное снижение концентрации ядерного глутатиона коррелирует с массивным увеличением жесткости цитоплазмы хрусталика и сопровождается значительным снижением скорости диффузии от поверхности к ядру хрусталика [7–10].Это также связано с увеличением окисленного глутатиона (GSSG) и окисленных белков хрусталика в ядре. Эта тенденция усугубляется при ядерной катаракте, которая имеет самый низкий уровень глутатиона и самый высокий уровень ядерного GSSG и окисленных белков. Ядерная катаракта также связана с дальнейшим увеличением жесткости ядерной цитоплазмы, из-за чего хирурги, специализирующиеся на лечении катаракты, называют их «ядерными склеротическими катарактами». Повышенная жесткость цитоплазмы при ядерной катаракте, вероятно, связана с повышенным сшиванием дисульфидных белков, хотя это еще предстоит напрямую продемонстрировать.Таким образом, с возрастом цитоплазма хрусталика становится жесткой, снижая скорость диффузии глутатиона от поверхности к ядру. Это увеличивает окисление в ядре, еще больше уплотняя цитоплазму. Эта петля положительной обратной связи делает ядро стареющего хрусталика особенно чувствительным к окислительному воздействию.
Ядерная катаракта также связана с дальнейшим увеличением жесткости ядерной цитоплазмы, из-за чего хирурги, специализирующиеся на лечении катаракты, называют их «ядерными склеротическими катарактами». Повышенная жесткость цитоплазмы при ядерной катаракте, вероятно, связана с повышенным сшиванием дисульфидных белков, хотя это еще предстоит напрямую продемонстрировать.Таким образом, с возрастом цитоплазма хрусталика становится жесткой, снижая скорость диффузии глутатиона от поверхности к ядру. Это увеличивает окисление в ядре, еще больше уплотняя цитоплазму. Эта петля положительной обратной связи делает ядро стареющего хрусталика особенно чувствительным к окислительному воздействию.
Следует отметить, что существует альтернативный взгляд на физиологию хрусталика, который расходится с предыдущим описанием. На основе присутствия ионных токов, измеренных вокруг внешней стороны линзы, за последние 25 лет была сформулирована гипотеза, предполагающая, что через линзу циркулирует ток жидкости [11]. Эта гипотеза предполагает, что ионы диффундируют через внеклеточное пространство к ядру и проникают в цитоплазму клеток глубоких волокон. Накопление ионов создает осмотический градиент, который втягивает воду в более глубокие клетки волокна. Затем эта жидкость вытекает из линзы от ядра к экваториальной поверхности, в основном через щелевые переходы. Предполагается, что циркуляция жидкости хрусталика удаляет продукты метаболизма и доставляет метаболические субстраты к более глубоким клеткам волокон хрусталика. Хотя циркуляция линз может быть привлекательной концепцией, она не была напрямую проверена, и ее прогнозы, похоже, противоречат опубликованным исследованиям.Например, неясно, есть ли в центре хрусталика взрослого человека гликолитический метаболизм, которому необходима эта транспортная система. Что наиболее важно, поток воды от центра к периферии линзы предотвратит диффузию глутатиона через щелевые соединения в противоположном направлении. Если модель циркуляции хрусталика верна, должен быть достаточный гликолитический метаболизм, синтез глутатиона и восстановление глутатиона для поддержания восстанавливающей среды в ядре.
Эта гипотеза предполагает, что ионы диффундируют через внеклеточное пространство к ядру и проникают в цитоплазму клеток глубоких волокон. Накопление ионов создает осмотический градиент, который втягивает воду в более глубокие клетки волокна. Затем эта жидкость вытекает из линзы от ядра к экваториальной поверхности, в основном через щелевые переходы. Предполагается, что циркуляция жидкости хрусталика удаляет продукты метаболизма и доставляет метаболические субстраты к более глубоким клеткам волокон хрусталика. Хотя циркуляция линз может быть привлекательной концепцией, она не была напрямую проверена, и ее прогнозы, похоже, противоречат опубликованным исследованиям.Например, неясно, есть ли в центре хрусталика взрослого человека гликолитический метаболизм, которому необходима эта транспортная система. Что наиболее важно, поток воды от центра к периферии линзы предотвратит диффузию глутатиона через щелевые соединения в противоположном направлении. Если модель циркуляции хрусталика верна, должен быть достаточный гликолитический метаболизм, синтез глутатиона и восстановление глутатиона для поддержания восстанавливающей среды в ядре. Тестирование этой модели ожидает доказательства того, что в ядре существует достаточный метаболизм для поддержания его восстанавливающей среды, а также прямой демонстрации того, что жидкость течет от центра хрусталика к его периферии.
Тестирование этой модели ожидает доказательства того, что в ядре существует достаточный метаболизм для поддержания его восстанавливающей среды, а также прямой демонстрации того, что жидкость течет от центра хрусталика к его периферии.
2. Кислородная токсичность
В целом, большинство из нас склонны думать о кислороде как о «хорошем», а недостаток кислорода или гипоксии — как о «плохом». дыхание. Многие патологические синдромы, которые включают системную или местную гипоксию, включая асфиксию, гипоксия-реперфузионное повреждение, респираторный дистресс-синдром недоношенных, диабетическую ретинопатию и дегенерацию желтого пятна, придают этой точке зрения значительный медицинский и научный вес.
Доказательства чувствительности хрусталика пожилого человека к вызванному кислородом повреждению были непосредственно продемонстрированы в исследовании пациентов, получавших длительную гипербарическую кислородную терапию [12]. У пациентов с тяжелым атеросклерозом часто возникают язвы на ногах из-за плохого кровоснабжения периферических тканей.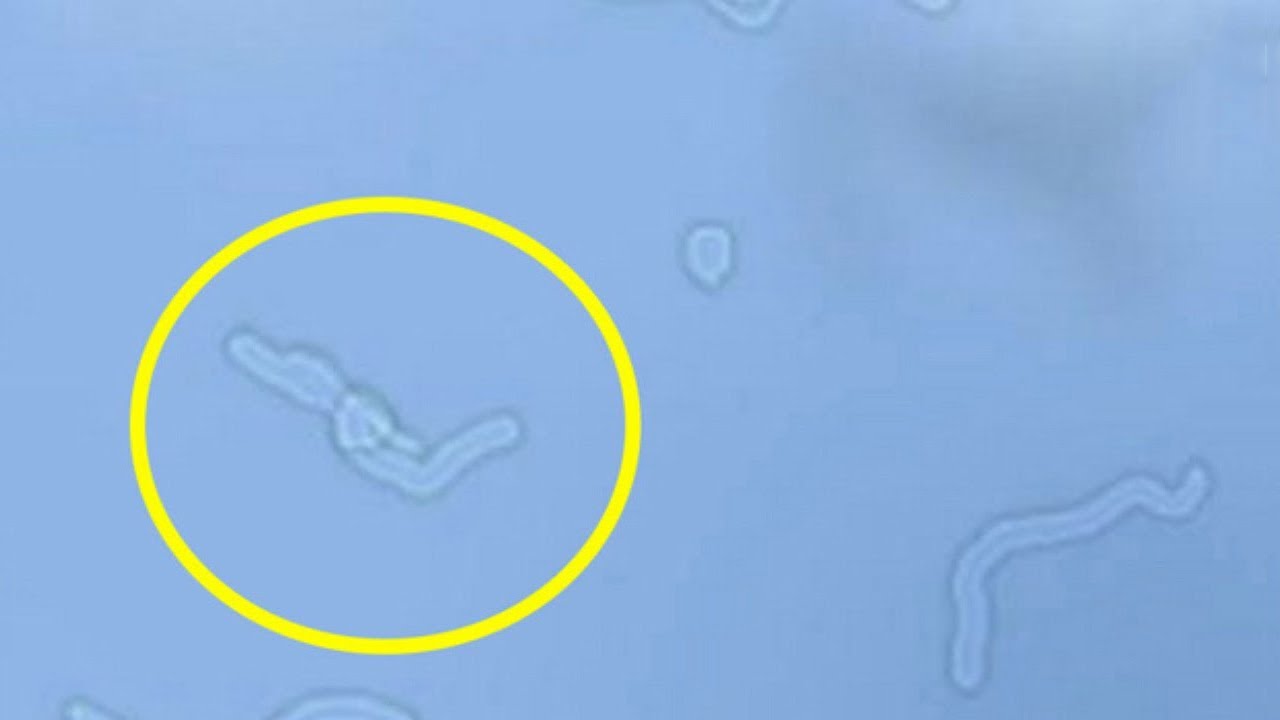 Вдыхание чистого кислорода при повышенном давлении увеличивает уровень растворенного кислорода в крови, который поставляет больше кислорода периферическим тканям и способствует заживлению язв на ногах.В этом исследовании у всех субъектов, кроме одного, развилась миопия во время лечения гипербарическим кислородом. «Миопический сдвиг» обычно предшествует возникновению ядерной катаракты. Из 15 пациентов с прозрачными линзами в начале лечения у семи развилась явная ядерная катаракта, а у семи — повышенное ядерное помутнение. Ни у одного из пациентов в нелеченой контрольной группе не развился миопический сдвиг или ядерная катаракта, хотя эти пациенты были несколько старше и имели более тяжелую периферическую ишемию.Единственному получавшему лечение субъекту, у которого не было обнаружено увеличения миопии или помутнения ядер, было 23 года, в то время как всем другим субъектам было более 40 лет. Результаты этого исследования, которые согласуются с результатами последующих испытаний на животных [13] и более краткосрочным лечением человека.
Вдыхание чистого кислорода при повышенном давлении увеличивает уровень растворенного кислорода в крови, который поставляет больше кислорода периферическим тканям и способствует заживлению язв на ногах.В этом исследовании у всех субъектов, кроме одного, развилась миопия во время лечения гипербарическим кислородом. «Миопический сдвиг» обычно предшествует возникновению ядерной катаракты. Из 15 пациентов с прозрачными линзами в начале лечения у семи развилась явная ядерная катаракта, а у семи — повышенное ядерное помутнение. Ни у одного из пациентов в нелеченой контрольной группе не развился миопический сдвиг или ядерная катаракта, хотя эти пациенты были несколько старше и имели более тяжелую периферическую ишемию.Единственному получавшему лечение субъекту, у которого не было обнаружено увеличения миопии или помутнения ядер, было 23 года, в то время как всем другим субъектам было более 40 лет. Результаты этого исследования, которые согласуются с результатами последующих испытаний на животных [13] и более краткосрочным лечением человека. испытуемые [14,15] предполагают, что воздействие на хрусталик повышенного содержания кислорода вызывает ядерную катаракту. Миопический сдвиг, наблюдаемый у всех пожилых людей, связан с увеличением преломляющей силы хрусталика, что, скорее всего, вызвано затвердением цитоплазмы хрусталика.Эти результаты согласуются с последствиями возрастной жесткости цитоплазмы хрусталика, упомянутой выше, которая может сделать линзы пожилых людей менее способными противостоять окислительному повреждению.
испытуемые [14,15] предполагают, что воздействие на хрусталик повышенного содержания кислорода вызывает ядерную катаракту. Миопический сдвиг, наблюдаемый у всех пожилых людей, связан с увеличением преломляющей силы хрусталика, что, скорее всего, вызвано затвердением цитоплазмы хрусталика.Эти результаты согласуются с последствиями возрастной жесткости цитоплазмы хрусталика, упомянутой выше, которая может сделать линзы пожилых людей менее способными противостоять окислительному повреждению.
Важно помнить, что люди и все другие организмы на Земле зависят от физиологических механизмов, которые «адаптированы» к окружающей среде, в которой парциальное давление кислорода составляет менее 21 процента. Воздействие на организмы кислорода с более высоким парциальным давлением, чем обычно встречается в их окружающей среде, имеет патологические последствия, независимо от того, рассматриваете ли вы дыхание воздуха млекопитающих или облигатных анаэробных бактерий.Для млекопитающих вредное воздействие кислорода называется кислородным отравлением. Кислородное отравление вызывает наиболее заметные повреждения легких и нервной ткани. Вредные эффекты проявляются в верхних дыхательных путях всего через 4 часа после воздействия 95% O 2 [16]. Специалисты в области терапевтического использования кислорода отмечают, что «запас прочности между эффективными и потенциально токсичными дозами кислорода относительно невелик» [16, с. 205]. Как показано выше, длительное системное воздействие гипероксии также может вызвать катаракту.
Кислородное отравление вызывает наиболее заметные повреждения легких и нервной ткани. Вредные эффекты проявляются в верхних дыхательных путях всего через 4 часа после воздействия 95% O 2 [16]. Специалисты в области терапевтического использования кислорода отмечают, что «запас прочности между эффективными и потенциально токсичными дозами кислорода относительно невелик» [16, с. 205]. Как показано выше, длительное системное воздействие гипероксии также может вызвать катаракту.
Учитывая его потенциальную токсичность, стоит подумать о том, каким образом избыток кислорода может повредить клетки. Принято считать, что большинство вредных воздействий кислорода происходит из-за избыточного производства активных форм кислорода (АФК) в условиях, когда защита от АФК недостаточна. АФК, которые обычно встречаются внутри и вокруг клеток, возникают из-за того, что кислородом один, два или три электрона восстанавливается до воды. Эти промежуточные продукты представляют собой супероксид-анион (), который является побочным продуктом нормальной митохондриальной активности, пероксид водорода (H 2 O 2 ), который образуется из O2 — под действием супероксиддисмутазы и -продукт ряда других окислительных реакций и гидроксильный радикал (HO • ) [17]. Клетки также сталкиваются с оксидом азота, пероксинитритом, гипохлоритом и другими окислительными формами, которые могут возникать в результате метаболических или патологических процессов. Защиту от АФК обеспечивают ферменты супероксиддисмутаза, каталаза и несколько пероксидаз, а также восстанавливающие агенты в цитоплазме, такие как аскорбат и глутатион. Воздействие на клетки кислорода при более высоком парциальном давлении, чем «нормальное» для этой клетки, приводит к избыточному производству АФК [17]. Если антиоксидантная защита клетки недостаточна, чтобы справиться с избытком АФК, она может окислять липиды, белки и нуклеиновые кислоты, что приводит к временному или необратимому повреждению.Когда накопленных повреждений достаточно, клетки могут подвергнуться апоптозу или некрозу [18].
Клетки также сталкиваются с оксидом азота, пероксинитритом, гипохлоритом и другими окислительными формами, которые могут возникать в результате метаболических или патологических процессов. Защиту от АФК обеспечивают ферменты супероксиддисмутаза, каталаза и несколько пероксидаз, а также восстанавливающие агенты в цитоплазме, такие как аскорбат и глутатион. Воздействие на клетки кислорода при более высоком парциальном давлении, чем «нормальное» для этой клетки, приводит к избыточному производству АФК [17]. Если антиоксидантная защита клетки недостаточна, чтобы справиться с избытком АФК, она может окислять липиды, белки и нуклеиновые кислоты, что приводит к временному или необратимому повреждению.Когда накопленных повреждений достаточно, клетки могут подвергнуться апоптозу или некрозу [18].
Важный организационный принцип в размышлениях об окислительном повреждении заключается в том, что клетки, живущие в разных средах или в разных частях тела, могут быть «адаптированы» к разным уровням кислорода. Эта концепция особенно применима к глазу. Клетки базального слоя эпителия роговицы обычно подвергаются воздействию высоких уровней кислорода, близких к pO 2 в воздухе (160 мм рт. Ст. Или 21% O 2 ).Артериальное pO 2 обычно составляет 100 мм рт. Во внутренней ткани сетчатки, рядом с внутренними сосудами сетчатки или в прилегающем стекловидном теле, pO 2 составляет примерно 20 мм рт. Ст. (Примерно 3% O 2 ) [19,20], что близко к нормальный уровень кислорода в большинстве тканей. В стекловидном теле около задней части хрусталика человека pO 2 падает примерно до 7 мм рт. передняя и боковые поверхности линзы обычно составляют около 3 мм рт.4%) [22]. Низкое содержание кислорода у поверхностей линзы и потребление кислорода клетками линзы приводит к еще более низкому pO 2 в ядре линзы [23,24]. Следовательно, клетки глаза подвергаются воздействию условий, которые для типичных клеток могут варьироваться от гипероксических до сильно гипоксических.
Эта концепция особенно применима к глазу. Клетки базального слоя эпителия роговицы обычно подвергаются воздействию высоких уровней кислорода, близких к pO 2 в воздухе (160 мм рт. Ст. Или 21% O 2 ).Артериальное pO 2 обычно составляет 100 мм рт. Во внутренней ткани сетчатки, рядом с внутренними сосудами сетчатки или в прилегающем стекловидном теле, pO 2 составляет примерно 20 мм рт. Ст. (Примерно 3% O 2 ) [19,20], что близко к нормальный уровень кислорода в большинстве тканей. В стекловидном теле около задней части хрусталика человека pO 2 падает примерно до 7 мм рт. передняя и боковые поверхности линзы обычно составляют около 3 мм рт.4%) [22]. Низкое содержание кислорода у поверхностей линзы и потребление кислорода клетками линзы приводит к еще более низкому pO 2 в ядре линзы [23,24]. Следовательно, клетки глаза подвергаются воздействию условий, которые для типичных клеток могут варьироваться от гипероксических до сильно гипоксических. Клетки эпителия роговицы, которые обычно подвергаются высокому воздействию кислорода, должны иметь защитные механизмы, снижающие выработку АФК или защищающие от АФК [25]. И наоборот, клетки, которые обычно никогда не подвергаются более 1% O 2 , с меньшей вероятностью будут противостоять вредному воздействию высокого содержания кислорода и ROS.
Клетки эпителия роговицы, которые обычно подвергаются высокому воздействию кислорода, должны иметь защитные механизмы, снижающие выработку АФК или защищающие от АФК [25]. И наоборот, клетки, которые обычно никогда не подвергаются более 1% O 2 , с меньшей вероятностью будут противостоять вредному воздействию высокого содержания кислорода и ROS.
Хотя этот сценарий, вероятно, применим к большинству клеток глаза, клетки хрусталика не являются типичными. Как указано выше, клетки около поверхности хрусталика имеют очень высокий уровень глутатиона, который является важной защитой от окислительного повреждения, а клетки хрусталика содержат много антиоксидантных ферментов [26]. Следовательно, хотя кажется, что линза подвергается воздействию относительно низкого уровня кислорода, она имеет сильную антиоксидантную защиту. Зрелые клетчатые волокна еще более атипичны. Эти клетки не имеют митохондрий, пероксисом, эндоплазматического ретикулума или других органелл, которые, как известно, генерируют АФК.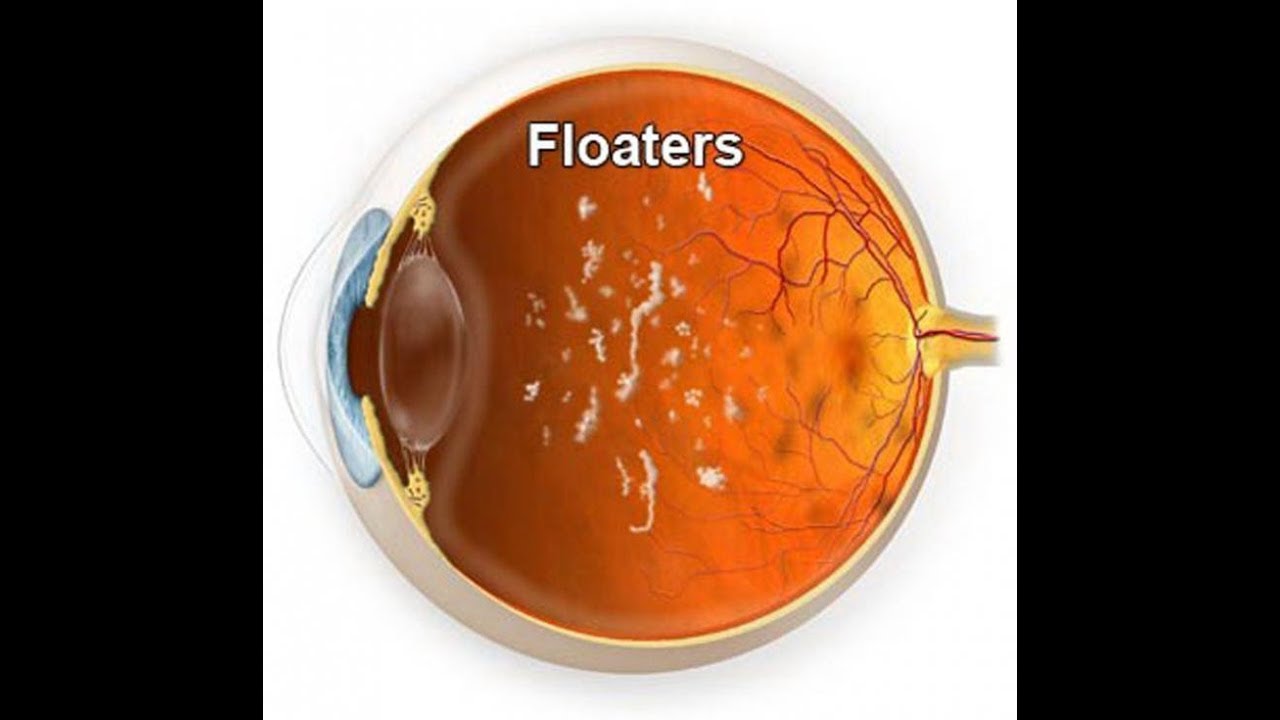 Они также находятся в среде с очень низким содержанием кислорода [24,27]. С их высоким уровнем глутатиона клетки поверхностных волокон, вероятно, наименее подвержены окислительному повреждению в организме.
Они также находятся в среде с очень низким содержанием кислорода [24,27]. С их высоким уровнем глутатиона клетки поверхностных волокон, вероятно, наименее подвержены окислительному повреждению в организме.
Если хрусталик подвергается очень низкому уровню окислительного стресса, уместно спросить, почему клетки хрусталика так хорошо защищены от окислительного повреждения. Ответ, вероятно, связан с уникальной структурой линзы. В отличие от типичных клеток, зрелые клеточные волокна существуют десятилетиями с небольшой способностью восстанавливать повреждения своих липидов или белков, и эти составляющие никогда не заменяются [28–30].Следовательно, вполне логично, что зрелые клетчатые волокна сильно защищены от окислительного повреждения. Поскольку зрелые клеточные волокна получают большую часть или всю антиоксидантную защиту от метаболически активных клеток около поверхности хрусталика, также имеет смысл, что поверхностные клетки должны иметь высокий уровень малых антиоксидантов, таких как аскорбат и глутатион, поскольку поверхностные клетки поставляют эти антиоксиданты для зрелых волокон. клетки путем простой диффузии через щелевые контакты. Таким образом, клетки в ядре хрусталика зависят от двух факторов: их прозрачность: диффузия антиоксидантов из клеток вблизи поверхности хрусталика и защита от окислителей, таких как молекулярный кислород и АФК.
клетки путем простой диффузии через щелевые контакты. Таким образом, клетки в ядре хрусталика зависят от двух факторов: их прозрачность: диффузия антиоксидантов из клеток вблизи поверхности хрусталика и защита от окислителей, таких как молекулярный кислород и АФК.
3. Механизмы, поддерживающие среду с низким содержанием кислорода вокруг и внутри линзы
(a) Распределение кислорода вокруг линзы
Тонкий волоконно-оптический датчик кислорода (оптод) использовался для картирования pO 2 в нескольких регионах передней камеры, а также в задней и стекловидном камерах пациентов, перенесших витрэктомию, операцию по удалению катаракты или глаукомы [21,22]. Кислород диффундировал из поверхностных сосудов сетчатки в стекловидное тело, достигая там парциального давления около 20 мм рт. Ст. [20,31].Однако pO 2 в задней части хрусталика человека низкое, примерно 1 процент (7 мм рт. Ст.) [21]. Измерения на животных и у пациентов, перенесших операцию витрэктомии, показывают, что потребление кислорода хрусталиком, гелевая структура стекловидного тела и реакция аскорбата (витамина С) с кислородом помогают поддерживать это низкое значение [32].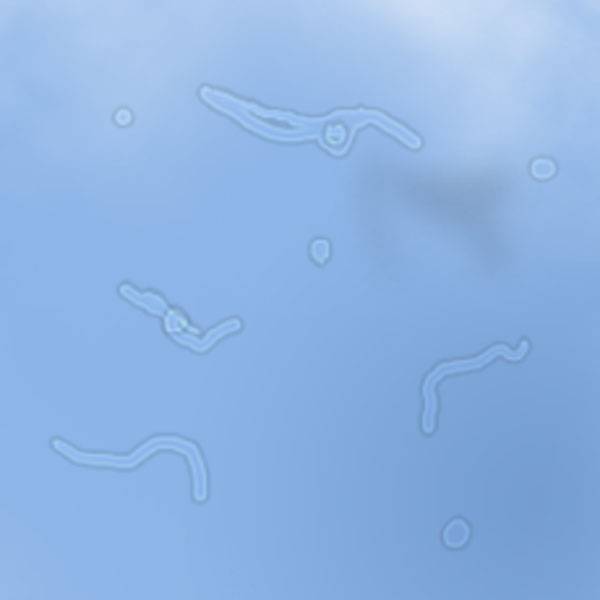
Крутой градиент кислорода также присутствует через заполненную жидкостью переднюю камеру, от ≈24 мм рт. Ст. На внутренней поверхности роговицы до ≈3 мм рт. Ст. Возле передней капсулы хрусталика [22].Поскольку роговица бессосудистая, pO 2 на ее внутренней поверхности устанавливается за счет диффузии кислорода из воздуха на внешней поверхности роговицы и потребления кислорода клетками роговицы [33]. Точно так же градиент кислорода в передней камере должен быть связан с потреблением кислорода эпителиальными клетками хрусталика и лежащими под ним клетками поверхностных волокон. Трудно сказать, повышается ли уровень кислорода перед линзой во время повседневной активности, когда водная среда может перемешиваться движениями глаз или конвективным перемешиванием.Первоначальные попытки стимулировать конвективное перемешивание путем изменения ориентации глаза кролика не вызвали заметных изменений внутриглазного распределения кислорода (C.J. Siegfried, 2010, неопубликованные данные). В любом случае окислительный метаболизм поверхностных клеток хрусталика должен гарантировать, что уровни кислорода в клетках более глубоких волокон намного ниже, чем у поверхности хрусталика. Этот прогноз подтверждается измерениями градиентов кислорода через хрусталик у кроликов [27] и в ядре хрусталика человека [24], а также гораздо более высоким pO 2 перед хрусталиком после операции по удалению катаракты и имплантации интраокулярной линзы, когда поверхностные ткани в передней части хрусталика были удалены [22].
В любом случае окислительный метаболизм поверхностных клеток хрусталика должен гарантировать, что уровни кислорода в клетках более глубоких волокон намного ниже, чем у поверхности хрусталика. Этот прогноз подтверждается измерениями градиентов кислорода через хрусталик у кроликов [27] и в ядре хрусталика человека [24], а также гораздо более высоким pO 2 перед хрусталиком после операции по удалению катаракты и имплантации интраокулярной линзы, когда поверхностные ткани в передней части хрусталика были удалены [22].
(b) Кислород и гелеобразное состояние стекловидного тела
В нормальном глазу пространство между задней поверхностью хрусталика и внутренней поверхностью сетчатки заполнено гелем, стекловидное тело. Гелевое состояние стекловидного тела гарантирует, что движение молекул внутри него происходит только за счет диффузии [34,35]. Измерения, проведенные с помощью кислородных микроэлектродов или спектроскопии ядерного магнитного резонанса, показали, что кислород диффундирует в стекловидное тело из сосудов сетчатки [19,36].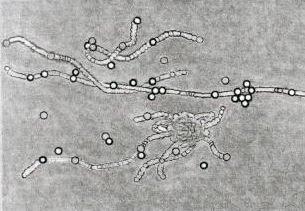
Распределение кислорода ( a ) в нормальном глазу и ( b ) после дегенерации или удаления стекловидного тела. ( a ) В глазу с неповрежденным стекловидным телом кислород диффундирует в стекловидное тело из сосудов, расположенных вблизи поверхности сетчатки.Большая часть этого кислорода потребляется тканью сетчатки, находящейся дальше от сосуда (изогнутые красные стрелки). Уровень кислорода самый низкий в центре стекловидного тела из-за реакции между аскорбатом и кислородом. ( b ) После того, как гель стекловидного тела удален во время витрэктомии или дегенерирует и отслаивается от поверхности сетчатки, большая часть полости стекловидного тела заполняется жидкостью.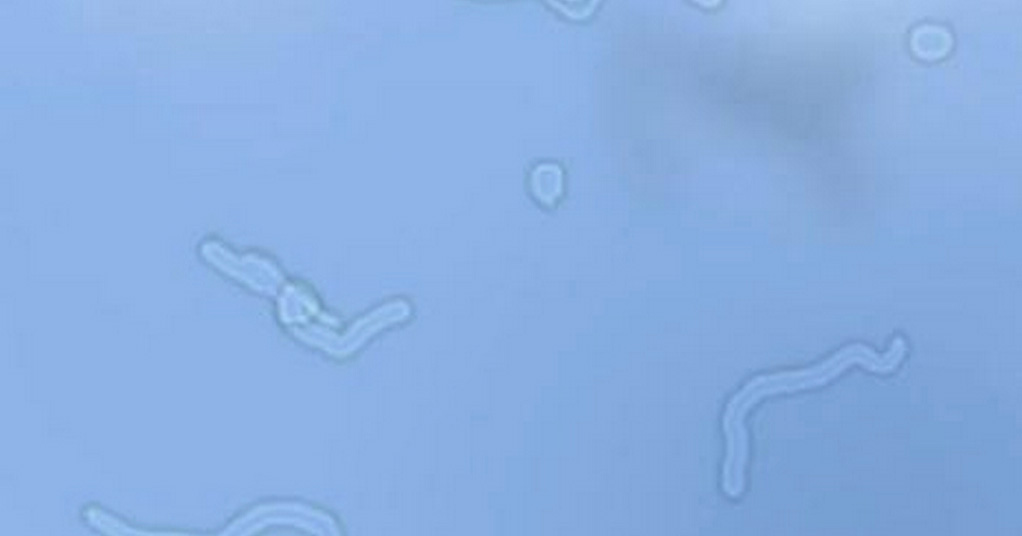 Эта жидкость легко смешивается (изогнутые черные стрелки), унося кислород от сетчатки и распределяя его по полости стекловидного тела.Смешивание увеличивает воздействие кислорода на аскорбат стекловидного тела, способствуя его окислению до дегидроаскорбат. Смешивание также доставляет больше кислорода к задней поверхности хрусталика, где он диффундирует в хрусталик, вызывая ядерную катаракту. Высокая концентрация молекул антиоксидантов, таких как глутатион, в коре хрусталика, вероятно, объясняет относительную устойчивость этой части хрусталика к окислительному повреждению.
Эта жидкость легко смешивается (изогнутые черные стрелки), унося кислород от сетчатки и распределяя его по полости стекловидного тела.Смешивание увеличивает воздействие кислорода на аскорбат стекловидного тела, способствуя его окислению до дегидроаскорбат. Смешивание также доставляет больше кислорода к задней поверхности хрусталика, где он диффундирует в хрусталик, вызывая ядерную катаракту. Высокая концентрация молекул антиоксидантов, таких как глутатион, в коре хрусталика, вероятно, объясняет относительную устойчивость этой части хрусталика к окислительному повреждению.
Первым шагом почти во всех операциях на сетчатке является удаление геля стекловидного тела и замена его сбалансированным физиологическим раствором.Поскольку гель стекловидного тела не регенерируется, витрэктомия навсегда изменяет физическое состояние материала в камере стекловидного тела. Когда гель стекловидного тела удаляется, движение головы или глаз вызывает циркуляцию и перемешивание жидкости в камере стекловидного тела [38,39].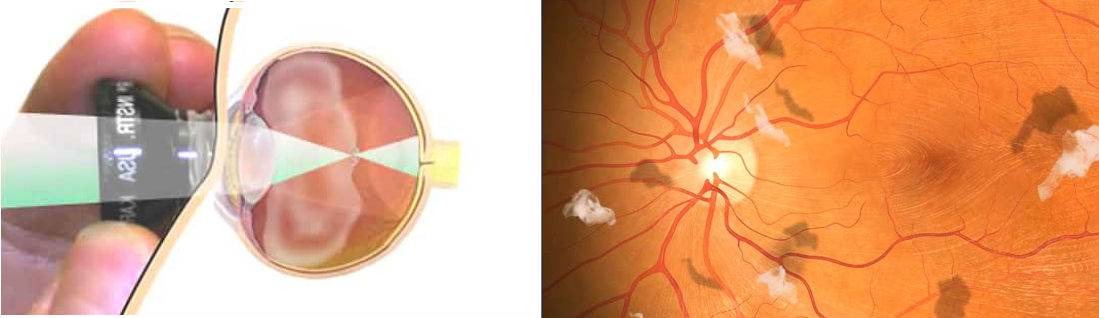 Перемешивание стекловидного тела уносит кислород от поверхности сетчатки и распределяет его по камере стекловидного тела ( b ). В соответствии с этой точкой зрения, глаза, в которых ранее была проведена витрэктомия, имели более высокий pO 2 вблизи задней поверхности хрусталика, чем глаза с неповрежденным стекловидным гелем [21].
Перемешивание стекловидного тела уносит кислород от поверхности сетчатки и распределяет его по камере стекловидного тела ( b ). В соответствии с этой точкой зрения, глаза, в которых ранее была проведена витрэктомия, имели более высокий pO 2 вблизи задней поверхности хрусталика, чем глаза с неповрежденным стекловидным гелем [21].
Гель стекловидного тела имеет тенденцию к деградации у пожилых людей. С возрастом беспорядочно ориентированные коллагеновые фибриллы в центре стекловидного тела объединяются, создавая заполненные жидкостью лакуны. По мере продолжения этого процесса лакуны сливаются, образуя более крупные заполненные жидкостью пространства, окруженные тяжами агрегированных коллагеновых фибрилл [40,41]. Продвинутая дегенерация стекловидного тела связана с усилением тракции оставшегося стекловидного тела на поверхности сетчатки. Это растяжение может повредить сетчатку, вызывая отслоение сетчатки, синдром тракции желтого пятна или отверстие желтого пятна. Коллапс стекловидного тела также увеличивает тенденцию геля стекловидного тела отделяться от поверхности сетчатки, этот процесс называется задней отслойкой стекловидного тела (PVD). После PVD оставшийся гель стекловидного тела сжимается, оставляя заполненное жидкостью пространство на поверхности сетчатки. Таким образом, дегенерация стекловидного тела является разновидностью «медленной витрэктомии».
Коллапс стекловидного тела также увеличивает тенденцию геля стекловидного тела отделяться от поверхности сетчатки, этот процесс называется задней отслойкой стекловидного тела (PVD). После PVD оставшийся гель стекловидного тела сжимается, оставляя заполненное жидкостью пространство на поверхности сетчатки. Таким образом, дегенерация стекловидного тела является разновидностью «медленной витрэктомии».
Предыдущие исследования показали, что дегенерация стекловидного тела связана с повышенным ядерным помутнением [38,42]. Состояние геля стекловидного тела не было связано с возникновением кортикальных или задних субкапсулярных помутнений, двух других основных типов возрастной катаракты.В глазах пациентов от 50 до 70 лет состояние геля стекловидного тела было более значимым предиктором помутнения ядра, чем возраст. На основании этих результатов мы предсказали, что сохранение или замена геля стекловидного тела задержит образование ядерной катаракты.
Коллагеновые фибриллы в геле стекловидного тела образованы сердцевиной из коллагена типа II, обернутой внешним слоем коллагена типа IX и типа XI [40]. Коллаген IX типа имеет концевую боковую цепь протеогликана, которая выступает из поверхности фибрилл.Группа Пола Бишопа показала, что с возрастом количество боковых цепей протеогликана экспоненциально уменьшается. Когда это произошло, большее количество внутреннего коллагена II стало доступно для антител [43]. На основе этих результатов они предположили, что постепенная потеря протеогликановых групп из коллагена стекловидного тела типа IX позволяет фибриллам коллагена агрегироваться, что способствует возрастному коллапсу геля стекловидного тела.
Коллаген IX типа имеет концевую боковую цепь протеогликана, которая выступает из поверхности фибрилл.Группа Пола Бишопа показала, что с возрастом количество боковых цепей протеогликана экспоненциально уменьшается. Когда это произошло, большее количество внутреннего коллагена II стало доступно для антител [43]. На основе этих результатов они предположили, что постепенная потеря протеогликановых групп из коллагена стекловидного тела типа IX позволяет фибриллам коллагена агрегироваться, что способствует возрастному коллапсу геля стекловидного тела.
Хотя потеря коллагена IX типа является важным наблюдением, которое помогает объяснить тенденцию геля стекловидного тела к коллапсу у пожилых людей, оно не объясняет, почему гелеобразное состояние стекловидного тела сильно различается у пациентов того же возраста.Исследования, которые измеряли степень дегенерации стекловидного тела в глазах пожилых людей, показали, что некоторые глаза в данной возрастной группе имели обширное разжижение стекловидного тела, в то время как другие имели почти неповрежденный гель стекловидного тела [32,38,44].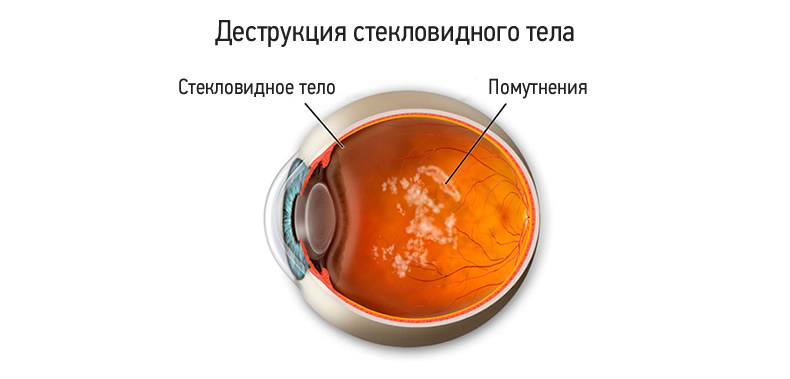 Если гелеобразное состояние стекловидного тела важно для защиты хрусталика от ядерной катаракты за счет минимизации воздействия кислорода, факторы, ответственные за разжижение стекловидного тела, являются важными факторами риска образования ядерной катаракты.
Если гелеобразное состояние стекловидного тела важно для защиты хрусталика от ядерной катаракты за счет минимизации воздействия кислорода, факторы, ответственные за разжижение стекловидного тела, являются важными факторами риска образования ядерной катаракты.
Повышенное натяжение сетчатки, вызванное дегенерацией стекловидного тела, может вызвать отслоение сетчатки или макулярное отверстие.По этой причине витреоретинальные хирурги исследовали использование ферментов для разрушения геля стекловидного тела или отделения его от поверхности сетчатки. Недавние исследования на животных показали, что ферментативное разрушение геля стекловидного тела приводит к увеличению переноса кислорода из сосудистой сети сетчатки в полость стекловидного тела и ядро хрусталика [23,45]. Следовательно, дегенерация геля стекловидного тела, как и витрэктомия, подвергает заднюю часть хрусталика и ядро хрусталика воздействию повышенного количества кислорода и увеличивает риск образования ядерной катаракты.
(c) Уровни кислорода и аскорбата в стекловидном теле
Наши предыдущие измерения распределения кислорода в стекловидном теле перед витрэктомией показали, что уровни кислорода были ниже в центральном стекловидном теле, чем за линзой [21]. После витрэктомии уровень кислорода увеличился в обоих местах, и градиент кислорода исчез. Потеря кислородного градиента соответствует перемешиванию стекловидного тела после витрэктомии.
Одно из объяснений градиента кислорода в неповрежденном геле стекловидного тела состоит в том, что стекловидное тело человека потребляет кислород.Это сделало бы уровень кислорода самым низким на самом большом расстоянии от источника кислорода, сетчатки глаза. Чтобы проверить эту возможность, мы сконструировали микрореспирометр для измерения метаболизма кислорода в небольших количествах стекловидного тела. Стекловидная жидкость, удаленная из трупных глаз или собранная у пациентов во время витрэктомии, потребляла кислород со скоростью, при которой весь кислород в образце истощался в течение 1-2 часов [32]. Мы предположили, что кислород может быть удален в результате реакции с большим количеством аскорбата (витамина С), обычно присутствующего в стекловидном теле человека [46].Воздействие на стекловидное тело аскорбата, обедненного кислородом, из стекловидного тела на 5%. Удаление аскорбата из стекловидного тела с помощью аскорбатоксидазы предотвратило потребление кислорода стекловидным телом. Эти исследования показали, что аскорбат является важным компонентом реакции стекловидного тела, потребляющего кислород. Кипячение стекловидного тела или обработка его хелатирующими средствами для меди или железа снижали скорость потребления кислорода, но менее чем на 50 процентов. Это предполагает наличие термостабильного катализатора в стекловидном теле, который отвечает за ускорение реакции между аскорбатом и кислородом [32].
Мы предположили, что кислород может быть удален в результате реакции с большим количеством аскорбата (витамина С), обычно присутствующего в стекловидном теле человека [46].Воздействие на стекловидное тело аскорбата, обедненного кислородом, из стекловидного тела на 5%. Удаление аскорбата из стекловидного тела с помощью аскорбатоксидазы предотвратило потребление кислорода стекловидным телом. Эти исследования показали, что аскорбат является важным компонентом реакции стекловидного тела, потребляющего кислород. Кипячение стекловидного тела или обработка его хелатирующими средствами для меди или железа снижали скорость потребления кислорода, но менее чем на 50 процентов. Это предполагает наличие термостабильного катализатора в стекловидном теле, который отвечает за ускорение реакции между аскорбатом и кислородом [32].
Затем мы определили уровни аскорбата и скорость потребления кислорода в образцах стекловидного тела, взятых у ряда пациентов, перенесших витрэктомию. Чтобы оценить, влияет ли разжижение стекловидного тела на концентрацию аскорбата или реакцию между аскорбатом и кислородом, была разработана субъективная система оценки состояния геля стекловидного тела. Пациенты с твердым стекловидным телом имели более высокий уровень аскорбата стекловидного тела и более высокое потребление кислорода, чем пациенты с более жидким стекловидным телом или пациенты, перенесшие ранее витрэктомию.Мы предположили, что разрушение или дегенерация геля стекловидного тела позволяет увеличить перемешивание стекловидного тела, в результате чего кислород, который диффундирует из сосудов сетчатки, смешивается с жидкостью стекловидного тела. Это усилит реакцию между аскорбатом и кислородом, истощит аскорбат в стекловидном теле и позволит большему количеству кислорода достичь хрусталика. Таким образом, относительно высокий уровень аскорбата в стекловидном теле человека (2 мМ) может помочь защитить хрусталик от воздействия кислорода.
Пациенты с твердым стекловидным телом имели более высокий уровень аскорбата стекловидного тела и более высокое потребление кислорода, чем пациенты с более жидким стекловидным телом или пациенты, перенесшие ранее витрэктомию.Мы предположили, что разрушение или дегенерация геля стекловидного тела позволяет увеличить перемешивание стекловидного тела, в результате чего кислород, который диффундирует из сосудов сетчатки, смешивается с жидкостью стекловидного тела. Это усилит реакцию между аскорбатом и кислородом, истощит аскорбат в стекловидном теле и позволит большему количеству кислорода достичь хрусталика. Таким образом, относительно высокий уровень аскорбата в стекловидном теле человека (2 мМ) может помочь защитить хрусталик от воздействия кислорода.
4. Может ли снижение содержания кислорода в стекловидном теле защитить хрусталик от ядерной катаракты?
Измерение кислорода в стекловидном теле пациентов, которым предстоит витрэктомия, показало, что у диабетиков было значительно меньше кислорода в стекловидном теле, чем у недиабетиков [47]. Основываясь на этом наблюдении, мы предположили, что диабетики будут защищены от ядерной катаракты после витрэктомии. Чтобы проверить эту возможность, мы использовали фотографию Шаймпфлюга для измерения рассеяния света в линзах согласившихся пациентов с диабетом и недиабетом до, а также через шесть и 12 месяцев после витрэктомии [48]. Рассеяние света в ядре хрусталика прооперированного глаза сравнивали с рассеянием света на неоперированном глазу. В этом исследовании диабетиков можно разделить на две группы. Многим была сделана витрэктомия из-за осложнений ишемической диабетической ретинопатии.Ишемическая диабетическая ретинопатия возникает в результате вызванного диабетом повреждения капилляров сетчатки, что приводит к ишемии тканей и разрастанию кровеносных сосудов сетчатки в стекловидное тело. Эти аномальные сосуды часто кровоточат и вызывают тракцию сетчатки, что требует витрэктомии. У других диабетиков, участвовавших в исследовании, ишемической ретинопатии не было; им делали витрэктомию по причинам, не связанным с диабетом.
Основываясь на этом наблюдении, мы предположили, что диабетики будут защищены от ядерной катаракты после витрэктомии. Чтобы проверить эту возможность, мы использовали фотографию Шаймпфлюга для измерения рассеяния света в линзах согласившихся пациентов с диабетом и недиабетом до, а также через шесть и 12 месяцев после витрэктомии [48]. Рассеяние света в ядре хрусталика прооперированного глаза сравнивали с рассеянием света на неоперированном глазу. В этом исследовании диабетиков можно разделить на две группы. Многим была сделана витрэктомия из-за осложнений ишемической диабетической ретинопатии.Ишемическая диабетическая ретинопатия возникает в результате вызванного диабетом повреждения капилляров сетчатки, что приводит к ишемии тканей и разрастанию кровеносных сосудов сетчатки в стекловидное тело. Эти аномальные сосуды часто кровоточат и вызывают тракцию сетчатки, что требует витрэктомии. У других диабетиков, участвовавших в исследовании, ишемической ретинопатии не было; им делали витрэктомию по причинам, не связанным с диабетом. У диабетиков без признаков ишемической диабетической ретинопатии ядерная катаракта после витрэктомии развивалась так же быстро, как и у недиабетиков.Пациенты с ишемической ретинопатией не показали значительного прогрессирования помутнения ядер в течение 1 года наблюдения после витрэктомии. Эти данные свидетельствуют о том, что ишемическая ретинопатия, вызванная снижением доставки кислорода к сетчатке, снижает уровень кислорода в стекловидном теле, защищая хрусталик от ядерной катаракты после витрэктомии. Более прямые проверки этой гипотезы требуют средств защиты хрусталика от воздействия кислорода после витрэктомии в глазах, которые в противном случае были бы подвержены катаракте после витрэктомии.В нашей лаборатории разрабатываются меры, позволяющие достичь этой цели.
У диабетиков без признаков ишемической диабетической ретинопатии ядерная катаракта после витрэктомии развивалась так же быстро, как и у недиабетиков.Пациенты с ишемической ретинопатией не показали значительного прогрессирования помутнения ядер в течение 1 года наблюдения после витрэктомии. Эти данные свидетельствуют о том, что ишемическая ретинопатия, вызванная снижением доставки кислорода к сетчатке, снижает уровень кислорода в стекловидном теле, защищая хрусталик от ядерной катаракты после витрэктомии. Более прямые проверки этой гипотезы требуют средств защиты хрусталика от воздействия кислорода после витрэктомии в глазах, которые в противном случае были бы подвержены катаракте после витрэктомии.В нашей лаборатории разрабатываются меры, позволяющие достичь этой цели.
В исследовании, описанном выше, ишемическая диабетическая ретинопатия была связана с более низкой ядерной помутнением на исходном уровне в прооперированных и других неоперированных глазах. Одним из объяснений этого результата является то, что низкий уровень кислорода в глазу у больных ишемическим диабетом защищает хрусталик от нормального возрастного развития помутнения ядер. Если эта интерпретация верна, то можно предположить, что терапия, снижающая содержание кислорода в стекловидном теле, замедлит или предотвратит помутнение ядра, которое происходит у каждого человека с возрастом.Хотя это захватывающая возможность, следует рассмотреть по крайней мере одно альтернативное объяснение.
Если эта интерпретация верна, то можно предположить, что терапия, снижающая содержание кислорода в стекловидном теле, замедлит или предотвратит помутнение ядра, которое происходит у каждого человека с возрастом.Хотя это захватывающая возможность, следует рассмотреть по крайней мере одно альтернативное объяснение.
Ранее мы показали, что дегенерация стекловидного тела является важным фактором риска помутнения ядер [38]. Дегенерация стекловидного тела также является основной причиной отслоения сетчатки, макулярного отверстия, синдрома витреомакулярной тракции и других проблем сетчатки. Большинству пациентов с диабетом, не страдающих диабетом и не ишемическим диабетом, в нашем исследовании была проведена витрэктомия по поводу одного из состояний сетчатки, связанных с дегенерацией стекловидного тела.Следовательно, некоторая часть помутнения ядра, обнаруженная на исходном уровне в этой группе, вероятно, была следствием повышенного воздействия кислорода, вызванного возрастной дегенерацией стекловидного тела. Было высказано предположение, что диабет может вызывать раннюю дегенерацию стекловидного тела [49], но другие исследования показали обратное [50]. Если ишемическая диабетическая ретинопатия не связана с ранней дегенерацией стекловидного тела, у больных ишемическим диабетом дегенерация стекловидного тела может быть меньше, чем у тех, кто перенес операцию по поводу других заболеваний сетчатки.Более неповрежденный гель стекловидного тела, возможно, способствовал более низкой ядерной непрозрачности, наблюдаемой в их линзах на исходном уровне. В любом случае наши результаты предполагают, что сохранение структуры стекловидного тела защищает хрусталик от ядерной катаракты, а в отсутствие геля стекловидного тела пониженное содержание кислорода в стекловидном теле может защитить от образования ядерной катаракты.
Было высказано предположение, что диабет может вызывать раннюю дегенерацию стекловидного тела [49], но другие исследования показали обратное [50]. Если ишемическая диабетическая ретинопатия не связана с ранней дегенерацией стекловидного тела, у больных ишемическим диабетом дегенерация стекловидного тела может быть меньше, чем у тех, кто перенес операцию по поводу других заболеваний сетчатки.Более неповрежденный гель стекловидного тела, возможно, способствовал более низкой ядерной непрозрачности, наблюдаемой в их линзах на исходном уровне. В любом случае наши результаты предполагают, что сохранение структуры стекловидного тела защищает хрусталик от ядерной катаракты, а в отсутствие геля стекловидного тела пониженное содержание кислорода в стекловидном теле может защитить от образования ядерной катаракты.
5. Резюме
Линза представляет собой необычную структуру в необычных условиях. Метаболически активные клетки в тонкой зоне на поверхности хрусталика поставляют важные восстанавливающие вещества, особенно глутатион, метаболически инертным зрелым клеткам волокна в более глубоких слоях хрусталика. С возрастом цитоплазма в более глубоких слоях хрусталика человека становится более жесткой. Это замедляет диффузию глутатиона от поверхностных клеток к ядру хрусталика и GSSG от ядра к поверхностным клеткам. Эти изменения делают ядро старого хрусталика человека более восприимчивым к окислительному повреждению. Хрусталик защищен от окислительного повреждения, потому что он имеет низкий окислительный метаболизм и существует в среде с низким содержанием кислорода. Кроме того, поверхностные клетки, особенно клетки эпителия, потребляют большую часть кислорода, воздействию которого подвергается хрусталик.Гель стекловидного тела защищает заднюю часть хрусталика от воздействия кислорода сосудов сетчатки. Утрата гелевой структуры стекловидного тела вследствие возрастной дегенерации или витрэктомии увеличивает перемешивание стекловидного тела. Смешивание доставляет в хрусталик больше кислорода, что приводит к образованию ядерной катаракты. Пациенты с ишемической диабетической ретинопатией имеют более низкий уровень кислорода в стекловидном теле и, по крайней мере, частично защищены от ядерной катаракты в течение первого года после витрэктомии.
С возрастом цитоплазма в более глубоких слоях хрусталика человека становится более жесткой. Это замедляет диффузию глутатиона от поверхностных клеток к ядру хрусталика и GSSG от ядра к поверхностным клеткам. Эти изменения делают ядро старого хрусталика человека более восприимчивым к окислительному повреждению. Хрусталик защищен от окислительного повреждения, потому что он имеет низкий окислительный метаболизм и существует в среде с низким содержанием кислорода. Кроме того, поверхностные клетки, особенно клетки эпителия, потребляют большую часть кислорода, воздействию которого подвергается хрусталик.Гель стекловидного тела защищает заднюю часть хрусталика от воздействия кислорода сосудов сетчатки. Утрата гелевой структуры стекловидного тела вследствие возрастной дегенерации или витрэктомии увеличивает перемешивание стекловидного тела. Смешивание доставляет в хрусталик больше кислорода, что приводит к образованию ядерной катаракты. Пациенты с ишемической диабетической ретинопатией имеют более низкий уровень кислорода в стекловидном теле и, по крайней мере, частично защищены от ядерной катаракты в течение первого года после витрэктомии. Терапевтические стратегии, которые снижают уровень кислорода вокруг хрусталика или защищают хрусталик от воздействия повышенного количества кислорода из сетчатки, могут замедлить или предотвратить образование ядерной катаракты.
Терапевтические стратегии, которые снижают уровень кислорода вокруг хрусталика или защищают хрусталик от воздействия повышенного количества кислорода из сетчатки, могут замедлить или предотвратить образование ядерной катаракты.
Ссылки
3. Пау Х., Хартвиг Х.-Г., Фассбендер Р. 1997. Топографическое распределение активности лактатдегидрогеназы в прозрачных линзах глаза человека и в линзах с различными типами старческой катаракты: гистохимическое исследование. Арка Грефе. Clin. Exp. Офтальмол. 235, 611–61710.1007 / BF00946936 (DOI: 10.1007 / BF00946936) [PubMed] [CrossRef] [Google Scholar] 5. Кальвин Х., Медведовский С., Дэвид Дж., Броглио Т., Хесс Дж., Фу С., Воргул Б. В. 1991. Быстрое разрушение волокон хрусталика у детенышей мышей с обедненным GSH. Инвестируйте офтальмол. Vis. Sci. 32, 1916–1924 [PubMed] [Google Scholar] 9. Хейс К. Р., Крам С. Л., Траскотт Р. Дж. 2004. Сильное увеличение жесткости ядра хрусталика человека с возрастом: основа пресбиопии? Мол. Vis. 10, 956–963 [PubMed] [Google Scholar] 13. Гиблин Ф. Дж., Падгаонкар В. А., Леверенц В.Р., Лин Л. Р., Лу М. Ф., Унакар Н. Дж., Данг Л., Дикерсонджр Дж., Редди В. 1995. Ядерное рассеяние света, образование дисульфидов и повреждение мембран в хрусталиках старых морских свинок, обработанных гипербарическим кислородом. Exp. Eye Res. 60, 219–23510.1016 / S0014-4835 (05) 80105-8 (doi: 10.1016 / S0014-4835 (05) 80105-8) [PubMed] [CrossRef] [Google Scholar] 14. Эвангер К., Хауген О. Х., Иргенс А., Аандеруд Л., Торсен Э. 2004. Изменения рефракции глаз у пациентов, получающих гипербарический кислород, вводимый через ороназальную маску или капюшон.Acta Ophthalmol. Сканд. 82, 449–45310.1111 / j.1395-3907.2004.00290.x (doi: 10.1111 / j.1395-3907.2004.00290.x) [PubMed] [CrossRef] [Google Scholar] 17. Фридович И. 1998. Кислородное отравление: радикальное объяснение. J. Exp. Биол. 201, 1203–1209 [PubMed] [Google Scholar] 18. Спектор А., Ван Г. М., Ван Р. Р., Ли В. К., Клейман Н. Дж. 1995. Кратковременное фотохимическое окислительное повреждение вызывает необратимое повреждение хрусталика и катаракту.
Гиблин Ф. Дж., Падгаонкар В. А., Леверенц В.Р., Лин Л. Р., Лу М. Ф., Унакар Н. Дж., Данг Л., Дикерсонджр Дж., Редди В. 1995. Ядерное рассеяние света, образование дисульфидов и повреждение мембран в хрусталиках старых морских свинок, обработанных гипербарическим кислородом. Exp. Eye Res. 60, 219–23510.1016 / S0014-4835 (05) 80105-8 (doi: 10.1016 / S0014-4835 (05) 80105-8) [PubMed] [CrossRef] [Google Scholar] 14. Эвангер К., Хауген О. Х., Иргенс А., Аандеруд Л., Торсен Э. 2004. Изменения рефракции глаз у пациентов, получающих гипербарический кислород, вводимый через ороназальную маску или капюшон.Acta Ophthalmol. Сканд. 82, 449–45310.1111 / j.1395-3907.2004.00290.x (doi: 10.1111 / j.1395-3907.2004.00290.x) [PubMed] [CrossRef] [Google Scholar] 17. Фридович И. 1998. Кислородное отравление: радикальное объяснение. J. Exp. Биол. 201, 1203–1209 [PubMed] [Google Scholar] 18. Спектор А., Ван Г. М., Ван Р. Р., Ли В. К., Клейман Н. Дж. 1995. Кратковременное фотохимическое окислительное повреждение вызывает необратимое повреждение хрусталика и катаракту. II. Механизм действия. Exp. Eye Res. 60, 483–49310.1016 / S0014-4835 (05) 80063-6 (DOI: 10.1016 / S0014-4835 (05) 80063-6) [PubMed] [CrossRef] [Google Scholar] 20. Сакауэ Х., Цукахара Ю., Неги А., Огино Н., Хонда Ю. 1989. Измерение напряжения кислорода стекловидного тела в глазах человека. Jpn J. Ophthalmol. 33, 199–203 [PubMed] [Google Scholar] 21. Холекамп Н. М., Шуй Ю. Б., Биб Д. С. 2005. Операция по витрэктомии увеличивает воздействие кислорода на хрусталик: возможный механизм образования ядерной катаракты. Являюсь. J. Ophthalmol. 139, 302–31010.1016 / j.ajo.2004.09.046 (doi: 10.1016 / j.ajo.2004.09.046) [PubMed] [CrossRef] [Google Scholar] 24.МакНалти Р., Ван Х., Матиас Р. Т., Ортверт Б. Дж., Траскотт Р. Дж. У., Басснетт С. 2004. Регулирование уровня кислорода в тканях в хрусталике млекопитающих. J. Physiol. (Лондон). 559, 883–898 [Бесплатная статья PMC] [PubMed] [Google Scholar] 28. Cenedella R. 1989. Старение и скорость дифференцировки клеток хрусталика in vivo, измеренные химическим методом.
II. Механизм действия. Exp. Eye Res. 60, 483–49310.1016 / S0014-4835 (05) 80063-6 (DOI: 10.1016 / S0014-4835 (05) 80063-6) [PubMed] [CrossRef] [Google Scholar] 20. Сакауэ Х., Цукахара Ю., Неги А., Огино Н., Хонда Ю. 1989. Измерение напряжения кислорода стекловидного тела в глазах человека. Jpn J. Ophthalmol. 33, 199–203 [PubMed] [Google Scholar] 21. Холекамп Н. М., Шуй Ю. Б., Биб Д. С. 2005. Операция по витрэктомии увеличивает воздействие кислорода на хрусталик: возможный механизм образования ядерной катаракты. Являюсь. J. Ophthalmol. 139, 302–31010.1016 / j.ajo.2004.09.046 (doi: 10.1016 / j.ajo.2004.09.046) [PubMed] [CrossRef] [Google Scholar] 24.МакНалти Р., Ван Х., Матиас Р. Т., Ортверт Б. Дж., Траскотт Р. Дж. У., Басснетт С. 2004. Регулирование уровня кислорода в тканях в хрусталике млекопитающих. J. Physiol. (Лондон). 559, 883–898 [Бесплатная статья PMC] [PubMed] [Google Scholar] 28. Cenedella R. 1989. Старение и скорость дифференцировки клеток хрусталика in vivo, измеренные химическим методом. Вкладывать деньги. Офтальмол. Vis. Sci. 30, 575–579 [PubMed] [Google Scholar] 29. Cenedella R. J. 1995. Роль транскрипции, трансляции и белкового обмена в контроле распределения 3-гидрокси-3-метилглутарил-кофермента А-редуктазы в хрусталике.Вкладывать деньги. Офтальмол. Vis. Sci. 36, 2133–2141 [PubMed] [Google Scholar] 31. Берковиц Б. А., Уилсон С. А., Хатчелл Д. Л., Лондон Р. Э. 1991. Количественное определение парциального давления кислорода в витрэктомизированном глазу кролика in vivo с использованием 19F ЯМР [опубликованная ошибка появляется в Magn. Резон. Med. 1991, 22 , 512]. Magn. Резон. Med. 21, 233–24110.1002 / mrm.1910210208 (doi: 10.1002 / mrm.1910210208) [PubMed] [CrossRef] [Google Scholar] 33. Бонанно Дж. А., Стикель Т., Нгуен Т., Биль Т., Картер Д., Бенджамин В. Дж., Сони П. С. 2002. Оценка потребления кислорода роговицей человека путем неинвазивного измерения давления кислорода в слезе при ношении гидрогелевых линз. Вкладывать деньги.
Вкладывать деньги. Офтальмол. Vis. Sci. 30, 575–579 [PubMed] [Google Scholar] 29. Cenedella R. J. 1995. Роль транскрипции, трансляции и белкового обмена в контроле распределения 3-гидрокси-3-метилглутарил-кофермента А-редуктазы в хрусталике.Вкладывать деньги. Офтальмол. Vis. Sci. 36, 2133–2141 [PubMed] [Google Scholar] 31. Берковиц Б. А., Уилсон С. А., Хатчелл Д. Л., Лондон Р. Э. 1991. Количественное определение парциального давления кислорода в витрэктомизированном глазу кролика in vivo с использованием 19F ЯМР [опубликованная ошибка появляется в Magn. Резон. Med. 1991, 22 , 512]. Magn. Резон. Med. 21, 233–24110.1002 / mrm.1910210208 (doi: 10.1002 / mrm.1910210208) [PubMed] [CrossRef] [Google Scholar] 33. Бонанно Дж. А., Стикель Т., Нгуен Т., Биль Т., Картер Д., Бенджамин В. Дж., Сони П. С. 2002. Оценка потребления кислорода роговицей человека путем неинвазивного измерения давления кислорода в слезе при ношении гидрогелевых линз. Вкладывать деньги. Офтальмол. Vis. Sci. 43, 371–376 [PubMed] [Google Scholar] 38. Харокопос Дж. Дж., Шуй Й.-Б., Маккиннон М., Холекамп Н. М., Гордон М. О., Биби Д. С. 2004. Важность разжижения стекловидного тела при возрастной катаракте. Вкладывать деньги. Офтальмол. Vis. Sci. 45, 77–8510.1167 / iovs.03-0820 (doi: 10.1167 / iovs.03-0820) [PubMed] [CrossRef] [Google Scholar] 42.Розен Э. 1962. Отслойка стекловидного тела, связанная с ядерным склерозом. Являюсь. J. Ophthalmol. 54, 837–841 [PubMed] [Google Scholar] 43. Бишоп П. Н., Холмс Д. Ф., Кадлер К. Э., МакЛеод Д., Бос К. Дж. 2004. Возрастные изменения на поверхности коллагеновых фибрилл стекловидного тела. Вкладывать деньги. Офтальмол. Vis. Sci. 45, 1041–104610.1167 / iovs.03-1017 (doi: 10.1167 / iovs.03-1017) [PubMed] [CrossRef] [Google Scholar] 44. О’Мэлли П. 1976. Характер синерезиса стекловидного тела. Исследование 800 вскрытых глаз. В достижениях в хирургии стекловидного тела (ред. Ирвин А.Р., О’Мэлли К.), стр. 17–33, Спрингфилд, Иллинойс: Томас [Google Scholar] 47.
Офтальмол. Vis. Sci. 43, 371–376 [PubMed] [Google Scholar] 38. Харокопос Дж. Дж., Шуй Й.-Б., Маккиннон М., Холекамп Н. М., Гордон М. О., Биби Д. С. 2004. Важность разжижения стекловидного тела при возрастной катаракте. Вкладывать деньги. Офтальмол. Vis. Sci. 45, 77–8510.1167 / iovs.03-0820 (doi: 10.1167 / iovs.03-0820) [PubMed] [CrossRef] [Google Scholar] 42.Розен Э. 1962. Отслойка стекловидного тела, связанная с ядерным склерозом. Являюсь. J. Ophthalmol. 54, 837–841 [PubMed] [Google Scholar] 43. Бишоп П. Н., Холмс Д. Ф., Кадлер К. Э., МакЛеод Д., Бос К. Дж. 2004. Возрастные изменения на поверхности коллагеновых фибрилл стекловидного тела. Вкладывать деньги. Офтальмол. Vis. Sci. 45, 1041–104610.1167 / iovs.03-1017 (doi: 10.1167 / iovs.03-1017) [PubMed] [CrossRef] [Google Scholar] 44. О’Мэлли П. 1976. Характер синерезиса стекловидного тела. Исследование 800 вскрытых глаз. В достижениях в хирургии стекловидного тела (ред. Ирвин А.Р., О’Мэлли К.), стр. 17–33, Спрингфилд, Иллинойс: Томас [Google Scholar] 47. Холекамп Н. М., Шуй Ю.-Б., Бибе Д. 2006. Более низкое внутриглазное давление кислорода у пациентов с диабетом: возможный вклад в снижение частоты ядерной склеротической катаракты. Являюсь. J. Ophthalmol. 141, 1027–103210.1016 / j.ajo.2006.01.016 (doi: 10.1016 / j.ajo.2006.01.016) [PubMed] [CrossRef] [Google Scholar]
Холекамп Н. М., Шуй Ю.-Б., Бибе Д. 2006. Более низкое внутриглазное давление кислорода у пациентов с диабетом: возможный вклад в снижение частоты ядерной склеротической катаракты. Являюсь. J. Ophthalmol. 141, 1027–103210.1016 / j.ajo.2006.01.016 (doi: 10.1016 / j.ajo.2006.01.016) [PubMed] [CrossRef] [Google Scholar]Повреждения диска зрительного нерва, фовеаля и экстрафовеальной области вследствие хирургического отделения стекловидное тело | Нейроофтальмология | JAMA Офтальмология
Цель Оценить морфологические результаты хирургического витреоретинального разделения у молодых взрослых приматов.
Материалы и методы Витрэктомия и механическое отделение стекловидного тела от внутренней ограничивающей пластинки (ILL) задней сетчатки и поверхности диска зрительного нерва были выполнены на 25 глазах молодых взрослых особей яванского макака in vivo. Гистохимические исследования лектина использовали для оценки витреоретинального интерфейса. Морфологические исходы сведены в таблицу.
Морфологические исходы сведены в таблицу.
Результаты В 11 из 25 областей глаза остаточное стекловидное тело оставалось прикрепленным к ILL в некоторых областях.Локализованные разрывы ILL или отделение ILL от нейральной сетчатки были отмечены в 9 глазах. Утрата ткани сетчатки, включая отрыв ганглиозных клеток, внутреннего плексиформного или внутреннего ядерного слоев, наблюдалась на 7 глазах. Отрыв пучков аксонов в диске зрительного нерва отмечен в 9 глазах. Примечательно, что частичные или полные фовеальные разрывы были отмечены в 11 глазах. По данным интраоперационных наблюдений хирургов, небольшие поверхностные кровоизлияния в диск зрительного нерва или сетчатки наблюдались в 3 из 25 глаз. Ни на одном из глаз, на которых выполнялась только витрэктомия, не было выявлено повреждения ILL или потери ткани сетчатки или диска зрительного нерва.
Заключение Повреждение диска зрительного нерва, ямки и экстрафовеальной сетчатки может возникнуть в результате хирургического отделения стекловидного тела от сетчатки у молодых взрослых приматов.
Клиническая значимость Эти данные подтверждают мнение о том, что хирургически индуцированное повреждение на уровне витреоретинального интерфейса может помочь объяснить дефекты поля зрения, отмеченные после операции по закрытию полных макулярных отверстий. Эти данные также подтверждают необходимость разработки дополнительных методов, способствующих разделению стекловидного тела, тем самым снижая риск травматических осложнений, связанных с чисто механическими процедурами.
ЖИВОЕ тело — это соединительная ткань, занимающая примерно 80% объема глаза и обеспечивающая структурную и метаболическую поддержку тканей глаза. Стекловидное тело представляет собой полутвердый прозрачный гель, состоящий в основном из воды. Примерно 1% этого геля состоит из других компонентов, включая коллаген и гиалуроновую кислоту. 1 Самое сильное прилегание стекловидного тела к сетчатке происходит в основании стекловидного тела. 1 Другие области прочного витреоретинального прикрепления включают перипапиллярную область около диска зрительного нерва, заднюю часть стекловидного тела, связанную с ямкой, и области вдоль основных сосудов сетчатки. Молекулярные основы витреоретинальной адгезии не выяснены. Однако 2 хондроитинсульфатных протеогликана, каждый с молекулярной массой примерно 240 кДа, были выделены из витреоретинальной границы раздела стекловидного тела, где они, как предполагается, участвуют в адгезии стекловидного тела нервной сетчатки (GSH и SRR, неопубликованные данные, 1994 г.).
Молекулярные основы витреоретинальной адгезии не выяснены. Однако 2 хондроитинсульфатных протеогликана, каждый с молекулярной массой примерно 240 кДа, были выделены из витреоретинальной границы раздела стекловидного тела, где они, как предполагается, участвуют в адгезии стекловидного тела нервной сетчатки (GSH и SRR, неопубликованные данные, 1994 г.).
Современные методы лечения макулярных отверстий, отслоения сетчатки и многих других витреоретинальных аномалий основаны на предпосылке, что тракция, опосредованная корой стекловидного тела, является непосредственной причиной визуально угрожающего заболевания.По некоторым хирургическим показаниям выполняется или рекомендуется механическое удаление коры стекловидного тела. 2 , 3 Хирургические процедуры для лечения идиопатических 2 , 4 -6 и травматических 7 , 8 полных макулярных отверстий включали удаление заднего гиалоида из макулярных отверстий и задние поверхности сетчатки. По мере того, как все большее число пациентов подвергаются хирургическим процедурам для закрытия макулярных отверстий, сообщается о таких осложнениях, как глубокие дефекты поля зрения. 9 , 10 Споры относительно причины этих дефектов поля зрения существуют. Однако вероятной причиной может быть механическое повреждение внутренней сетчатки в результате процедуры.
По мере того, как все большее число пациентов подвергаются хирургическим процедурам для закрытия макулярных отверстий, сообщается о таких осложнениях, как глубокие дефекты поля зрения. 9 , 10 Споры относительно причины этих дефектов поля зрения существуют. Однако вероятной причиной может быть механическое повреждение внутренней сетчатки в результате процедуры.
В рамках продолжающегося исследования с целью выяснения молекулярных основ витреоретинальной адгезии и разработки стратегий фармакологического нарушения витреоретинальной адгезии, мы провели несколько контрольных экспериментов для определения немедленных и долгосрочных эффектов хирургического отделения кортикального слоя стекловидного тела от внутреннего. ограничивающая пластинка (ILL) у молодых взрослых приматов.Здесь мы сообщаем об осложнениях и степени полноты хирургической дезинсекции стекловидного тела. Наши данные, которые демонстрируют значительное повреждение внутренней сетчатки, желтого пятна и зрительного нерва, подтверждают мнение о том, что хирургическое отделение стекловидного тела от ILL может объяснить некоторые случаи, в которых в результате этих хирургических вмешательств возникают глубокие дефекты поля зрения. Результаты показывают, что ферментативные или другие немеханические методы отделения коры стекловидного тела от ILL могут привести к снижению операционного риска и улучшению результатов.
Результаты показывают, что ферментативные или другие немеханические методы отделения коры стекловидного тела от ILL могут привести к снижению операционного риска и улучшению результатов.
Хирургическая процедура и ткани
Двадцать пять экспериментальных и 5 контрольных (имитационных) процедур были выполнены на 17 обезьянах яванского макака в возрасте от 6 до 10 лет. Обезьян Cynomolgus помещали в сжимающую клетку и вводили в бедро 0,7 мл гидрохлорида кетамина (Ketaset, 100 мг / мл; AVECO Inc; Форт-Додж, штат Айова), чтобы вызвать седативный эффект.Впоследствии обезьян перевезли в операционную. Маскирующая анестезия с использованием от 1% до 5% изофлорана (Forane; Baxter PPI, Liberty Corner, NJ) применялась до достижения мышечной релаксации. Впоследствии обезьян интубировали с помощью эндотрахеальной трубки диаметром 3 мм. После проверки положения трубки и регулировки расширяемой эндотрахеальной манжеты обезьян помещали на обогревающее одеяло, чтобы поддерживать температуру их тела на протяжении всей процедуры. Были наложены прекардиальные электрокардиографические электроды и манжета для измерения кровяного давления, а жизненные показатели контролировались каждые 15 минут на протяжении всей процедуры.Внутривенный катетер калибра 20 вводили в заднюю большеберцовую вену и вводили 0,9% стерильный изотонический раствор хлорида натрия со скоростью 30 мл / ч. Шеи обезьян были чрезмерно вытянуты, чтобы обеспечить адекватную верхнюю витрэктомию. Боковые тарсоррафии были выполнены, чтобы обеспечить адекватный доступ к глазному яблоку, и места склеротомии были размещены на 2,25 мм кзади от нижне-височного лимба. Канюли диаметром 2,5 мм были вшиты на место полигалактиновым швом 5-0 (Викрил). Были расположены дополнительные участки склеротомии 2.25 мм кзади от лимба, в надвисочном и нижневисочном квадрантах. Резак стекловидного тела вводили через участок надвисочной склеротомии, а оптоволоконный осветитель вводили через участок надоназальной склеротомии.
После проверки положения трубки и регулировки расширяемой эндотрахеальной манжеты обезьян помещали на обогревающее одеяло, чтобы поддерживать температуру их тела на протяжении всей процедуры. Были наложены прекардиальные электрокардиографические электроды и манжета для измерения кровяного давления, а жизненные показатели контролировались каждые 15 минут на протяжении всей процедуры.Внутривенный катетер калибра 20 вводили в заднюю большеберцовую вену и вводили 0,9% стерильный изотонический раствор хлорида натрия со скоростью 30 мл / ч. Шеи обезьян были чрезмерно вытянуты, чтобы обеспечить адекватную верхнюю витрэктомию. Боковые тарсоррафии были выполнены, чтобы обеспечить адекватный доступ к глазному яблоку, и места склеротомии были размещены на 2,25 мм кзади от нижне-височного лимба. Канюли диаметром 2,5 мм были вшиты на место полигалактиновым швом 5-0 (Викрил). Были расположены дополнительные участки склеротомии 2.25 мм кзади от лимба, в надвисочном и нижневисочном квадрантах. Резак стекловидного тела вводили через участок надвисочной склеротомии, а оптоволоконный осветитель вводили через участок надоназальной склеротомии. Ядро стекловидного тела удаляли из каждого глаза и заменяли стерильным сбалансированным солевым раствором (BSS; Alcon, San Antonio, Tex). В экспериментальных глазах канюля с силиконовым наконечником использовалась для создания заднего раздела стекловидного тела, охватывающего макулу и диск зрительного нерва.Были предприняты сознательные усилия, чтобы применить тракцию, которая располагалась по окружности или по касательной к сетчатке, насколько это возможно; вертикального подъема прикрепленного заднего гиалоидного лица не было. Затем инструменты были удалены, порты для склеротомии были закрыты полигалактиновыми швами 7-0, а инфузионные линии были зажаты. Обезьян умерщвляли с использованием 2 мл 2% пентобарбитала гидрохолорида (Sleepaway; Fort Dodge Inc, Fort Dodge), вводимого через внутривенную линию. Была проведена энуклеация, и глаза были немедленно обработаны, как описано ниже.Клинья глаз (сетчатка, пигментный эпителий сетчатки, головка зрительного нерва, цилиарное тело, хрусталик, задняя капсула хрусталика, зонулы, радужная оболочка и роговица) были подготовлены, как описано ниже, для гистопатологического и иммуногистохимического анализов.
Ядро стекловидного тела удаляли из каждого глаза и заменяли стерильным сбалансированным солевым раствором (BSS; Alcon, San Antonio, Tex). В экспериментальных глазах канюля с силиконовым наконечником использовалась для создания заднего раздела стекловидного тела, охватывающего макулу и диск зрительного нерва.Были предприняты сознательные усилия, чтобы применить тракцию, которая располагалась по окружности или по касательной к сетчатке, насколько это возможно; вертикального подъема прикрепленного заднего гиалоидного лица не было. Затем инструменты были удалены, порты для склеротомии были закрыты полигалактиновыми швами 7-0, а инфузионные линии были зажаты. Обезьян умерщвляли с использованием 2 мл 2% пентобарбитала гидрохолорида (Sleepaway; Fort Dodge Inc, Fort Dodge), вводимого через внутривенную линию. Была проведена энуклеация, и глаза были немедленно обработаны, как описано ниже.Клинья глаз (сетчатка, пигментный эпителий сетчатки, головка зрительного нерва, цилиарное тело, хрусталик, задняя капсула хрусталика, зонулы, радужная оболочка и роговица) были подготовлены, как описано ниже, для гистопатологического и иммуногистохимического анализов.
Глаза немедленно фиксировали в 4% параформальдегиде в 100 мМ натрий-какодилатном буфере, pH 7,4. Исследования проводились в соответствии с рекомендациями Ассоциации исследований зрения в офтальмологии и Национальных институтов здравоохранения по уходу за лабораторными животными.Перед проведением всех процедур было получено согласие Комитета по уходу за животными Университета Сент-Луиса.
Результаты световой микроскопии и гистохимии лектинов
После энуклеации передние сегменты глаза иссекали, а наглазники и передние сегменты фиксировали на 2-4 часа путем погружения в 4 штуки.0% формальдегид (свежевыработанный из параформальдегида) в 100 мМ натрий-какодилатном буфере, pH 7,4. Наглазники ополаскивали в течение минимум 6 часов в 100 мМ натрий-какодилатном буфере, заливали акриламидом и делали срезы толщиной приблизительно от 5 до 6 мкм на криостате при -20 ° C.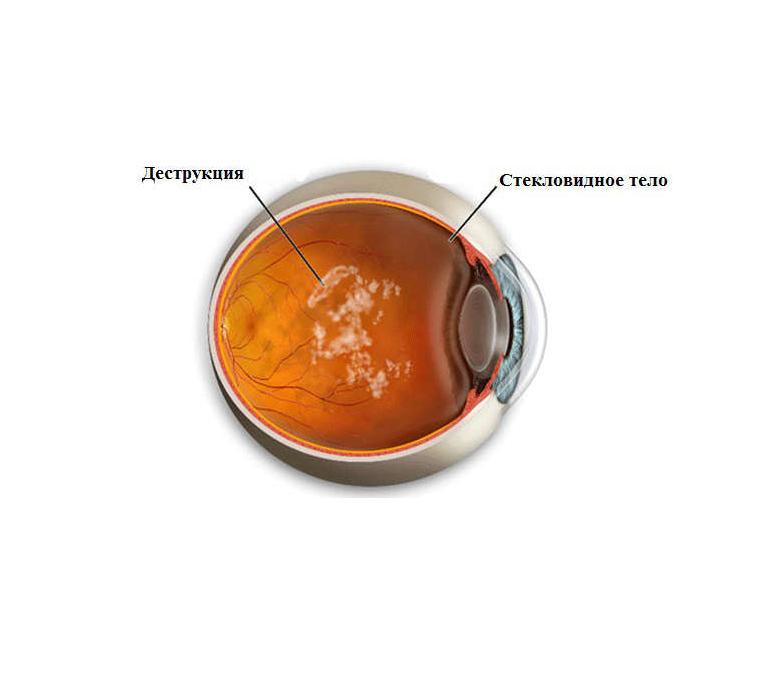 11 Меридиональные серийные срезы от плоской части глаза до зрительного нерва были вырезаны из каждого глаза.
11 Меридиональные серийные срезы от плоской части глаза до зрительного нерва были вырезаны из каждого глаза.
Для гистохимических исследований лектина срезы подвергали действию агглютинина Agaricus bisporus в концентрации 50 мг / мл в 10 мМ фосфатно-солевом растворе, содержащем от 1 мМ хлорида магния до 1 мМ хлорида кальция и 1 мг / мл безглобулиновой бычьей сыворотки. альбумин и обработали, как описано ранее. 11 Соседние срезы окрашивали гематоксилин-эозином. Затем предметные стекла промывали смесью фосфатно-буферного раствора с хлоридом магния и хлоридом кальция. Контроли включали инкубацию срезов с агглютинином A bisporus в присутствии конкурентного гаптена. Срезы исследовали с помощью эпифлуоресцентной микроскопии с использованием светового микроскопа (модель Vanox VH-2; Olympus America Inc, Мелвилл, штат Нью-Йорк) и фотографировали с использованием имеющейся в продаже пленки (Kodak Ektachrome ASA 400; Kodak, Рочестер, штат Нью-Йорк), установленной на индекс экспозиции 800.
Фокальные области прикрепленной коры стекловидного тела наблюдались в области глазного дна, лежащей в основе механически индуцированной задней отслойки стекловидного тела на 11 глазах; ограниченные разрывы или подъем ILL наблюдались в 9 глазах (Рисунок 1; Таблица 1). Наблюдалось большее повреждение или разрушение, включая отслоение ILL, отслоение фовеа, отслоение сетчатки, разрыв сетчатки и отрыв сосудов (рис. 1C, E-F). Фовеальная ткань разорвана на 11 глазах.Наблюдаемые поражения включали разрыв фовеальной области пупка (Рисунок 2B, D), отслоение перифовеальной ILL (Рисунок 2C), отслоение ямки (5 глаз) и отрыв фовеолы (Рисунок 2E-F), который гистологически неотличим от острая макулярная дыра. Повреждение диска зрительного нерва, включая потерю аксонов, наблюдалось в 9 глазах (рис. 3C-D). Небольшие поверхностные кровоизлияния в диск зрительного нерва или сетчатку были отмечены в 3 из 25 экспериментальных глаз. Никаких аналогичных патологических отклонений не было отмечено ни в одном из контрольных (ложно прооперированных) глаз (не показаны).
Эти данные показывают, что механически вызванная отслойка задней части стекловидного тела может вызвать немедленное повреждение и потерю нейросенсорной ткани заднего дна у молодых взрослых приматов. Из 25 глаз существенное повреждение диска зрительного нерва, ямки и экстрафовеальной сетчатки произошло в 11, 7 и 9 глазах соответственно. Неожиданно эти поражения обычно не обнаруживаются оперирующим хирургом. Последствия преднамеренного удаления ILL, 12 , 13 , которые, как ожидается, приведут к значительно большему повреждению и потере тканей, в этом исследовании не рассматривались.
Хотя значение этих повреждений для зрения у молодых взрослых приматов не может быть непосредственно установлено, можно ожидать дефектов зрения на основе локализации и тяжести индуцированных повреждений. В отличие от результатов предыдущих исследований, 14 -16 более свежие данные о ретинотопной организации приматов 17 предполагают, что более крупные и более периферические области ILL, слоя нервных волокон и отрыва ганглиозных клеток могут вызывать широкое распространение или клиновидность фигурные дефекты периферического поля зрения. Дефекты поля зрения, отмеченные после операции на макулярном отверстии, представляют собой абсолютные большие или клиновидные дефекты поля зрения. 18
Дефекты поля зрения, отмеченные после операции на макулярном отверстии, представляют собой абсолютные большие или клиновидные дефекты поля зрения. 18
Травма диска зрительного нерва была предложена Мелбургом и Томасом 19 как возможная причина дефектов поля зрения, связанных с восстановлением макулярного отверстия, и при проведении аспирации непосредственно через диск зрительного нерва рекомендовалось соблюдать осторожность. В 1 из 8 глаз с потерей поля зрения после операции на стекловидном теле Kerrison et al 20 отметили небольшое кровоизлияние, прилегающее к сосуду диска зрительного нерва после хирургического отделения заднего гиалоида от надвисочного зрительного нерва, частота, аналогичная результатам нашего исследования. .Расположение кровоизлияния соответствовало области потери поля зрения. Аналогичный периферический абсолютный дефект поля зрения был отмечен в другом глазу, который не подвергался обмену воздух-жидкость. Эти данные свидетельствуют о том, что в некоторых случаях контакт воздуха или газа с сетчаткой может не требоваться для развития дефектов поля зрения. Эти авторы считали потерю поля зрения результатом повреждения диска зрительного нерва, возможно, из-за срезания перипапиллярных аксонов и / или сосудов, 20 — открытие, отмеченное с высокой частотой в нашем исследовании.В другом отчете о дефектах поля зрения после операции на макулярном отверстии было обнаружено, что 18 6 из 8 глаз имели статистически значимое уменьшение толщины слоя перипапиллярных нервных волокон, соответствующее распределению дефектов поля зрения. Хаттон и др. Пришли к выводу, что «искусственное, резкое отслоение кортикального слоя стекловидного тела, возможно, в сочетании с довольно длительным прямым контактом газового пузыря с задним полюсом глаза» 18 (p2157) может быть причиной.
Эти авторы считали потерю поля зрения результатом повреждения диска зрительного нерва, возможно, из-за срезания перипапиллярных аксонов и / или сосудов, 20 — открытие, отмеченное с высокой частотой в нашем исследовании.В другом отчете о дефектах поля зрения после операции на макулярном отверстии было обнаружено, что 18 6 из 8 глаз имели статистически значимое уменьшение толщины слоя перипапиллярных нервных волокон, соответствующее распределению дефектов поля зрения. Хаттон и др. Пришли к выводу, что «искусственное, резкое отслоение кортикального слоя стекловидного тела, возможно, в сочетании с довольно длительным прямым контактом газового пузыря с задним полюсом глаза» 18 (p2157) может быть причиной.
Представление о том, что повреждение диска зрительного нерва или периферического сетчатки может вызвать потерю периферического поля зрения, согласуется с результатами исследования Cullinane and Cleary, 21 , которые продемонстрировали, что 18 (24%) из 75 глаз развили периферические дефекты поля зрения после «полного» хирургическая задняя отслойка стекловидного тела. Ни в одном из 20 глаз, в которых механическое разделение стекловидного тела ограничивалось желтым пятном (стекловидное тело не было отделено от диска зрительного нерва или периферической сетчатки), не было обнаружено подобных дефектов периферического поля зрения.
Ни в одном из 20 глаз, в которых механическое разделение стекловидного тела ограничивалось желтым пятном (стекловидное тело не было отделено от диска зрительного нерва или периферической сетчатки), не было обнаружено подобных дефектов периферического поля зрения.
Имеются убедительные доказательства того, что дефекты поля зрения после некоторых хирургических вмешательств на макулярных отверстиях могут быть связаны с высыханием сетчатки или диска зрительного нерва. 22 Задний гиалоид, прикрепленный к диску зрительного нерва или периферической сетчатке, может действовать как резервуар гидратации. При удалении может облегчиться иссушение диска зрительного нерва или сетчатки. Освобождение нервной сетчатки от ее базальной мембраны может повысить восприимчивость к высыханию, холоду или другим механизмам.Удаление ILL непосредственно подвергает нервные клетки воздействию внутриглазной среды, подвергая ганглиозные клетки (если они не оторваны) и интернейроны сетчатки потенциально большему риску высыхания. Подробное обсуждение этих и других причин ятрогенной потери поля зрения можно найти в других источниках. 9 , 18
Подробное обсуждение этих и других причин ятрогенной потери поля зрения можно найти в других источниках. 9 , 18
В этом исследовании документально подтверждено значительное повреждение внутренней сетчатки, желтого пятна и зрительного нерва после хирургического отделения стекловидного тела от ILL. Эти наблюдения могут помочь объяснить случаи, когда дефекты поля зрения возникают в результате аналогичных хирургических процедур у людей.Наши результаты показывают, что другие немеханические методы, включая ферментативную витрэктомию 23 , 24 для отделения коры стекловидного тела от ILL, могут привести к снижению операционных осложнений и улучшению зрения.
Принята к публикации 10 июля 2001 г.
Это исследование было поддержано грантом RO1 EY06463 Национального института глаз, Бетезда, Мэриленд (д-р Хагеман), исследовательским грантом от American Cyanamid Corp и American Home Products, Перл-Ривер, штат Нью-Джерси (д-р Хагеман), и исследованием по предотвращению слепоты. Inc, Нью-Йорк, штат Нью-Йорк (Департамент офтальмологии и визуальных наук, Университет Айовы).
Inc, Нью-Йорк, штат Нью-Йорк (Департамент офтальмологии и визуальных наук, Университет Айовы).
Мы благодарим Gena Bohning, H. Culver Boldt, MD, Patricia Duffel, MA, Mary McDonald, Bobbie Schneider и Ramona Weber за их помощь и обсуждения.
Автор, ответственный за переписку: Стивен Р. Рассел, доктор медицины, факультет офтальмологии и визуальных наук, Университет Айовы, доктор Хокинс, 200, комната 11196 I, Айова-Сити, Айова 52242 (электронная почта: [email protected]).
1. пол БП Стекловидное тело. Моисей RAHart WMeds. Физиология глаза Адлера: клиническое применение. 8th St Louis Mosby – Year Book Inc 1987; 246–267 Google Scholar2.Kelly NEWendel RT Хирургия стекловидного тела по поводу идиопатических макулярных отверстий: результаты пилотного исследования. Arch Ophthalmol. 1991; 109654-659Google ScholarCrossref 3.
Bovino JA Макулярная хирургия. Энглвуд Клиффс, Нью-Джерси Эпплтон и Ланге 1994; 184
4. Вендель RTPatel ACKelly NESalzano TCWells JWNovack Г.Д. Хирургия стекловидного тела при макулярных отверстиях. Офтальмология. 1993; 1001671-1676Google ScholarCrossref 5.Freeman WRAzen СПКим JWel-Haig WMishell DR IIIБейли Группа исследования витрэктомии для лечения макулярных отверстий, витрэктомия для лечения 3-й или 4-й стадии макулярных отверстий полной толщины: результаты многоцентрового рандомизированного клинического исследования. Arch Ophthalmol. 1997; 11511-21Google ScholarCrossref 6.Capone А Jr Нарушения макулярной поверхности. Координаторы. 1996; 1-13 Google Scholar8, Гарсия-Аруми JCorcostegui BCavero LSararols L Роль витреоретинальной хирургии в лечении посттравматического макулярного отверстия. Retina. 1997; 17372–377Google ScholarCrossref 9.Boldt
HCMunden
PMFolk
JCMehaffey
MG Дефекты поля зрения после операции на макулярной ямке. Am J Ophthalmol. 1996; 122371-381Google Scholar 10.Ripandelli
GCoppe
А-МФальсини
Б.Федели
RStirpe
M Осложнения при удалении задней коры стекловидного тела.Видеманн
PKohen
Светодиоды. Заболевания желтого пятна и сетчатки: последние достижения в диагностике и терапии. 29 Базель, Швейцария S Karger AG1997; 55–60 Google Scholar 11. Рассел
SRShepherd
JDHageman
GS Распределение гликоконъюгатов во внутренней ограничивающей мембране сетчатки человека. Invest Ophthalmol Vis Sci. , 1991; 321986-1995. Google Scholar, 12.Юн.
HSBrooks
HL
JrCapone
А
JrL’Hernault
NLGrossniklaus
H Ультраструктурные особенности ткани, удаленной во время идиопатической операции на макулярном отверстии.
Retina. 1997; 17372–377Google ScholarCrossref 9.Boldt
HCMunden
PMFolk
JCMehaffey
MG Дефекты поля зрения после операции на макулярной ямке. Am J Ophthalmol. 1996; 122371-381Google Scholar 10.Ripandelli
GCoppe
А-МФальсини
Б.Федели
RStirpe
M Осложнения при удалении задней коры стекловидного тела.Видеманн
PKohen
Светодиоды. Заболевания желтого пятна и сетчатки: последние достижения в диагностике и терапии. 29 Базель, Швейцария S Karger AG1997; 55–60 Google Scholar 11. Рассел
SRShepherd
JDHageman
GS Распределение гликоконъюгатов во внутренней ограничивающей мембране сетчатки человека. Invest Ophthalmol Vis Sci. , 1991; 321986-1995. Google Scholar, 12.Юн.
HSBrooks
HL
JrCapone
А
JrL’Hernault
NLGrossniklaus
H Ультраструктурные особенности ткани, удаленной во время идиопатической операции на макулярном отверстии. Am J Ophthalmol. 1996; 12267-75Google Scholar13.Park
DWSipperley
JOSneed
С.Р.Дугель
PUJacobsen
J Операция по удалению макулярного отверстия с пилингом внутренней ограничивающей мембраны и интравитреальным воздухом. Офтальмология. 1999; 1061392–1398Google ScholarCrossref 14.Wolff
EPenman
GG Положение, которое занимают периферические волокна сетчатки в слое нервных волокон и в нервной головке. Британская медицинская ассоциация, изд., XVI Concilium Ophthalmologicum Brittania. Лондон, Англия Британская медицинская ассоциация 1951; 625–635Google Scholar15.Radius
RLAnderson
DR Ход аксонов через сетчатку и головку зрительного нерва. Arch Ophthalmol. 1979; 971154-1158Google ScholarCrossref 16. Minckler
DS Организация пучков нервных волокон в головке зрительного нерва приматов.
Am J Ophthalmol. 1996; 12267-75Google Scholar13.Park
DWSipperley
JOSneed
С.Р.Дугель
PUJacobsen
J Операция по удалению макулярного отверстия с пилингом внутренней ограничивающей мембраны и интравитреальным воздухом. Офтальмология. 1999; 1061392–1398Google ScholarCrossref 14.Wolff
EPenman
GG Положение, которое занимают периферические волокна сетчатки в слое нервных волокон и в нервной головке. Британская медицинская ассоциация, изд., XVI Concilium Ophthalmologicum Brittania. Лондон, Англия Британская медицинская ассоциация 1951; 625–635Google Scholar15.Radius
RLAnderson
DR Ход аксонов через сетчатку и головку зрительного нерва. Arch Ophthalmol. 1979; 971154-1158Google ScholarCrossref 16. Minckler
DS Организация пучков нервных волокон в головке зрительного нерва приматов. Arch Ophthalmol. 1980; 981630–1636Google ScholarCrossref 17.Ogden
Т.Е. Слой нервных волокон сетчатки макака: ретинотопная организация. Invest Ophthalmol Vis Sci. 1983; 2485-98 Google Scholar 18.Hutton
WLFuller
Д.Г.Снайдер
WB Новое открытие: дефект поля зрения после операции на макулярной дыре. Офтальмология. 1996; 1032152-2159Google ScholarCrossref 19. Melberg
NSThomas
М.А. Потеря поля зрения после витрэктомии pars plana с воздухо-жидкостным обменом. Am J Ophthalmol. 1995; 120386-388Google Scholar20.Kerrison
JBHaller
JAElman
MMiller
NR Потеря поля зрения после операции на стекловидном теле. Arch Ophthalmol. 1996; 114564-569Google ScholarCrossref 21.Cullinane
ACleary
PE Профилактика дефектов поля зрения после операции на макулярной ямке.
Arch Ophthalmol. 1980; 981630–1636Google ScholarCrossref 17.Ogden
Т.Е. Слой нервных волокон сетчатки макака: ретинотопная организация. Invest Ophthalmol Vis Sci. 1983; 2485-98 Google Scholar 18.Hutton
WLFuller
Д.Г.Снайдер
WB Новое открытие: дефект поля зрения после операции на макулярной дыре. Офтальмология. 1996; 1032152-2159Google ScholarCrossref 19. Melberg
NSThomas
М.А. Потеря поля зрения после витрэктомии pars plana с воздухо-жидкостным обменом. Am J Ophthalmol. 1995; 120386-388Google Scholar20.Kerrison
JBHaller
JAElman
MMiller
NR Потеря поля зрения после операции на стекловидном теле. Arch Ophthalmol. 1996; 114564-569Google ScholarCrossref 21.Cullinane
ACleary
PE Профилактика дефектов поля зрения после операции на макулярной ямке. Br J Ophthalmol. 2000; 84372–377Google ScholarCrossref 22. Велч
JC Обезвоживание как возможная причина дефекта поля зрения после витрэктомии pars plana по поводу макулярного отверстия. Am J Ophthalmol. 1997; 124698-699Google Scholar23.Trese
MTWilliams
GAHartzer
MK Новый подход к 3 стадии макулярных отверстий. Офтальмология. 2000; 1071607-1611Google ScholarCrossref 24.Tezel
THDel Priore
LVKaplan
HJ Задняя отслойка стекловидного тела с диспасом. Retina. 1998; 187-15 15Google ScholarCrossref
Br J Ophthalmol. 2000; 84372–377Google ScholarCrossref 22. Велч
JC Обезвоживание как возможная причина дефекта поля зрения после витрэктомии pars plana по поводу макулярного отверстия. Am J Ophthalmol. 1997; 124698-699Google Scholar23.Trese
MTWilliams
GAHartzer
MK Новый подход к 3 стадии макулярных отверстий. Офтальмология. 2000; 1071607-1611Google ScholarCrossref 24.Tezel
THDel Priore
LVKaplan
HJ Задняя отслойка стекловидного тела с диспасом. Retina. 1998; 187-15 15Google ScholarCrossrefМногообещающий подход в лазерной витрэктомии, выполняемый путем плазменного удаления стекловидного тела с помощью лазера Nd: YAG с диодной накачкой и модуляцией добротности
Blodi, C. F. Дэвид Каснер, доктор медицины Путь к плоской витрэктомии. Ophthalmol Eye Dis 14 8 (Приложение 1), 1–4.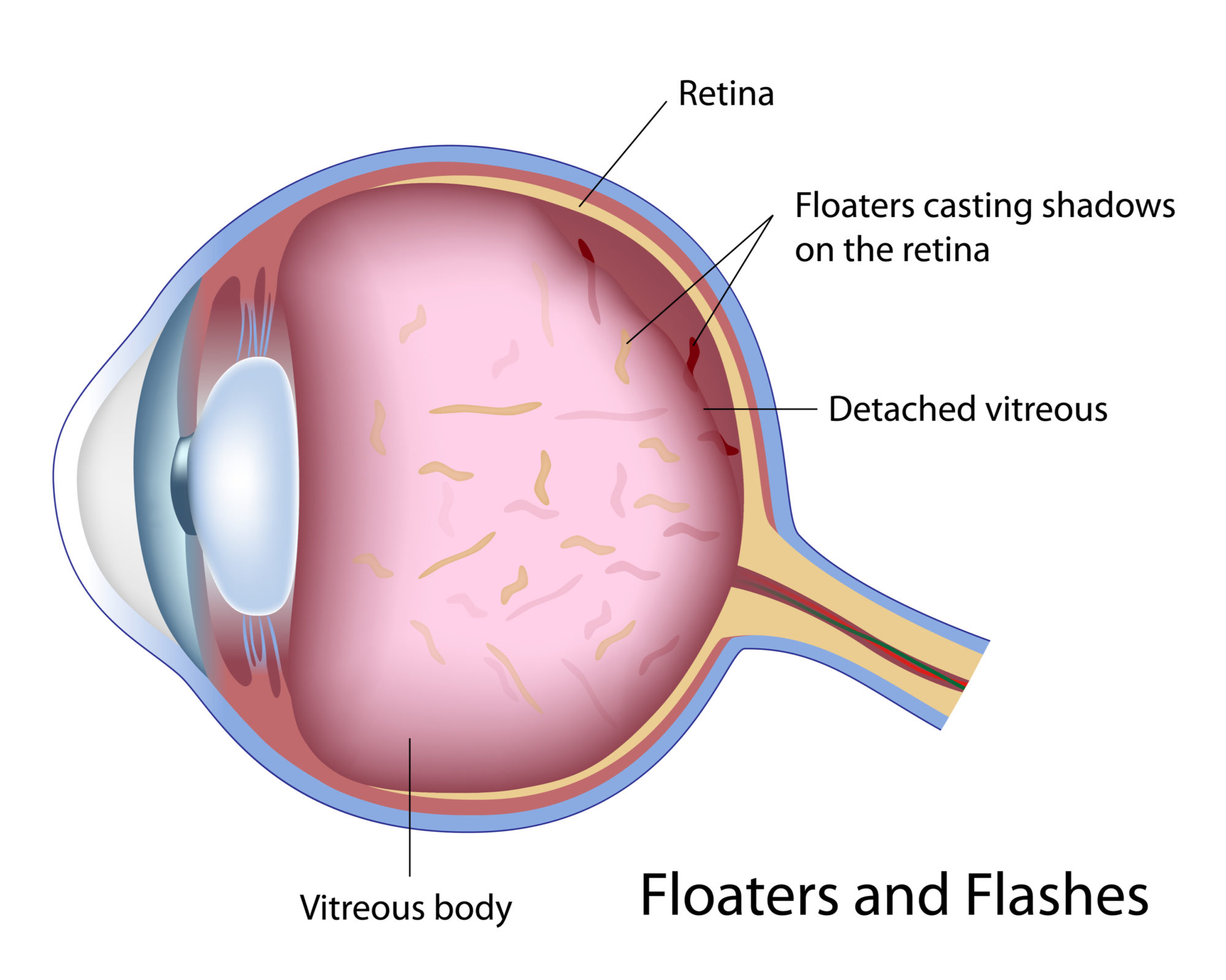 https://doi.org/10.4137/OED.S40424 (2016).
https://doi.org/10.4137/OED.S40424 (2016).
Артикул Google Scholar
Machemer, R., Buettner, H., Norton, E. W. и Parel, J. M. Витрэктомия: доступ к pars plana. Пер. Являюсь. Акад. Офтальмол. Отоларингол. 75 (4), 813–820 (1971).
CAS PubMed Google Scholar
O’Malley, C. & Heintz, R.M.Sr .. Витрэктомия с альтернативной системой инструментов. Ann Ophthalmol 7 (4), 585–588, 591–594 (1975).
CAS PubMed Google Scholar
Чарльз С. История витрэктомии: инновации и эволюция. Retina сегодня 9 (10), 27–29 (2008).
Google Scholar
де Оливейра, П. Р. К., Бергер, А. Р. и Чоу, Д. Р. Витреоретинальные инструменты: резаки для витрэктомии, системы эндоиллюминации и широкоугольные системы обзора.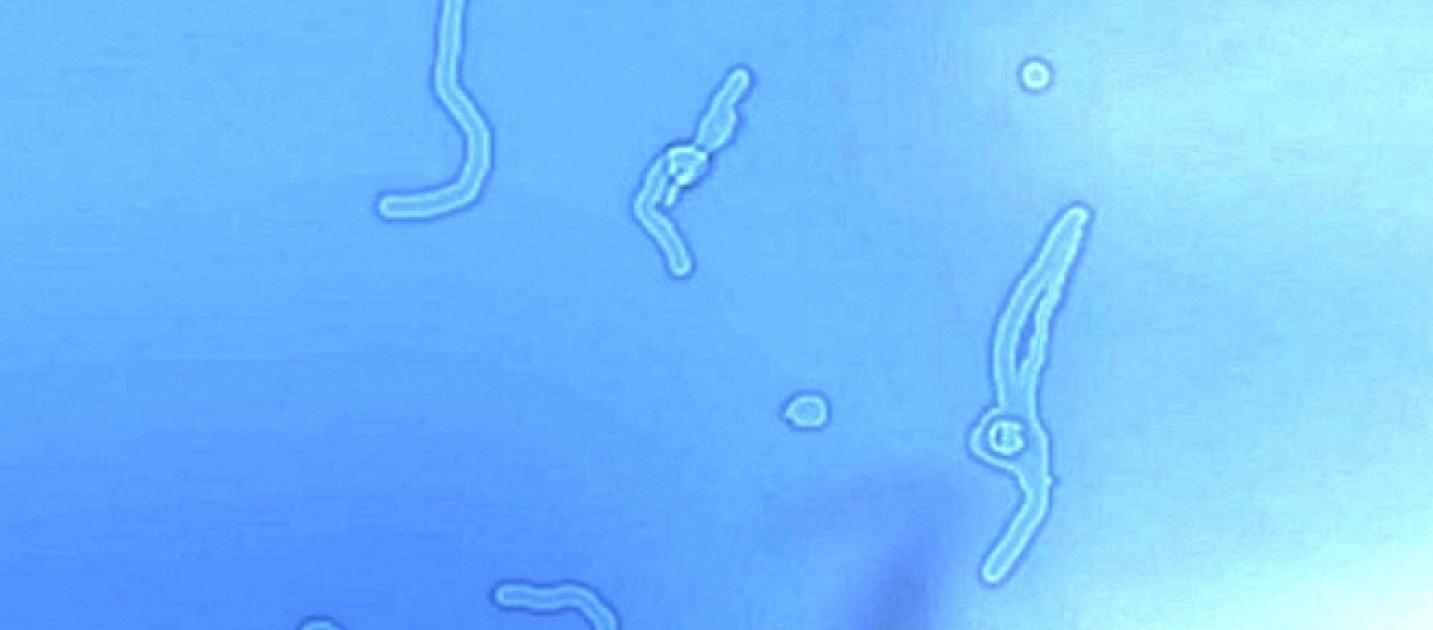 Внутр. J. Retina Vitreous 2 , 28. https://doi.org/10.1186/s40942-016-0052-9 (2016).
Внутр. J. Retina Vitreous 2 , 28. https://doi.org/10.1186/s40942-016-0052-9 (2016).
Артикул PubMed PubMed Central Google Scholar
Чарльз С. Инженерный подход к витреоретинальной хирургии. Retina 24 (3), 435–444. https://doi.org/10.1097/00006982-200406000-00015 (2004).
Артикул PubMed Google Scholar
Banko, A. & Kehlman, C. Устройство и способ удаления материала, использующие высокочастотные колебания. Патент США 3589363 (1971)
Girard, L.J., Nieves, R. & Hawkins, R.S. Ультразвуковая фрагментация для витрэктомии и связанных хирургических процедур. Пер. Разд. Офтальмол. Являюсь. Акад. Офтальмол. Отоларингол. 81 (3 Pt 1), 432–450 (1976).
CAS PubMed Google Scholar
Leitgeb, N., Schuy, S. & Zirm, M. Ультразвуковая витрэктомия — альтернатива применяемым в настоящее время механическим процедурам. Альбрехт. Фон. Graefes Arch. Клин. Exp. Офтальмол. 209 (4), 263–268. https://doi.org/10.1007/bf00419061 (1979).
Ультразвуковая витрэктомия — альтернатива применяемым в настоящее время механическим процедурам. Альбрехт. Фон. Graefes Arch. Клин. Exp. Офтальмол. 209 (4), 263–268. https://doi.org/10.1007/bf00419061 (1979).
CAS Статья PubMed Google Scholar
Pastor-Idoate, S. et al. Ультраструктурные и гистопатологические данные после витрэктомии pars plana с использованием новой гиперзвуковой витректорной системы.Качественная предварительная оценка. PLoS ONE 12 (4), e0173883. https://doi.org/10.1371/journal.pone.0173883 (2017).
CAS Статья PubMed PubMed Central Google Scholar
Станга П. Э., Пастор-Идоат С., Замбрано И., Карлин П. и МакЛеод Д. Анализ производительности новой гиперзвуковой системы витректора. PLoS ONE 12 (6), e0178462. https://doi.org/10.1371 / journal.pone.0178462 (2017).
CAS Статья PubMed PubMed Central Google Scholar
Хейл, Г. М. и Куэрри, М. Р. Оптические константы воды в диапазоне длин волн от 200 нм до 200 микрометров. Прил. Опт. 12 (3), 555–563. https://doi.org/10.1364/AO.12.000555 (1973).
ADS CAS Статья PubMed Google Scholar
D’Amico, D. J. et al. Многоцентровый клинический опыт использования эрбиевого YAG-лазера в витреоретинальной хирургии. Офтальмология 103 (10), 1575–1585. https://doi.org/10.1016/S0161-6420(96)30460-0 (1996).
CAS Статья PubMed Google Scholar
Brazitikos, P. D. et al. Экспериментальная хирургия глаза с использованием высокочастотного эрбиевого лазера: YAG. Инвест.Офтальмол. Vis. Sci. 39 (9), 1667–1675 (1998).
CAS PubMed Google Scholar
Mrochen, M., Petersen, H., Wüllner, C. & Seiler, T. Экспериментальные результаты эрбиевой лазерной витрэктомии. Klin Monbl Augenheilkd 212 (1), 50–54. https://doi.org/10.1055/s-2008-1034831 (1998) ( [Германия] ).
CAS Статья PubMed Google Scholar
Краузе М., Стиб Д., Фот Х. Дж., Вайндлер Дж. И Рупрехт К. В. Абляция стекловидного тела эрбиевым лазером на основе YAG. Инвест. Офтальмол. Vis. Sci. 40 (6), 1025–1032 (1999).
CAS PubMed Google Scholar
Петерсен, Х., Мрохен, М. и Зайлер, Т. Сравнение эрбиевой: иттрий-алюминиево-гранатовой лазерной витрэктомии и механической витрэктомии: клиническое исследование. Офтальмология 107 (7), 1389–1392.https://doi.org/10.1016/s0161-6420(00)00123-8 (2000).
CAS Статья PubMed Google Scholar
Биндер, С., Столба, У., Келлнер, Л. и Кребс, И. Эрбий: лазерная витрэктомия YAG: клинические результаты. Am. J. Ophthalmol. 130 (1), 82–86. https://doi.org/10.1016/s0002-9394(00)00399-8 (2000).
CAS Статья PubMed Google Scholar
Ридель П., Мрохен М., Деницки К. и Зайлер Т. Артефакты движения в стекловидном теле во время витрэктомии. Офтальмолог 97 (9), 615–618. https://doi.org/10.1007/s003470070048 (2000) ( [Германия] ).
CAS Статья PubMed Google Scholar
Mrochen, M., Riedel, P., Donitzky, C. & Seiler, T. Об образовании паровых пузырьков во время эрбия: лазерная витрэктомия YAG. Офтальмолог 98 (2), 163–167.https://doi.org/10.1007/s003470170178 (2001) ( [Германия] ).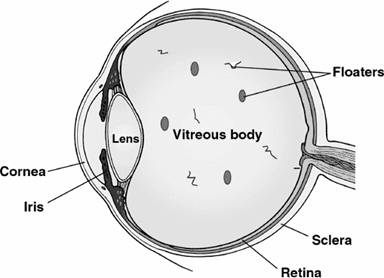
CAS Статья PubMed Google Scholar
Краузе, М. Х. и Д’Амико, Д. Дж. Абляция стекловидного тела с помощью эрбиевого лазера с высокой частотой повторения. Eur. J. Ophthalmol. 13 (5), 424–432. https://doi.org/10.1177/112067210301300502 (2003).
CAS Статья PubMed Google Scholar
, Sigma Aldrich https://www.sigmaaldrich.com/chemistry/stockroom-reagents/learning-center/technical-library/needle-gauge-chart.html, 6 февраля 2018 г.
Краусс, Дж. М., Пулиафито, Калифорния, Миглиор, С., Стейнерт, Р. Ф. и Ченг, Х. М. Изменения стекловидного тела после фоторазрушения неодим-YAG-лазером. Arch. Офтальмол. 104 (4), 592–597. https://doi.org/10.1001/archopht.1986.01050160148031 (1986).
CAS Статья PubMed Google Scholar

Абделькави, С. А. Реологические свойства стекловидного тела после фотодеструкции лазера Nd: YAG с модуляцией добротности. Biophysl. Rev. Lett. 7 (1 и 2), 29–39. https://doi.org/10.1142/S179304801250004X (2012).
Артикул Google Scholar
Абделькави, С. А., Абдель-Салам, А. М., Гоним, Д. Ф. и Гали, С. К. Реология стекловидного тела после лазерного фоторазрушения Nd: YAG. Cell Biochem. Биофиз. 68 (2), 267–274. https://doi.org/10.1007/s12013-013-9706-5 (2014).
CAS Статья PubMed Google Scholar
Малисон, И. Х. Межпредметное сравнение показателя преломления плавленого кремнезема. J. Opt. Soc. Являюсь. 55 (10), 1205–1209. https://doi.org/10.1364/JOSA.55.001205 (1965).
ADS CAS Статья Google Scholar
Regal, S. et al. Определение оптических параметров глаза свиньи и создание имитационной модели. Дж Био 12 (11), e201800398 (1-13). https://doi.org/10.1002/jbio.201800398 (2019).
et al. Определение оптических параметров глаза свиньи и создание имитационной модели. Дж Био 12 (11), e201800398 (1-13). https://doi.org/10.1002/jbio.201800398 (2019).
Артикул Google Scholar
Дьёрдь, Э., Михайлеску, И. Н., Серра, П., Перес дель Пино, А. и Моренца, Дж. Л. Облучение титана одиночным импульсом Nd: YAG-лазером: влияние интенсивности лазера на морфологию поверхности. Surf. Пальто. Techol. 154 (1), 63–67. https://doi.org/10.1016/S0257-8972(01)01699-1 (2002).
Артикул Google Scholar
Дак Ф. А. Физические свойства ткани 320 (Academic Press, Лондон, Сан-Диего, Нью-Йорк, 1990).
Google Scholar
Sebag, J. Стекловидное тело, структура, функция и патобиология 1-е изд., 17–58 (Springer, New York, 1990).

Лаппас, Н. Т. и Лаппас, К. М. Аналитические образцы — стекловидное тело в судебной токсикологии 113–142 (Academic Press, London, San Diego, Waltham, 2016).
Google Scholar
Ли Б., Литт М. и Бухсбаум Г. Реология стекловидного тела: Часть 1. Вязкоупругость стекловидного тела человека. Биореология 29 (5–6), 521–533. https://doi.org/10.3233/BIR-1992-295-612 (1992).
CAS Статья PubMed Google Scholar
Сильва А. Ф., Алвес М. А. и Оливейра М. С. Реологическое поведение стекловидного тела. Rheol. Acta 56 (4), 377–386. https://doi.org/10.1007/s00397-017-0997-0 (2017).
CAS Статья Google Scholar
Кавано С. И., Хонда Ю. и Неги А. Влияние биологических стимулов на вязкость стекловидного тела. Acta Ophthalmol (Копен) 60 (6), 977–991. https://doi.org/10.1111/j.1755-3768.1982.tb00630.x (1982).
https://doi.org/10.1111/j.1755-3768.1982.tb00630.x (1982).
CAS Статья Google Scholar
Дэвид Т., Смай С., Даббс Т. и Джеймс Т. Модель плавного движения стекловидного тела человеческого глаза во время саккадического движения. Phys. Med. Биол. 43 (6), 1385–1399. https://doi.org/10.1088/0031-9155/43/6/001 (1998).
CAS Статья PubMed Google Scholar
Noulas, A. V. et al. Гель стекловидного тела свиньи: макромолекулярная композиция с особым акцентом на гиалуронан-связывающие протеогликаны. Biochimie 84 (4), 295–302. https://doi.org/10.1016/S0300-9084(02)01389-5 (2002).
CAS Статья PubMed Google Scholar
Ли Б., Литт М. и Бухсбаум Г. Реология стекловидного тела: Часть 2. Вязкоупругость стекловидного тела крупного рогатого скота и свиньи. Биореология 31 (4), 327–338. https://doi.org/10.3233/BIR-1994-31403 (1994).
Биореология 31 (4), 327–338. https://doi.org/10.3233/BIR-1994-31403 (1994).
Артикул PubMed Google Scholar
Pokki, J. et al. Измерение локальной вязкоупругости стекловидного тела с помощью внутриглазных микрозондов. Биомедицинские микроустройства 17 (5), 85 (1–9). https://doi.org/10.1007/s10544-015-9988-z (2015).
Артикул Google Scholar
Donati, S. et al. Заменители стекловидного тела: настоящее и будущее. BioMed. Res. Int. https://doi.org/10.1155/2014/351804 (2014).
Артикул PubMed PubMed Central Google Scholar
Чирила Т. В., Хонг Ю. Стекловидное тело. В справочнике по свойствам биоматериалов (ред. Мерфи, W. и др. ) 125–134 (Springer, New York, 2016). https://doi.org/10.1007 / 978-1-4939-3305-1.
Глава Google Scholar
Шафер, Д. М. Внутриглазные инъекции как дополнение к другим процедурам отслоения сетчатки. В Спорные аспекты лечения отслоения сетчатки (ред. Шепенс, К. Л. и Реган, К. Д. Дж.) 186–204 (Little, Brown and Company, Бостон, 1965).
Google Scholar
Sauder, G., Руф, Э., Моэдл, С. и Тайзел, Р. Наносекундная лазерная хирургия катаракты в LOCS III степени 4 и 5: серия случаев. Asia-Pac. J. Ophthalmol. 6 (5), 425–428. https://doi.org/10.22608/apo.2017123 (2017).
Артикул Google Scholar
Какие витамины и минералы восстанавливают стекловидное тело
Глазной врач, исследующий глаз пациента
Кредит изображения: IPGGutenbergUKLtd / iStock / Getty Images
Стекловидное тело — это жидкость, которая заполняет заднюю часть глаза.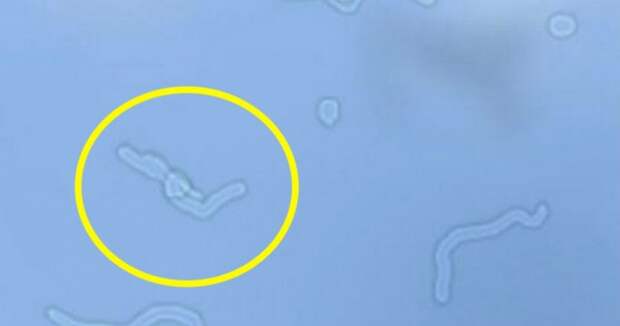 Это густое гелеобразное вещество помогает глазам сохранять форму, а также защищает структуры внутри глаза. С возрастом стекловидное тело может разрушаться и слипаться. Этот процесс может привести к появлению мутных пятен, черных пятен, которые будут попадать в поле зрения. Лечение не может восстановить эту жидкость, но определенные питательные вещества могут помочь предотвратить распад компонентов стекловидного тела.
Это густое гелеобразное вещество помогает глазам сохранять форму, а также защищает структуры внутри глаза. С возрастом стекловидное тело может разрушаться и слипаться. Этот процесс может привести к появлению мутных пятен, черных пятен, которые будут попадать в поле зрения. Лечение не может восстановить эту жидкость, но определенные питательные вещества могут помочь предотвратить распад компонентов стекловидного тела.
Окисление
Разрушение стекловидного тела может быть результатом окисления. Это естественный процесс, происходящий в вашем теле, в результате которого нестабильные молекулы, часто называемые свободными радикалами, повреждают клетки, в том числе клетки, составляющие стекловидное тело.Свободные радикалы образуются в результате воздействия радиации, сигаретного дыма или химических веществ, а также в результате естественного процесса переваривания и хранения пищи, поясняет Национальный центр дополнительной и альтернативной медицины. Вы можете ограничить воздействие факторов окружающей среды, чтобы снизить риск окислительного стресса.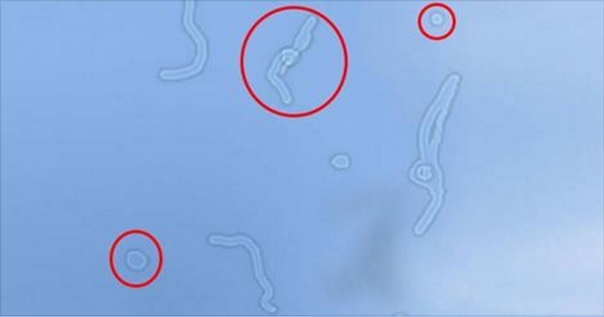 Чтобы предотвратить образование свободных радикалов в результате процессов в организме, вы можете употреблять здоровую пищу, содержащую антиоксиданты, питательные вещества, которые могут помочь предотвратить окисление.
Чтобы предотвратить образование свободных радикалов в результате процессов в организме, вы можете употреблять здоровую пищу, содержащую антиоксиданты, питательные вещества, которые могут помочь предотвратить окисление.
Антиоксиданты
Многие питательные вещества обладают антиоксидантными свойствами, и эти питательные вещества могут помочь снизить риск появления плавающих помутнений и других повреждений стекловидного тела.Некоторые из этих полезных питательных веществ включают витамин C, витамин E, бета-каротин, лютеин и зеаксантин. Не следует увеличивать потребление без предварительной консультации с врачом. Она может оценить ваш рацион и помочь составить план питания, отвечающий всем вашим потребностям в питании.
Источники
Ваш врач может порекомендовать вам принимать витаминные добавки, содержащие одно или несколько антиоксидантных питательных веществ. Однако вместо этого она может посоветовать вам выбирать здоровую пищу, которая обеспечит вас питательными веществами, необходимыми для поддержания здоровья стекловидного тела и других частей глаз. Например, темно-зеленые листовые овощи содержат лютеин и зеаксантин, или вы можете выбрать клубнику, апельсины и шпинат для получения витамина С. Кроме того, многие орехи и семена, такие как миндаль и семена подсолнечника, содержат витамин Е. Если ваш врач рекомендует это вы увеличиваете потребление антиоксидантов с помощью диеты, она поможет вам составить план питания, который обеспечит вас источниками питательных веществ, которые соответствуют вашим потребностям здоровья.
Например, темно-зеленые листовые овощи содержат лютеин и зеаксантин, или вы можете выбрать клубнику, апельсины и шпинат для получения витамина С. Кроме того, многие орехи и семена, такие как миндаль и семена подсолнечника, содержат витамин Е. Если ваш врач рекомендует это вы увеличиваете потребление антиоксидантов с помощью диеты, она поможет вам составить план питания, который обеспечит вас источниками питательных веществ, которые соответствуют вашим потребностям здоровья.
Соображения
Многие люди видят несколько плавающих помутнений, но если у вас появились новые помутнения, вам следует обратиться к врачу.Внезапное появление множества новых помутнений может указывать на отслойку сетчатки, и это требует немедленного внимания, чтобы предотвратить необратимые изменения в вашем зрении. Если вы хотите увеличить потребление антиоксидантов, сначала проконсультируйтесь с врачом. Некоторые продукты и питательные вещества могут мешать приему некоторых лекарств, например, антикоагулянтов. Ваш врач может помочь вам определить, есть ли у вас риск этих взаимодействий.
Ваш врач может помочь вам определить, есть ли у вас риск этих взаимодействий.
причин, форм и лечения болезни
Разрушение стекловидного тела — очень опасная проблема, которая при отсутствии лечения приводит к ухудшению и даже полной потере зрения.
Для начала стоит отметить, что стекловидное тело представляет собой гелеобразное вещество, заполняющее внутреннюю полость глазного яблока. Он не только формирует глаз, но и отвечает за преломление света и его передачу на сетчатку, а также обеспечивает тургор и эластичность тканей. Поэтому любое его изменение напрямую влияет на состояние зрительного анализатора.
Что такое разрушение стекловидного тела?
Деструкцией называют любые изменения структуры, состава и формы стекловидного тела.Обычно это явление носит возрастной характер — к 50 — 60 годам начинаются медленные деструктивные процессы. Но иногда болезнь появляется в более раннем и даже детском возрасте — уже требует помощи специалиста. Итак, какие изменения могут произойти?
Итак, какие изменения могут произойти?
- Самая частая форма деструкции Рассматривается частичное или полное расширение стекловидного тела. В таких случаях внутри начинают образовываться пустоты, которые постепенно заполняются жидкостью, волокнами, нитями белка — эти элементы могут свободно плавать в веществе стекловидного тела, вызывая нарушение зрения.
- Разрушение стекловидного тела может сопровождаться отложением кристаллов тирозина, холестерина или других веществ.
- Самой серьезной формой заболевания считается бивитервация стекловидного тела. В таких случаях вещество начинает постепенно сокращаться, растягивая витреоретинальные связки. Довольно часто в этом состоянии также наблюдается отслойка стекловидного тела от сетчатки, а также разрывы связок, кровоизлияния и другие опасные явления. Очень важно вовремя обратиться к врачу, так как повреждение сетчатки может привести к необратимым патологиям.
Почему происходит разрушение стекловидного тела?
На самом деле причины этого заболевания не всегда ясны. Известно только, что разрушение может быть вызвано любым фактором, который может нарушить физико-химические свойства и равновесие в коллоидном растворе стекловидного геля. К ним относятся воспалительные процессы и некоторые инфекционные заболевания глаз, а также нарушения в работе желез внутренней секреции, печени, почек и других органов.Иногда на состояние глазного яблока влияет вредная привычка, неправильный образ жизни, постоянное воздействие вредных химических веществ.
Известно только, что разрушение может быть вызвано любым фактором, который может нарушить физико-химические свойства и равновесие в коллоидном растворе стекловидного геля. К ним относятся воспалительные процессы и некоторые инфекционные заболевания глаз, а также нарушения в работе желез внутренней секреции, печени, почек и других органов.Иногда на состояние глазного яблока влияет вредная привычка, неправильный образ жизни, постоянное воздействие вредных химических веществ.
Деструкция стекловидного тела: диагностика и лечение
Сначала проконсультируйтесь с опытным офтальмологом. Как правило, для постановки окончательного диагноза врач должен осмотреть глазное дно, сделать некоторые лабораторные исследования и провести ультразвуковое исследование. Только тогда он определит не только наличие заболевания, но и стадию его развития.На сегодняшний день существует несколько методов лечения деструкции:
- Если нет серьезной угрозы для зрения, врач назначит прием витаминов и некоторых стимулирующих препаратов.

- Помните, что при таком заболевании нужно придерживаться исключительно здорового образа жизни, отказаться от вредных привычек и регулярно проходить обследования.
- Если состояние глазного яблока более серьезное, возможно, врач назначит витрэктомию — это хирургический метод лечения, суть которого заключается в частичном иссечении стекловидного тела и заполнении свободного пространства специальным раствором.Если разрушение сказывается на состоянии других элементов глаза, они также требуют лечения — например, иногда необходимо пересадить искусственный хрусталик глаза.
На сегодняшний день существует еще и безопасный, и безболезненный метод — витреолиз. С помощью лазерного луча врач разрушает плавающие внутри частицы и волокна, не нарушая целостности стекловидного тела. К сожалению, эта методика не слишком распространена и проводится только в некоторых специализированных клиниках.
Может ли стресс привести к повреждению сетчатки?
Стресс — это эмоциональная реакция, которую мы испытываем как мысленно, так и физически в опасных, антагонистических, разочаровывающих или интенсивных ситуациях.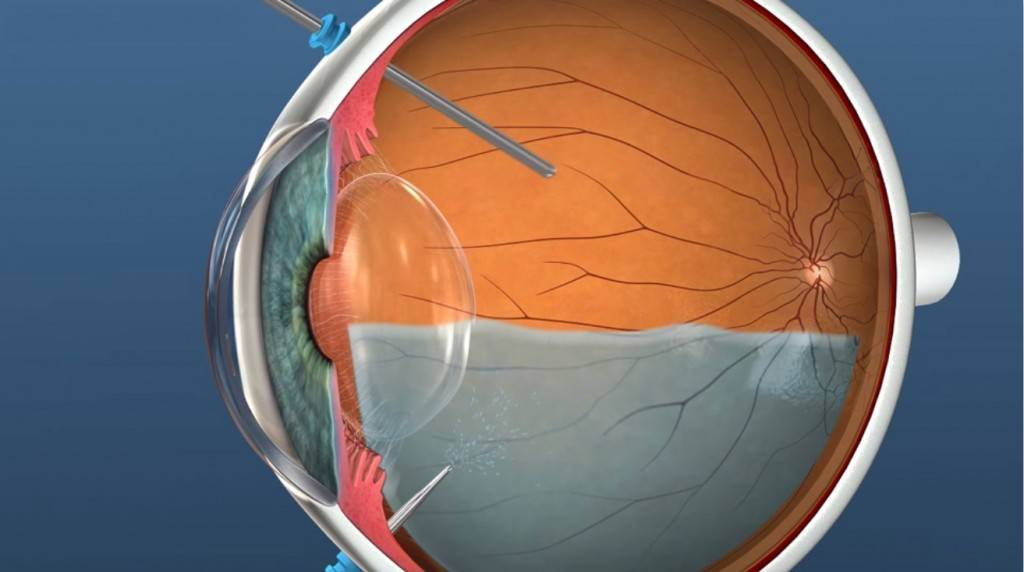 Это больше, чем просто ощущение, это может оказать глубокое влияние на все аспекты нашего здоровья. Но может ли это повредить сетчатку?
Это больше, чем просто ощущение, это может оказать глубокое влияние на все аспекты нашего здоровья. Но может ли это повредить сетчатку?
Биология стресса
Когда мы сталкиваемся с ситуацией, вызывающей стресс, наш мозг запускает сигнал тревоги, который резонирует по всему телу через нервную систему и наши гормоны.Во время стресса главным гормоном является кортизол, который повышает уровень глюкозы в кровотоке и увеличивает способность мозга усваивать глюкозу. Кортизол также ограничивает другие системы, включая иммунную и пищеварительную системы.
Эта сложная система биологической сигнализации разработана, чтобы помочь нам выжить во времена опасности или бедствия. Как только предполагаемая угроза исчезнет, системы организма должны вернуться в нормальное состояние. Таким образом, короткие всплески стресса часто считаются здоровыми, поскольку они могут подтолкнуть нас к тому, чтобы спастись, уложиться в сжатые сроки или забить победный гол в игре.
Хронический стресс и здоровье
Постоянный или хронический стресс может иметь значительные и негативные последствия для организма. Одними из наиболее распространенных физических проявлений длительного стресса являются проблемы со сном, хронические головные боли и проблемы с пищеварением. Хронический стресс также связан с обострением серьезных проблем со здоровьем, включая болезни сердца, ожирение, диабет и высокое кровяное давление.
К сожалению, хронический стресс является обычным явлением для современного человека.Исследования показывают, что мы, наряду с другими приматами, такими как бабуины, чаще, чем любое другое животное, страдаем от состояния, связанного со стрессом. Это потому, что мы социальные существа с высоким уровнем интеллекта и большим количеством свободного времени. Энергия, которую наши предки когда-то тратили на защиту от хищников и решение других потенциально фатальных препятствий, теперь тратится на беспокойство по поводу экзистенциальных или абстрактных проблем, многие из которых удерживают нас в низком состоянии хронического стресса.
Стресс и сетчатка
Хронический стресс представляет собой в основном косвенную угрозу для сетчатки. Например, пожилые пациенты, у которых есть сосудистые заболевания, такие как высокое кровяное давление, уже подвержены риску серьезных заболеваний сетчатки, таких как возрастная дегенерация желтого пятна или окклюзия вены сетчатки. Поскольку хронический стресс может усугубить эти состояния, он также может увеличить вероятность развития серьезной проблемы с сетчаткой. Точно так же у диабетиков продолжительные периоды повышенного стресса могут повлиять на уровень сахара в крови и, возможно, привести к диабетической ретинопатии.
Узнать больше
Стресс может прямо или косвенно привести к множеству проблем со здоровьем по всему телу. Хотя полностью избавиться от стресса невозможно, важно, чтобы мы научились справляться с ним и как можно больше контролировать его. Если вам уже поставили диагноз серьезное заболевание сетчатки или вы находитесь в группе риска, свяжитесь с Austin Retina, чтобы узнать больше о борьбе со стрессом и других советах по здоровью сетчатки.
Может ли стресс и беспокойство вызывать проблемы со зрением?
Стресс и тревога часто сопровождаются множеством нежелательных физических симптомов, включая проблемы со зрением.Общие симптомы зрения, связанные со стрессом, могут включать сухость глаз, напряжение глаз, глазные спазмы, помутнение зрения и светочувствительность. Эти симптомы обычно проходят после того, как стрессовая ситуация проходит, но могут продолжаться на регулярной основе у людей, которые испытывают хронический стресс или тревогу. Стресс также может усугубить такие состояния, как диабет и высокое кровяное давление, которые потенциально могут вызвать или усугубить заболевания сетчатки и желтого пятна.
Может ли стресс вызвать отслоение сетчатки?
Стресс сам по себе не может вызвать отслоение сетчатки.Отслоение сетчатки чаще всего вызвано старением или травмой глаза.
Может ли стресс вызвать отслойку заднего стекловидного тела?
Как и в случае отслоения сетчатки, стресс сам по себе не может вызвать задней отслойки стекловидного тела (PVD). PVD — это просто нормальный процесс старения, при котором гель стекловидного тела, заполняющий глаз, отделяется от задней части глаза.
PVD — это просто нормальный процесс старения, при котором гель стекловидного тела, заполняющий глаз, отделяется от задней части глаза.
Специалист по кровоизлиянию в стекловидное тело — Верхний Ист-Сайд, Нью-Йорк, Нью-Йорк, и Форест-Хиллз, Форест-Хиллз, Нью-Йорк: Retina Associates, Нью-Йорк: Специалист по сетчатке
Что такое кровоизлияние в стекловидное тело?
Кровоизлияние в стекловидное тело — это кровотечение из гелеобразного вещества, заполняющего глаз.Кровь может блокировать попадание света на сетчатку и вызывать изменения зрения. Если у вас сильное кровотечение в глазу, это может привести к полной потере зрения.
Что вызывает кровоизлияние в стекловидное тело?
Диабетическая ретинопатия — наиболее частая причина кровоизлияния в стекловидное тело. Плохо контролируемый уровень сахара в крови повреждает ваши кровеносные сосуды, особенно мелкие кровеносные сосуды в глазу. Это повреждение может в конечном итоге вызвать кровотечение, ведущее к кровоизлиянию в стекловидное тело.
Кровоизлияние в стекловидное тело может также развиться в результате травмы глаза, головы или повреждения сетчатки, например, отверстия.
Каковы симптомы кровоизлияния в стекловидное тело?
Кровоизлияние в стекловидное тело может развиться очень быстро и неожиданно. К общим симптомам относятся:
- Затуманенное зрение
- Увеличение числа плавающих объектов
- Вспышки света
Вы можете заметить, что эти симптомы усиливаются, когда вы впервые встаете утром. Это потому, что кровь осела в задней части глаза, что привело к резким визуальным изменениям.
Какие методы лечения кровоизлияния в стекловидное тело?
Лечение кровоизлияния в стекловидное тело зависит от тяжести кровотечения.Команда Retina Associates из Нью-Йорка составляет индивидуальные планы лечения, основанные на основной причине кровотечения и ваших симптомах.
Если кровотечение слабое или полностью прекратилось, ваш специалист по сетчатке может порекомендовать наблюдение и предложить рекомендации, как минимизировать визуальные изменения.
Они также могут направить лечение первопричины. Например, если кровоизлияние в стекловидное тело вызвано диабетической ретинопатией, они могут порекомендовать лечение для улучшения здоровья глаз, такое как лазерная фотокоагуляция или инъекция лекарства в глаз.
Ваш офтальмолог может также предложить витрэктомию — хирургическую процедуру, которая требует удаления стекловидного тела из вашего глаза и устранения источника кровотечения. У Retina Associates of New York есть современный хирургический центр, расположенный по соседству с офисом на Манхэттене, где хирурги проводят все необходимые глазные процедуры.
Кровоизлияние в стекловидное тело может вызвать внезапные изменения вашего зрения. Для получения экспертной помощи и оценки свяжитесь с Retina Associates of New York по телефону или через Интернет сегодня.
.


