Аритмия: опасность и способы диагностики
По статистике ВОЗ, сердечно-сосудистые заболевания являются основной причиной смерти и даже пандемия коронавируса не изменила этого факта. Если вы подозреваете у себя наличие проблемы с сердцем, следует обязательно обратиться к врачу. Обычно первое обследование – это ЭКГ.
Аритмия – это изменения нормальной частоты, регулярности и источника возбуждения сердца. При этом далеко не любое учащенное сердцебиение можно отнести к аритмии. Например, сердце начинает биться чаще при эмоциональных или физических нагрузках. Ведь любому знакомо ощущение, когда сердце стучит чаще при испуге, от стресса, да просто после попытки догнать автобус или взбежать по высокой лестнице. Однако, если вы порой замечаете за своим сердцем неладное, не стоит отмахиваться от подозрений.
Аритмии различных видов, а также другие заболевания, влияющие на работу сердца, могут вызывать проблемы с кровообращением. Врач экспресс-клиник Confido доктор Андреас Абель говорит, что последствиями аритмии могут стать общая слабость и обессиленность, отеки, вызванные сердечной недостаточностью или осложнения, вызванные тромбами, например, инсульт.
Контролировать частоту сердечных сокращений помогут смарт-часы. Отслеживая частоту пульса и сердечный ритм, вы можете тренироваться с умом, не перегружая тело и сердце. «Тем не менее, возможную проблему со здоровьем, выявленную смарт-устройством, обязательно нужно проверить в лечебном учреждении с помощью соответствующего оборудования и тестов», – говорит Абель.
Простое и безопасное исследование
Лучшим помощником для диагностики проблем с сердечным ритмом является электрокардиограмма (ЭКГ), то есть съемка сердца, благодаря которой записываются электрические сигналы сердца. Кроме того, исследование помогает выявить проблемы с кровоснабжением сердца (например, инфаркт) и его избыточную нагрузку.
Кроме того, исследование помогает выявить проблемы с кровоснабжением сердца (например, инфаркт) и его избыточную нагрузку.
Исследование безболезненно для пациента. Доктор Абель объясняет, что при электрокардиографии пациент с обнаженной верхней частью тела лежит на спине. Для регистрации электроимпульсов сердца электроды прикрепляются к рукам, ногам и к груди. Во время процедуры нельзя двигаться. Регистрация импульсов выполняется быстро – вместе с подготовкой исследование ЭКГ обычно занимает 5-10 минут.
«В случае острого сердечного заболевания, такого как аритмия или инфаркт, изменения происходят быстро, так что электрокардиография сердца – самое важное и первостепенное обследование для диагностики таких заболеваний», – говорит врач. Он добавляет, что для точной интерпретации ЭКГ требуется опыт. Правильно прочитать электрокардиограмму может только врач.
«Если вы подозреваете у себя проблемы с сердцем, обследование можно пройти во всех экспресс-клиниках без предварительной регистрации. Если вы собираетесь обратиться к врачу со своими подозрениями, помните, что ранее сделанные электрокардиограммы помогут ему вынести правильный вердикт, не забудьте взять их с собой», – говорит Абель. Он поясняет, что различные заболевания могут вызывать изменения, которые остаются надолго в кривых записи биотоков.
Если вы собираетесь обратиться к врачу со своими подозрениями, помните, что ранее сделанные электрокардиограммы помогут ему вынести правильный вердикт, не забудьте взять их с собой», – говорит Абель. Он поясняет, что различные заболевания могут вызывать изменения, которые остаются надолго в кривых записи биотоков.
Нагрузочный тест и Холтер-ЭКГ – больше уверенности
Некоторые патологические изменения, например, нарушения кровообращения, часто не отображаются в кардиограмме, записанной в состоянии покоя. По мнению врача, при подозрении на подобное заболевание, помимо обычной ЭКГ следует выполнять тест на нагрузкой на сердце. Чаще всего для этого используют велоэргометр или специальную беговую дорожку. Тест с подготовкой и восстановлением обычно длится до 30 минут. Лучше всего для процедуры одеться в легкую спортивную одежду и обувь. «Тест позволяет оценить, насколько высокую нагрузку переносит пациент, как реагируют на нагрузку пульс и давление, а также возникают ли во время упражнений изменения в сердечной мышце, которые указывают на нарушение кровообращения», – подтверждает Абель.
Зачастую нарушения сердечного ритма, которые проявляются лишь эпизодически, не отражаются на ЭКГ, снятой в клинике в течение короткого периода времени. «В этом случае, помимо амбулаторного ЭКГ, нужно провести суточный мониторинг (суточное мониторирование ЭКГ по методу Холтер), при котором прикрепленные к телу электроды и специальное устройство записывают электрокардиограмму в течение всего периода измерения», – говорит Абель. После измерения кардиолог просматривает исследование и оценивает наличие аритмии. Узнайте больше об исследовании Холтер-ЭКГ тут
Снижение риска равно смене образа жизни
Факторы риска в слуачае аритмии точно такие же, как и для сердечно-сосудистых заболеваний в целом. По словам врача, контроль над массой тела, регулярная физическая активность, нормальное кровяное давление и уровень сахара в крови помогают снизить риски. Двигайтесь каждый день не менее 20-30 минут в день (не менее 150 минут в неделю). Выберите подходящий вид физической активности – быстрая ходьба, езда на велосипеде, бег, плавание и т. д.
д.
Следует избегать курения. При некоторых аритмиях играет роль наследственность, риск нарушения сердечного ритма с возрастом обычно увеличивается. Для людей старше 50 лет риск развития мерцательной аритмии удваивается каждые десять лет.
Статья вышла на портале MK-Эстония, mke.ee
450106, г.Уфа, ул. Ст. Кувыкина, 96. e-mail: [email protected]
Добрый день, дорогие друзья! Сегодня мы поговорим о нарушениях ритма сердца.
Фибрилляция предсердий (ФП) – одно из самых частых нарушений ритма сердца, для которого характерна нерегулярность, хаотичность сокращений сердца. Фибрилляция предсердий может наблюдаться как у молодых, так и у пожилых лиц, но с возрастом распространенность ФП значительно увеличивается.
Как известно, сердце состоит из отдельных мышечных волокон, которые в норме сокращаются синхронно, чтобы обеспечить постоянный ток крови по сосудам. При фибрилляции предсердий мышечные волокна предсердий начинают сокращаться неравномерно, что приводит к нерегулярности сокращений желудочков сердца: сердечный ритм то ускоряется, то замедляется.
Причины фибрилляции предсердий многообразны. Часто ФП развивается на фоне артериальной гипертензии, поскольку длительное повышение артериального давления приводит к увеличению камер сердца, растяжению мышечных волокон и, в конечном итоге, их нерегулярному сокращению. Развивается аритмия и при других заболеваниях сердца: ишемической болезни сердца, врожденных и приобретенных пороках сердца, миокардите – воспалении сердечной мышцы и постмиокардитическом кардиосклерозе. Из других причин следует отметить болезни щитовидной железы, приводящие к нарушению выработки гормонов, злоупотребление алкоголем, а также бесконтрольное применение мочегонных препаратов и различных растительных средств для похудания, которые вымывают из организма калий. Риск аритмии повышается у лиц, страдающих ожирением и сахарным диабетом. Но в ряде случаев, чаще у молодых, аритмия может возникать без каких-либо видимых причин.
Выделяют три формы аритмии: пароксизмальную, персистирующую и постоянную, или хроническую.
Проявления заболевания зависят от формы аритмии и от особенностей организма больного.
Диагностическая картина ФП может варьировать от ощущения сердцебиения, одышки, тяжести в груди, расстройства сна, сонливости, слабости, психосоциальных расстройств, чувство нехватки воздуха, головокружение. У ряда пациентов отмечается полное отсутствие какой-либо симптоматики, и первым проявлением ФП могут быть ишемический инсульт.
Основной метод диагностики фибрилляции предсердий – электрокардиограмма. Если аритмия возникает эпизодически, может потребоваться мониторирование ЭКГ с помощью специального прибора, который регистрирует кардиограмму в течение суток. Помимо этого, врач может назначить другие обследования: эхокардиографию, позволяющую оценить размеры и структуру сердца, анализы крови на уровень холестерина, сахара, калия, исследование функции щитовидной железы.
Фибрилляция предсердий может привести к развитию сердечной недостаточности, особенно при большой частоте сердечного ритма, что проявляется появлением одышки при нагрузках, а иногда и в покое, отеками, повышенной утомляемостью. Другим серьезным осложнением является инсульт, причиной которого является частое образование при фибрилляции предсердий тромбов в камерах сердца. Поэтому очень важно ее лечить!
Лечение фибрилляции предсердий зависит от ее формы. При пароксизмальной форме целью лечения является восстановление нормального ритма сердца. Для этого пациенту вводят специальные антиаритмические препараты, а после нормализации ритма для его поддержания назначается их прием в виде таблеток. Если приступ аритмии длится более двух суток, вначале назначаются препараты, уменьшающие свертываемость крови – антикоагулянты, которые предупреждают образование тромбов. В этом случае восстанавливать ритм можно только через 4 недели лечения. Если антиаритмические препараты оказываются неэффективными, применяется электрическая кардиоверсия: сердечный ритм восстанавливается разрядом электрического тока, который как бы «перезапускает» сердце.
При хронической форме аритмии лечение направлено на урежение сердечного ритма и предупреждение развития осложнений: инсульта и сердечной недостаточности. Для этого назначается постоянный прием препаратов, включающих бета-адреноблокаторы или антагонисты кальция, дигоксин, а также антикоагулянты. Также врач может назначить препараты для нормализации давления, мочегонные, снижающие холестерин.
Какого образа жизни следует придерживаться пациентам с фибрилляцией предсердий? Рекомендуется исключить физические и эмоциональные перегрузки, придерживаться принципов здорового питания, оказаться от приема алкоголя и курения. Необходимо регулярно принимать назначенные врачом препараты, не делая перерывы в лечении и не изменяя самостоятельно дозу и режим приема. При назначении антикоагулянтных препаратов необходим регулярный контроль показателей свертывания крови для того, чтобы подобрать правильную дозу и снизить риск развития кровотечения.
При соблюдении рекомендаций врача прогноз мерцательной аритмии благоприятный. Современные методы лечения позволяют предупреждать развитие осложнений и поддерживать хорошее качество жизни на протяжении многих лет.
Современные методы лечения позволяют предупреждать развитие осложнений и поддерживать хорошее качество жизни на протяжении многих лет.
Будьте здоровы!
Нарушения ритма сердца | ЧУЗ «КБ «РЖД-Медицина» им. Н.А. Семашко»
Нарушение ритма сердца является одной из наиболее частых причин госпитализации в кардиологическое отделение. Аритмии могут являться осложнением практически всех заболеваний сердца (ишемическая болезнь сердца, артериальная гипертония, кардиомиопатия, ревматическая болезнь, и т.д.).
- проявлением заболеваний других органов и систем (заболевания щитовидной железы, желудочно-кишечного тракта, органов дыхания, и т.д.)
- самостоятельным заболеванием.
Аритмия может протекать и практически бессимптомно, и со значительным ухудшением качества жизни, что в последнем случае приводит к частым визитам к терапевту и кардиологу, повторным госпитализациям в специализированные кардиологические отделения стационаров.
Важно, что прогноз аритмии во многом зависит от причины, ее вызвавшей, а также от вида аритмии. Наиболее опасны некоторые виды нарушений ритма, возникающие у пациентов, перенесших острый инфаркт миокарда, пациентов с сердечной недостаточностью, с кардиомиопатиями. С другой стороны при этих же заболеваниях возможны нарушения сердечного ритма, не представляющие опасность для пациентов. Поэтому самолечение при аритмиях недопустимо. Медикаменты, используемые при лечении этого заболевания, в том числе и высокоэффективные показаны далеко не всем больным. В случаях, когда аритмия не угрожает жизни больного назначение противоаритмических препаратов может принести больше вреда, чем пользы.
Наиболее опасны некоторые виды нарушений ритма, возникающие у пациентов, перенесших острый инфаркт миокарда, пациентов с сердечной недостаточностью, с кардиомиопатиями. С другой стороны при этих же заболеваниях возможны нарушения сердечного ритма, не представляющие опасность для пациентов. Поэтому самолечение при аритмиях недопустимо. Медикаменты, используемые при лечении этого заболевания, в том числе и высокоэффективные показаны далеко не всем больным. В случаях, когда аритмия не угрожает жизни больного назначение противоаритмических препаратов может принести больше вреда, чем пользы.
При выявлении нарушений ритма необходим комплекс диагностических мероприятий, позволяющий выявить причины аритмии, прогноз и необходимость назначения медикаментозной, либо немедикаментозной терапии. Во многих случаях устранение причин аритмии может позволить купировать и само нарушение ритма без назначения сильнодействующих антиаритмических препаратов. Так правильно подобранное лечение ишемической болезни сердца, артериальной гипертонии часто купирует аритмию. Если нарушение ритма вызвано заболеванием щитовидной железы (тиреотоксикоз), то специальное лечение этой патологии практически всегда купирует аритмию. Нередко нарушения ритма провоцируются обострением язвенной болезни желудка или 12-ти перстной кишки, эффективное лечение которых также приводит к устранению аритмии.
Если нарушение ритма вызвано заболеванием щитовидной железы (тиреотоксикоз), то специальное лечение этой патологии практически всегда купирует аритмию. Нередко нарушения ритма провоцируются обострением язвенной болезни желудка или 12-ти перстной кишки, эффективное лечение которых также приводит к устранению аритмии.
Однако, во многих случаях пациентам необходимо назначение специальных антиаритмических препаратов. В случае неэффективности антиаритмической медикаментозной терапии или ее непереносимости лечение должно быть продолжено в специализированных клиниках, в которых хирург-аритмолог путем специального катетерного исследования выявляет зоны сердечной мышцы, ответственные за возникновение аритмии и вызывает их деструкцию, тем самым ликвидируя нарушение ритма. Существуют виды аритмий, где этот метод лечения высокоэффективен, но, к сожалению, при некоторых часто встречающихся видах нарушений ритма он не превосходит по эффективности медикаментозное лечение.
На базе кардиологического отделения ДКБ им. Н.А. Семашко возможно пройти комплексное обследование с целью выявления происхождения аритмии, оценки ее прогноза, подбора антиаритмической терапии. В процессе обследования лиц этой патологией проводится суточное мониторирование ЭКГ, чреспищеводное электрофизиологическое исследование (при определенных показаниях), выполняется эхокардиография, велоэргометрия, обследование других органов и систем. В отделении имеется весь арсенал современных антиаритмических препаратов. При остро возникших нарушениях ритма в блоке интенсивной терапии проводится экстренное восстановление ритма медикаментозными и немедикаментозными средствами с дальнейшим подбором противорецидивной антиаритмической терапии. Лечение проводится согласно рекомендациям Всероссийского научного общества кардиологов и соответствует Российским стандартам оказания специализированной кардиологической помощи.
Н.А. Семашко возможно пройти комплексное обследование с целью выявления происхождения аритмии, оценки ее прогноза, подбора антиаритмической терапии. В процессе обследования лиц этой патологией проводится суточное мониторирование ЭКГ, чреспищеводное электрофизиологическое исследование (при определенных показаниях), выполняется эхокардиография, велоэргометрия, обследование других органов и систем. В отделении имеется весь арсенал современных антиаритмических препаратов. При остро возникших нарушениях ритма в блоке интенсивной терапии проводится экстренное восстановление ритма медикаментозными и немедикаментозными средствами с дальнейшим подбором противорецидивной антиаритмической терапии. Лечение проводится согласно рекомендациям Всероссийского научного общества кардиологов и соответствует Российским стандартам оказания специализированной кардиологической помощи.
Мерцательная аритмия. Диагностика — ФГБУ «НМИЦ ТПМ» Минздрава России
Мерцательная аритмия, или фибрилляция предсердий, – наиболее распространенное нарушение сердечного ритма. Мерцательная аритмия увеличивает риск инсульта, и важно вовремя ее диагностировать и начать лечение.
Мерцательная аритмия увеличивает риск инсульта, и важно вовремя ее диагностировать и начать лечение.
О мерцательной аритмии и диагностике заболевания рассказал заместитель главного врача консультативно-диагностического центра по организационно-методической работе, член регулярного совета по инсульту Европейского общества кардиологов, врач-кардиолог Александр Владимирович Емельянов.
Александр Владимирович, как проявляется мерцательная аритмия?
Вначале нерегулярный пульс кажется пароксизмальным, то есть вызывает внезапные приступы. Это может длиться минуты, часы или даже дни, пока ритм сердца самопроизвольно не нормализуется. Со временем приступы могут перерасти в хроническую фибрилляцию предсердий, которая требует медицинского лечения, поскольку приступы больше не заканчиваются спонтанно. Люди могут привыкать к нерегулярному пульсу – и заболевание остается незамеченным. Поэтому для предотвращения инсульта важно обнаруживать даже бессимптомные фазы мерцательной аритмии. Пациенты с тихими эпизодами фибрилляции предсердий нуждаются в специальной лекарственной терапии для профилактики инсульта.
Пациенты с тихими эпизодами фибрилляции предсердий нуждаются в специальной лекарственной терапии для профилактики инсульта.
Что происходит в сердце во время мерцательной аритмии?
Мышцы предсердия перестают ритмично сокращаться и синхронизироваться друг с другом. Это означает, что слишком мало крови достигает камер сердца, и способность сердца перекачивать кровь в целом снижается. Существует также вероятность того, что в определенных областях предсердий кровь может застаиваться, что приводит к образованию тромбов. Эти сгустки крови могут вызвать инсульт, если они забивают кровеносный сосуд в мозге. Мерцательная аритмия может привести к учащенному сердцебиению (тахикардии), нерегулярному сердцебиению и в некоторых случаях к замедлению сердечного ритма (брадикардия).
Как обнаружить фибрилляцию предсердий?
Самый простой способ обнаружить мерцательную аритмию – это проверить свой пульс. Если ваш пульс нерегулярный, высока вероятность фибрилляции предсердий. С помощью электрокардиограммы или ЭКГ можно быстро подтвердить подозрение на хроническую фибрилляцию предсердий.
С помощью электрокардиограммы или ЭКГ можно быстро подтвердить подозрение на хроническую фибрилляцию предсердий.
Случаи пароксизмальной фибрилляции предсердий, однако, гораздо сложнее проверить, так как ЭКГ должна быть выполнена во время приступа, чтобы обнаружить его. Поэтому для пациентов с пароксизмальной фибрилляцией предсердий обследование в кабинете врача может не привести к окончательному диагнозу. В этом случае выполняется долгосрочная ЭКГ (мониторирование ЭКГ по Холтеру), когда сердечная деятельность измеряется в течение 24 часов или дольше. Если результат все еще неоднозначен, может быть установлен кардиомонитор для постановки правильного диагноза.
Если вы почувствовали неладное, обнаружили у себя сбои пульса, следует немедленно обратиться к врачу-кардиологу. Специалист назначит вам необходимые исследования и определит тактику лечения. Записаться к врачу-кардиологу консультативно-диагностического центра Национального медицинского исследовательского центра терапии и профилактической медицины Минздрава России можно по телефону 8 (495) 790-71-72.
Преждевременные сокращения желудочков (ПВХ): симптомы и причины
Обзор
Желудочковые аритмииПреждевременные сокращения желудочков (ЖЭ) являются наиболее частой причиной нерегулярного сердечного ритма. Сердцебиение создается электрическим сигналом, который исходит из области специализированных клеток в верхней правой камере сердца, правом предсердии. Электрический сигнал проходит через сердце к атриовентрикулярному (АВ) узлу, кластеру специализированных клеток в центре сердца.От AV-узла сигнал проходит по специальным волокнам, встроенным в стенки сердца, к желудочкам, нижним камерам. Когда электрический ток поступает в желудочки, он заставляет их сокращаться и перекачивать богатую кислородом кровь в тело.
Что такое преждевременные сокращения желудочков?
Преждевременное сокращение желудочков (PVC) — это слишком раннее сердцебиение, которое возникает в желудочках и нарушает нормальный ритм сердца. Паттерн — это нормальный ритм, дополнительный бит (PVC), небольшая пауза, а затем более сильный, чем обычно, ритм. Сердце наполняется кровью во время паузы после ЖЭ, придавая следующему удару дополнительную силу. Эта закономерность может возникать случайно или через определенные промежутки времени.
Сердце наполняется кровью во время паузы после ЖЭ, придавая следующему удару дополнительную силу. Эта закономерность может возникать случайно или через определенные промежутки времени.
Симптомы и причины
Каковы симптомы ПВС?
Когда ЖЭ возникает как однократное преждевременное сердцебиение, пациенты могут описать это ощущение как «сердцебиение» или «пропущенное сердцебиение». Удары, следующие за ПВХ, могут быть достаточно сильными, чтобы вызвать боль или дискомфорт в груди. Люди, у которых есть частые или несколько из них, могут испытывать трепетание в груди или шее.Если ЖЭ случаются достаточно часто, чтобы снизить насосную способность сердца, человек может испытывать слабость, головокружение или обморок.
Что вызывает ЖЭ?
ЖЭ могут быть у здоровых людей любого возраста. В большинстве случаев нерегулярных ЖЭ основная причина не может быть идентифицирована. ЖЭ, которые возникают часто или в течение более длительных периодов времени, с большей вероятностью связаны с сердечными заболеваниями, травмами сердца или другими не сердечными состояниями, такими как химический дисбаланс в организме. Некоторые лекарства, алкоголь, запрещенные наркотики и высокий уровень адреналина из-за стресса, физических упражнений или кофеина также могут вызывать ЖЭ.
Некоторые лекарства, алкоголь, запрещенные наркотики и высокий уровень адреналина из-за стресса, физических упражнений или кофеина также могут вызывать ЖЭ.
Диагностика и тесты
Как диагностируется ЖЭ?
PVC может быть трудно диагностировать, потому что они возникают с непредсказуемыми интервалами. В большинстве случаев врачу трудно обнаружить ЖЭ во время обычного медицинского осмотра, если только пациент не имеет таковой во время обследования или других признаков структурных проблем с сердцем. У людей без каких-либо заболеваний сердца ЖЭ часто обнаруживаются случайно во время рутинной электрокардиограммы (ЭКГ). У пациентов с известным заболеванием сердца ЖЭ могут быть обнаружены во время других диагностических тестов для этого состояния.
Пациенту с симптомами ЖЭ, который обращается к кардиологу, будет сделана ЭКГ — стандартный тест для диагностики ЖЭ. Это относительно недорого, неинвазивно и точно. Монитор Холтера, портативная ЭКГ, обеспечивающая непрерывную запись в течение 24 или 48 часов, может использоваться для пациентов, у которых наблюдается ЖЭ хотя бы один раз в день. Информация с холтеровского монитора очень полезна для определения частоты ЖЭ и корреляции таких симптомов, как обморок или головокружение, с аритмией.
Информация с холтеровского монитора очень полезна для определения частоты ЖЭ и корреляции таких симптомов, как обморок или головокружение, с аритмией.
Американский колледж кардиологии рекомендует некоторым пациентам с ЖЭ, диагностированным с помощью ЭКГ, пройти тестирование с физической нагрузкой — измерение частоты сердечных сокращений, когда пациент ходит на беговой дорожке.
В крупных кардиологических центрах, таких как клиника Кливленда, также есть другие специализированные тесты более высокого уровня, доступные для пациентов с ЖЭ, которые не могут пройти тесты с физической нагрузкой или которые имеют высокий риск более сложных проблем с сердцем. Эти тесты могут включать в себя МРТ сердца, КТ сердца, ОФЭКТ перфузии миокарда, коронарную ангиографию или электрофизиологическое исследование.Электрофизиологи Cleveland Clinic ежегодно проводят более 4000 диагностических тестов на аритмию, что является одним из самых больших объемов пациентов в стране.
Ведение и лечение
Как обрабатывают ПВХ?
Людям, у которых периодически возникают ЖЭ без других симптомов, сердечных заболеваний или структурных проблем, лечение не требуется. Вы можете помочь контролировать свои ЖЭ, уменьшив или исключив потребление кофеина, табака и алкоголя, а также снизив уровень стресса и беспокойства.Если лекарства, которые вы регулярно принимаете, вызывают у вас ЖЭ, обсудите возможное изменение приема лекарств со своим врачом. Когда ЖЭ вызваны какой-либо формой, сердечным заболеванием или структурной аномалией, лечение этой проблемы часто приводит к исчезновению ЖЭ.
Вы можете помочь контролировать свои ЖЭ, уменьшив или исключив потребление кофеина, табака и алкоголя, а также снизив уровень стресса и беспокойства.Если лекарства, которые вы регулярно принимаете, вызывают у вас ЖЭ, обсудите возможное изменение приема лекарств со своим врачом. Когда ЖЭ вызваны какой-либо формой, сердечным заболеванием или структурной аномалией, лечение этой проблемы часто приводит к исчезновению ЖЭ.
Бета-блокатор может быть назначен пациентам с ЖЭ, страдающим сердечной недостаточностью или перенесшим сердечный приступ. Бета-адреноблокаторы — безопасные и эффективные препараты, которые часто используются для лечения сердечных аритмий. Другие препараты, которые можно использовать для лечения частых ЖЭ, включают блокаторы кальциевых каналов и другие более сильнодействующие препараты, влияющие на сердечный ритм.
Абляция — еще один вариант лечения для некоторых пациентов с частыми или длительными ЖЭ. В абляционной терапии радиочастотные волны используются для испарения крошечных количеств ткани в области сердца, где возникает лишнее сокращение. Это минимально инвазивная процедура, предназначенная для пациентов, которые не переносят бета-адреноблокаторы, у которых лекарства неэффективны или которые не могут соблюдать длительную медикаментозную терапию. Интервенционные кардиологи Cleveland Clinic являются экспертами в области радиочастотной абляции, ежегодно выполняя более 1200 абляций для лечения различных аритмий.
Это минимально инвазивная процедура, предназначенная для пациентов, которые не переносят бета-адреноблокаторы, у которых лекарства неэффективны или которые не могут соблюдать длительную медикаментозную терапию. Интервенционные кардиологи Cleveland Clinic являются экспертами в области радиочастотной абляции, ежегодно выполняя более 1200 абляций для лечения различных аритмий.
Пациентам с сердечными заболеваниями, у которых часто возникают ЖЭ или повышенные ЖЭ во время физических упражнений, может быть целесообразна ангиопластика или шунтирование.
Профилактика
Кто подвержен риску заражения ЖЭ?
Почти каждый человек когда-либо страдает ЖЭ, от детства до взрослого возраста. В исследовании, проведенном среди здоровых военнослужащих, частота ЖЭ составила 0,5% среди лиц моложе 20 лет и 2,2% среди лиц старше 50 лет. Это исследование показывает рост ЖЭ, как и при всех типах сердечных аномалий. ритмы — это происходит с возрастом.ЖЭ чаще встречаются у пожилых людей и у людей с сердечными заболеваниями, в том числе перенесшими сердечный приступ в анамнезе. Люди с семейным анамнезом сердечных аритмий (нарушений сердечного ритма) также имеют более высокий риск ЖЭ.
Люди с семейным анамнезом сердечных аритмий (нарушений сердечного ритма) также имеют более высокий риск ЖЭ.
Какие риски связаны с ПВХ?
Большинство ЖЭ возникают нечасто и являются доброкачественными. Частые ЖЭ могут увеличить риск развития других, более серьезных сердечных аритмий. Лица с частыми ЖЭ, имеющие основное заболевание сердца, структурные аномалии сердца или перенесшие сердечный приступ в прошлом, имеют более высокий риск смерти.
Жить с
Когда мне следует обратиться за медицинской помощью по поводу ЖЭ?
У большинства людей ЖЭ возникают нечасто и являются доброкачественными. Вам следует проконсультироваться с кардиологом, если вы испытываете частые, регулярные или продолжительные (продолжительностью несколько минут) ЖЭ, ЖЭ, структурные проблемы с сердцем, сердечные заболевания или сердечный приступ.
Ресурсы
Лечащие врачи
Доктора различаются по квалификации из-за разницы в обучении и опыте; больницы различаются по количеству доступных услуг. Чем сложнее ваша медицинская проблема, тем сильнее становятся эти различия в качестве и тем больше они имеют значение. Очевидно, что врач и больница, которые вы выберете для комплексной специализированной медицинской помощи, будут иметь прямое влияние на то, насколько хорошо вы себя чувствуете. Чтобы помочь вам сделать этот выбор, ознакомьтесь с результатами нашего Института сердца, сосудов и торакальной системы семьи Миллер.
Чем сложнее ваша медицинская проблема, тем сильнее становятся эти различия в качестве и тем больше они имеют значение. Очевидно, что врач и больница, которые вы выберете для комплексной специализированной медицинской помощи, будут иметь прямое влияние на то, насколько хорошо вы себя чувствуете. Чтобы помочь вам сделать этот выбор, ознакомьтесь с результатами нашего Института сердца, сосудов и торакальной системы семьи Миллер.
Кливлендская клиника кардиологов и хирургов Института сердечно-сосудистой и торакальной хирургии
Выбор врача для лечения нарушения сердечного ритма зависит от того, на каком этапе диагностики и лечения вы находитесь.Следующие отделения и отделения Института сердца, сосудов и торакальной хирургии лечат пациентов с аритмией:
- Секция электрофизиологии и кардиостимуляции: кардиологическое обследование для медицинского управления или электрофизиологические процедуры или устройства — позвоните в кардиологию по бесплатному телефону 800.
 223.2273, добавочный номер 4-6697 или запишитесь на прием онлайн.
223.2273, добавочный номер 4-6697 или запишитесь на прием онлайн. - Отделение торакальной и сердечно-сосудистой хирургии: хирургическая оценка хирургического лечения фибрилляции предсердий, установка эпикардиального электрода и, в некоторых случаях, при необходимости, имплантация и удаление электрода и устройства.Для получения более подробной информации, пожалуйста, свяжитесь с нами.
- Вы также можете воспользоваться консультацией MyConsult «второе мнение» через Интернет.
Институт сердца, сосудов и грудной клетки имеет специализированные центры для лечения определенных групп пациентов:
Узнайте больше об экспертах, специализирующихся на диагностике и лечении аритмий.
Для молодых пациентов с нарушениями сердечного ритма:
См. Раздел «О нас», чтобы узнать больше о Семейном кардиологическом, сосудистом и торакальном институте Сиделла и Арнольда Миллеров.
Ресурсы и информация для пациентов
Контакты
Если вам нужна дополнительная информация, нажмите здесь, чтобы связаться с нами, поговорите в чате с медсестрой или позвоните медсестре по ресурсам и информации Института сердечно-сосудистых заболеваний и грудной клетки Миллер по телефону 216. 445.9288 или по бесплатному телефону 866.289.6911. Будем рады Вам помочь.
445.9288 или по бесплатному телефону 866.289.6911. Будем рады Вам помочь.
Стать пациентом
Варианты лечения
T
Направляющие обработкиДиагностические тесты
Диагностические тесты используются для диагностики аномального сердцебиения и определения наиболее эффективного метода лечения.
Анатомия
Веб-чаты
Наши веб-чаты и видеочаты дают пациентам и посетителям еще одну возможность задать вопросы и пообщаться с нашими врачами.
Видео
Интерактивные инструменты
Ссылки на ресурсы
Почему выбирают клинику Кливленда для лечения?
Наши результаты говорят сами за себя. Ознакомьтесь с нашими фактами и цифрами, и если у вас возникнут вопросы, не стесняйтесь их задавать.
Блокада сердца: типы, диагностика, лечение, наблюдение
Обзор
Патрик Дж.Чоу, доктор медицины, говорит о блокированных импульсах в сердцеЧто такое блокада сердца?
Блокада сердца — это проблема с электрической системой вашего сердца, которая заставляет ваше сердце биться и контролирует его частоту и ритм. Это состояние также называется атриовентрикулярной (АВ) блокадой или нарушением проводимости.
Это состояние также называется атриовентрикулярной (АВ) блокадой или нарушением проводимости.
Что произойдет, если у меня блокада сердца?
Обычно электрические сигналы проходят от верхних камер сердца (предсердий) к нижним камерам (желудочкам). Атриовентрикулярный узел — это скопление клеток, которые соединяют электрическую активность — подобно мосту — от верхних камер вашего сердца к нижним камерам.Если у вас блокада сердца, электрический сигнал не проходит через AV-узел в желудочки. В результате сердце не функционирует эффективно, а это означает, что ваше сердце бьется медленно или пропускает удары, и оно не может качать кровь через свои камеры и выводить ее в тело, как это делает нормальное сердце.
Какие виды блокады сердца?
Блокада сердца может быть первой, второй или третьей степени, в зависимости от степени нарушения электрического сигнала.
- Блокада сердца первой степени: Электрический импульс все еще достигает желудочков, но проходит через АВ-узел медленнее, чем обычно.
 Импульсы задерживаются. Это самый легкий тип сердечной блокады.
Импульсы задерживаются. Это самый легкий тип сердечной блокады. - Блок сердца второй степени подразделяется на две категории: Тип I и Тип II. При блокаде сердца второй степени импульсы периодически блокируются.
- Тип I, также называемый блокадой Мобица I или АВ-блокадой Венкебаха: Это менее серьезная форма блокады сердца второй степени. Электрический сигнал становится все медленнее и медленнее, пока ваше сердце не перестанет биться.
- Тип II, также называемый Мобитц Тип II: В то время как большинство электрических сигналов периодически достигает желудочков, некоторые — нет, и ваше сердцебиение становится нерегулярным и медленнее, чем обычно.
- Третья степень блокада сердца: Электрический сигнал от предсердий к желудочкам полностью заблокирован. Чтобы компенсировать это, желудочек обычно начинает сокращаться сам по себе, действуя как альтернативный кардиостимулятор, но сердцебиение медленнее, часто нерегулярно и ненадежно.
 Блок третьей степени серьезно влияет на способность сердца перекачивать кровь к вашему телу.
Блок третьей степени серьезно влияет на способность сердца перекачивать кровь к вашему телу.
Сердечная блокада серьезна или опасна?
Может быть.Тип сердечной блокады, ее расположение и тяжесть, а также симптомы варьируются от человека к человеку. Если не лечить, тяжелая блокада сердца может вызвать внезапную остановку сердца (сердце внезапно перестает биться), но чаще всего может вызвать головокружение или обмороки.
Кто подвержен риску сердечной блокады?
У вас может быть повышенный риск сердечной блокады, если:
- У вашей матери аутоиммунное заболевание, например волчанка.
- Вы старше. Риск сердечной блокады увеличивается с возрастом.
- У вас есть другие сердечные заболевания, включая ишемическую болезнь сердца, порок сердечного клапана.
- У вас врожденные пороки сердца.
- У вас болезнь сердца, включая ревматический порок сердца или саркоидоз.
- У вас гиперактивный блуждающий нерв (замедляет работу сердца).

- Вы принимаете лекарства, замедляющие проведение сердечных электрических импульсов, в том числе некоторые сердечные лекарства (бета-блокаторы, блокаторы кальциевых каналов, дигоксин), лекарства от высокого кровяного давления, антиаритмические средства; миорелаксанты и седативные средства; антидепрессанты и нейролептики; диуретики; литий.Попросите вашего поставщика пересмотреть лекарства, которые вы принимаете.
Симптомы и причины
Что вызывает блокаду сердца?
Наиболее частой причиной сердечной блокады является сердечный приступ. Другие причины включают заболевание сердечной мышцы, обычно называемое кардиомиопатией, заболевания сердечного клапана и проблемы со структурой сердца. Блокада сердца также может быть вызвана повреждением сердца во время операции на открытом сердце, как побочный эффект некоторых лекарств или воздействия токсинов. Другой причиной может быть генетика.
Каковы симптомы блокады сердца?
Симптомы сердечной блокады различаются в зависимости от типа блока.
Блокада сердца первой степени:
- Симптомы могут отсутствовать.
- Может быть обнаружен во время обычной электрокардиограммы (ЭКГ), хотя частота сердечных сокращений и ритм обычно в норме.
Блокада первой степени часто встречается у спортсменов, подростков, молодых людей и людей с высокоактивным блуждающим нервом.
Симптомы блокады сердца второй степени:
- Обморок, головокружение.
- Боль в груди.
- Чувство усталости.
- Одышка.
- Учащенное сердцебиение.
- Учащенное дыхание.
- Тошнота.
Симптомы блокады сердца третьей степени:
- Головокружение, обмороки.
- Боль в груди.
- Чувство усталости.
- Одышка.
Симптомы блокады сердца третьей степени более выражены из-за низкой частоты сердечных сокращений. Если у вас серьезные симптомы, немедленно обратитесь за медицинской помощью.
Диагностика и тесты
Как диагностируется блокада сердца?
Ваш кардиолог сначала изучит вашу медицинскую историю и историю болезни семьи и задаст вопросы о вашем общем состоянии здоровья, вашем питании, уровне активности и ваших симптомах. Вас также спросят о лекарствах, которые вы принимаете (по рецепту или без рецепта), а также о том, курите ли вы или употребляете запрещенные наркотики.
Вас также спросят о лекарствах, которые вы принимаете (по рецепту или без рецепта), а также о том, курите ли вы или употребляете запрещенные наркотики.
Во время медицинского осмотра кардиолог послушает ваше сердце и проверит вашу частоту сердечных сокращений.Вас также проверит на наличие признаков сердечной недостаточности, таких как скопление жидкости в ступнях, лодыжках и ногах.
Ваш кардиолог может направить вас к электрофизиологу. Электрофизиологи — это врачи, специализирующиеся на электрической активности сердца. Вы можете пройти следующие тесты:
- ЭКГ: Электрокардиограмма (ЭКГ) регистрирует электрическую активность вашего сердца — его частоту сердечных сокращений и ритм, а также синхронизацию электрических сигналов, проходящих через ваше сердце.Этот тест может помочь определить тяжесть сердечной блокады (если она присутствует). Вам может потребоваться носить портативное устройство для амбулаторного мониторинга, такое как монитор Холтера или регистратор событий, в течение 24–48 часов или дольше, чтобы собрать больше информации об электрической активности вашего сердца.
 Если вам нужен монитор, вы получите подробную информацию о том, как им пользоваться.
Если вам нужен монитор, вы получите подробную информацию о том, как им пользоваться. - Имплантируемый петлевой регистратор: Это очень тонкое устройство, которое вводится под кожу груди и может контролировать сердечный ритм в течение пяти лет.Он имплантируется амбулаторно всего за несколько минут и полезен для пациентов, у которых случаются очень нечастые, но важные эпизоды без четкого объяснения их происхождения.
- Электрофизиологическое исследование: Электрофизиологическое исследование включает введение длинной тонкой трубки, называемой катетером, через кровеносный сосуд и направление ее к сердцу для измерения и записи электрической активности внутри вашего сердца. Если вам понадобится этот тест, вы получите более подробную информацию.
Какие осложнения блокады сердца?
Осложнения могут быть опасными для жизни и включают:
Ведение и лечение
Как лечится блокада сердца?
Ваш кардиолог определит, как блокада сердца (ее тип, расположение и тяжесть) влияет на способность сердца работать, и рассмотрит ваши симптомы, чтобы определить, как управлять своим состоянием. Симптомы и лечение варьируются от человека к человеку.
Симптомы и лечение варьируются от человека к человеку.
Иногда изменение лекарств или лечения сердечных заболеваний останавливает сердечную блокаду.
- Блокада первой степени: Если у вас блокада сердца первой степени, вам, вероятно, не понадобится лечение.
- Блокада второй степени: Если у вас есть блокада сердца второй степени и у вас есть симптомы, вам может потребоваться кардиостимулятор, чтобы ваше сердце билось должным образом. Кардиостимулятор — это небольшое устройство, которое посылает в ваше сердце электрические импульсы.
- Блокада третьей степени: Блокада сердца третьей степени часто впервые обнаруживается во время чрезвычайной ситуации. Лечение почти всегда включает кардиостимулятор.
Если вам нужен кардиостимулятор, ваш кардиолог / электрофизиолог расскажет вам о деталях, о типе, который лучше всего подходит для вас, и о том, чего ожидать до, во время и после того, как вы получите кардиостимулятор.
Профилактика
Можно ли предотвратить блокаду сердца?
Некоторые случаи блокады сердца могут быть врожденными (присутствуют при рождении).Но чаще всего блокада сердца развивается после рождения. Некоторые причины невозможно предотвратить. Мы также знаем, что риск сердечной блокады увеличивается с возрастом, как и сердечные заболевания. Некоторые причины сердечных заболеваний можно предотвратить.
Шаги, которые вы можете предпринять, чтобы сохранить свое сердце и тело как можно более здоровым, включают:
- Вести здоровый образ жизни , который включает в себя здоровую для сердца диету, регулярные физические упражнения, достаточное количество сна каждую ночь, снижение стресса, ограничение алкоголя и отказ от курения и употребления запрещенных наркотиков.
- Поговорите со своим врачом о пересмотре лекарств и других добавок , которые вы принимаете, чтобы определить, изменяются ли какие-либо нормальные уровни калия, кальция и магния — веществ в вашем организме, которые влияют на электрическую систему вашего сердца.
 При необходимости ваш поставщик медицинских услуг может изменить ваше лекарство на лекарство другого класса.
При необходимости ваш поставщик медицинских услуг может изменить ваше лекарство на лекарство другого класса.
Перспективы / Прогноз
Как блокада сердца влияет на мою жизнь?
Если у вас блокада сердца первой степени, спросите своего кардиолога или электрофизиолога, какие изменения, если таковые имеются, вам необходимо внести в свой образ жизни или лекарства.Этот тип сердечной блокады обычно не мешает вашей нормальной деятельности.
Если у вас есть кардиостимулятор для блокады сердца второй или третьей степени, ваш кардиолог может порекомендовать некоторые ограничения в отношении типов упражнений, в которых вы можете участвовать (например, контактные виды спорта). Однако в целом кардиостимулятор не будет серьезно ограничивать вашу способность заниматься спортом и проводить досуг.
Ваш кардиолог захочет периодически проверять ваш кардиостимулятор, чтобы убедиться, что он по-прежнему соответствует вашим потребностям.Мониторинг осуществляется как дистанционно, так и лично. Для удаленного мониторинга используется беспроводная сотовая связь, часто также с использованием синего зуба или Wi-Fi. Это позволяет врачу практически непрерывно наблюдать за вами. Вам также необходимо будет лично осмотреть ваш кардиостимулятор для полной оценки и настройки, как правило, один раз в год. Важно следовать инструкциям врача по мониторингу кардиостимулятора, чтобы он мог убедиться, что ваш кардиостимулятор правильно регулирует ваше сердцебиение.
Для удаленного мониторинга используется беспроводная сотовая связь, часто также с использованием синего зуба или Wi-Fi. Это позволяет врачу практически непрерывно наблюдать за вами. Вам также необходимо будет лично осмотреть ваш кардиостимулятор для полной оценки и настройки, как правило, один раз в год. Важно следовать инструкциям врача по мониторингу кардиостимулятора, чтобы он мог убедиться, что ваш кардиостимулятор правильно регулирует ваше сердцебиение.
Жить с
Есть ли особые инструкции или информация, которыми я должен поделиться с другими, если у меня есть кардиостимулятор?
Если у вас есть кардиостимулятор:
- Избегайте близкого контакта с магнитными устройствами и любыми устройствами, излучающими электрическое поле.Это включает в себя пребывание на расстоянии не менее шести дюймов от сотовых телефонов.
- Проходя через пункты досмотра в аэропортах, зданиях судов или в любом другом месте, где требуется проверка безопасности, используйте средство проверки обратного рассеяния (когда вы поднимаете руки) или получите ручную проверку.
 Не позволяйте техникам пользоваться ручными жезлами. Если вам необходимо пройти через станции сканирования, это, скорее всего, укажет на наличие металла, но не повредит кардиостимулятору. Сообщите специалистам службы безопасности, что у вас есть кардиостимулятор.Всегда имейте при себе карточку с указанием типа вашего кардиостимулятора.
Не позволяйте техникам пользоваться ручными жезлами. Если вам необходимо пройти через станции сканирования, это, скорее всего, укажет на наличие металла, но не повредит кардиостимулятору. Сообщите специалистам службы безопасности, что у вас есть кардиостимулятор.Всегда имейте при себе карточку с указанием типа вашего кардиостимулятора. - Сообщите всем своим врачам, стоматологу и другим поставщикам медицинских услуг, что у вас есть кардиостимулятор. Некоторые медицинские процедуры, такие как магнитно-резонансная томография (МРТ), могут мешать работе кардиостимуляторов. Однако часто можно провести МРТ.
Когда мне следует позвонить своему лечащему врачу?
Позвоните своему врачу, если почувствуете:
- Головокружение или обморок.
- Боль в груди.
- Учащенное сердцебиение или пропущенное сердцебиение.
- Слабость.
- Одышка.
- Опухшие ступни, лодыжки или ноги.
Тяжелая аритмия, вызванная мутациями сердечных кальциевых каналов L-типа
Аннотация
Синдром Тимоти (TS) — мультисистемное заболевание, вызывающее обморок и внезапную смерть от сердечной аритмии. К характерным особенностям относятся врожденные пороки сердца, иммунодефицит, перемежающаяся гипогликемия, когнитивные нарушения и аутизм.Все индивидуумы TS имеют синдактилию (перепончатость пальцев рук и ног). Мы обнаружили, что TS является результатом повторяющейся мутации de novo сердечного кальциевого канала L-типа (Ca V 1.2), G406R. G406 расположен в альтернативно сплайсированном экзоне 8A, кодирующем трансмембранный сегмент S6 домена I. Здесь мы описываем двух индивидуумов с тяжелым вариантом TS (TS2). Ни у одного ребенка синдактилии не было. У обоих пациентов наблюдалось резкое удлинение интервала QT на электрокардиограмме, при этом интервал QT с поправкой на частоту сердечных сокращений составлял от 620 до 730 мс, что приводило к множественным аритмиям и внезапной смерти.У одного человека была тяжелая умственная отсталость и скелетная миопатия немалинового стержня. Мы идентифицировали de novo миссенс-мутаций в экзоне 8 Ca V 1.2 у обоих пациентов.
К характерным особенностям относятся врожденные пороки сердца, иммунодефицит, перемежающаяся гипогликемия, когнитивные нарушения и аутизм.Все индивидуумы TS имеют синдактилию (перепончатость пальцев рук и ног). Мы обнаружили, что TS является результатом повторяющейся мутации de novo сердечного кальциевого канала L-типа (Ca V 1.2), G406R. G406 расположен в альтернативно сплайсированном экзоне 8A, кодирующем трансмембранный сегмент S6 домена I. Здесь мы описываем двух индивидуумов с тяжелым вариантом TS (TS2). Ни у одного ребенка синдактилии не было. У обоих пациентов наблюдалось резкое удлинение интервала QT на электрокардиограмме, при этом интервал QT с поправкой на частоту сердечных сокращений составлял от 620 до 730 мс, что приводило к множественным аритмиям и внезапной смерти.У одного человека была тяжелая умственная отсталость и скелетная миопатия немалинового стержня. Мы идентифицировали de novo миссенс-мутаций в экзоне 8 Ca V 1.2 у обоих пациентов. Одна из них была мутацией, аналогичной мутации, обнаруженной в экзоне 8A классического TS, G406R. Другая мутация — G402S. Экзон 8 кодирует ту же область, что и экзон 8A, и оба являются взаимоисключающими. Сплайсированная форма Ca V 1.2, содержащая экзон 8, сильно экспрессируется в сердце и головном мозге, составляя ≈80% от Ca V 1.2 мРНК. G406R и G402S вызывают пониженную инактивацию каналов, что приводит к поддержанию деполяризующих кальциевых токов L-типа. Компьютерное моделирование показало удлинение потенциалов действия кардиомиоцитов и отсроченную постдеполяризацию — факторы, повышающие риск аритмии. Эти данные показывают, что мутации с усилением функции экзонов 8 и 8A Ca V 1.2 вызывают различные формы TS.
Одна из них была мутацией, аналогичной мутации, обнаруженной в экзоне 8A классического TS, G406R. Другая мутация — G402S. Экзон 8 кодирует ту же область, что и экзон 8A, и оба являются взаимоисключающими. Сплайсированная форма Ca V 1.2, содержащая экзон 8, сильно экспрессируется в сердце и головном мозге, составляя ≈80% от Ca V 1.2 мРНК. G406R и G402S вызывают пониженную инактивацию каналов, что приводит к поддержанию деполяризующих кальциевых токов L-типа. Компьютерное моделирование показало удлинение потенциалов действия кардиомиоцитов и отсроченную постдеполяризацию — факторы, повышающие риск аритмии. Эти данные показывают, что мутации с усилением функции экзонов 8 и 8A Ca V 1.2 вызывают различные формы TS.
Синдром Тимоти (TS) — мультисистемное заболевание, характеризующееся простой синдактилией и опасными для жизни сердечными аритмиями.Первые случаи TS были описаны в 1992 и 1995 годах как спорадические случаи синдрома удлиненного интервала QT, врожденного порока сердца и синдактилии (1–3). Со временем и терапией, продлевающей жизнь, стало ясно, что TS проявляет основные фенотипические аномалии во многих системах органов (4). Все пациенты с TS имели удлинение интервала QT на электрокардиограмме, синдактилию, аномальные зубы и родились лысыми. У большинства из них были аритмии, в том числе брадикардия, атриовентрикулярная блокада, желудочковая тахикардия (торсады) и фибрилляция желудочков.Десять из 17 детей TS умерли со средним возрастом смерти 2,5 года. Дополнительные общие признаки включали врожденный порок сердца, дисморфические черты лица, миопию, иммунодефицит, рецидивирующие инфекции, перемежающуюся гипогликемию и гипотермию. Наконец, у многих детей с TS были задержки в развитии, включая языковые, моторные и общие когнитивные нарушения. Некоторые не издавали звуков речи в младенчестве. Были выявлены серьезные проблемы с артикуляцией, приемом и выражением лица.Пятеро детей были обследованы на аутизм, и трое соответствовали критериям этого расстройства. Один ребенок TS соответствовал критериям расстройств аутистического спектра, и у одного была серьезная задержка языкового развития.
Со временем и терапией, продлевающей жизнь, стало ясно, что TS проявляет основные фенотипические аномалии во многих системах органов (4). Все пациенты с TS имели удлинение интервала QT на электрокардиограмме, синдактилию, аномальные зубы и родились лысыми. У большинства из них были аритмии, в том числе брадикардия, атриовентрикулярная блокада, желудочковая тахикардия (торсады) и фибрилляция желудочков.Десять из 17 детей TS умерли со средним возрастом смерти 2,5 года. Дополнительные общие признаки включали врожденный порок сердца, дисморфические черты лица, миопию, иммунодефицит, рецидивирующие инфекции, перемежающуюся гипогликемию и гипотермию. Наконец, у многих детей с TS были задержки в развитии, включая языковые, моторные и общие когнитивные нарушения. Некоторые не издавали звуков речи в младенчестве. Были выявлены серьезные проблемы с артикуляцией, приемом и выражением лица.Пятеро детей были обследованы на аутизм, и трое соответствовали критериям этого расстройства. Один ребенок TS соответствовал критериям расстройств аутистического спектра, и у одного была серьезная задержка языкового развития. Таким образом, TS представляет собой сложное физиологическое расстройство и нарушение развития, затрагивающее несколько систем органов, включая сердце, пальцы и мозг.
Таким образом, TS представляет собой сложное физиологическое расстройство и нарушение развития, затрагивающее несколько систем органов, включая сердце, пальцы и мозг.
TS представлен как единичный признак во всех семьях, кроме одной. В этой семье пострадали двое из трех братьев и сестер. Ни один из родителей ни в одной семье не пострадал.Мы обнаружили, что TS является результатом идентичной, de novo , миссенс-мутации с усилением функции в экзоне 8A сердечного кальциевого канала L-типа (Ca V 1.2) (4, 5). Ca V 1.2 важен для связи возбуждения и сокращения в сердце. Мы обнаружили, что он также экспрессируется в других тканях, включая мозг, гладкие мышцы, иммунную систему, зубы и яички. Функциональная экспрессия мутантных и WT каналов в гетерологичных системах продемонстрировала, что причинная мутация, G406R, приводит почти к полному отсутствию инактивации потенциал-зависимых каналов.Возникающие в результате входящие внутрь токи Ca 2+ , вероятно, вызывают внутриклеточную перегрузку Ca 2+ во множестве типов клеток. Таким образом, аномальная передача сигналов Ca 2+ является причиной TS.
Таким образом, аномальная передача сигналов Ca 2+ является причиной TS.
Необычной особенностью TS была его молекулярная однородность; все случаи возникли в результате идентичной, de novo , миссенс-мутации G406R в экзоне 8A. Кроме того, во всех случаях TS проявлялась простая синдактилия. Здесь мы описываем два случая нетипичного TS (TS2). У обоих наблюдалось сильное удлинение интервала QT с интервалом QT с поправкой на частоту сердечных сокращений (QTc) в диапазоне от 620 до 730 мс, и было несколько эпизодов аритмий.Один недавно умер от торсадов и фибрилляции желудочков. У этого человека было много других значительных фенотипических аномалий, включая тяжелую умственную отсталость и заболевание скелетных мышц, известное как немалиновая миопатия (НМ) (5). Ни в одном из этих случаев синдактилии не было. Как и в случае TS, мы обнаружили, что фенотип у этих людей возник в результате de novo миссенс-мутаций Ca V 1.2. Однако эти мутации затрагивают экзон 8, а не экзон 8A. Одна мутация была аналогична мутации, идентифицированной в классическом TS, G406R, тогда как другая была G402S.Как и в случае с TS, мы обнаружили, что обе мутации вызывали почти полный отказ от инактивации зависимых от напряжения каналов, что приводило к поддержанию внутренних токов Ca 2+ .
Одна мутация была аналогична мутации, идентифицированной в классическом TS, G406R, тогда как другая была G402S.Как и в случае с TS, мы обнаружили, что обе мутации вызывали почти полный отказ от инактивации зависимых от напряжения каналов, что приводило к поддержанию внутренних токов Ca 2+ .
Материалы и методы
Выявление предмета и фенотипический анализ. Фенотипический анализ включал анамнез, физический осмотр, электрокардиографию и эхокардиографию. Информированное согласие или согласие было получено от отдельных лиц или их опекунов в соответствии со стандартами, установленными местными наблюдательными советами учреждений.В таблице 1 приведены подробности отдельных случаев.
Таблица 1. Фенотипические особенности TS2 Генотипический анализ и анализ последовательностей. Геномную ДНК из лимфоцитов периферической крови или клеточных линий, полученных из лимфоцитов, трансформированных вирусом Эпштейна-Барра, получали с использованием набора для выделения ДНК Puregene (Gentra Systems, Миннеаполис).Геномную ДНК из буккальных мазков получали с использованием набора QIAamp DNA Mini Kit (Qiagen, Valencia, CA). ПЦР-амплификацию образцов ДНК экзонов Ca V 1.2 и мутационные анализы проводили, как описано (4, 6). Экзоны 8 (первый) и 8A (второй) были обозначены в соответствии с их порядком в геномной ДНК. Олигонуклеотиды и условия ПЦР для амплификации экзонов небулина 145–148, 151–171, 173 и 175–182 были получены от K. Pelin (Университет Хельсинки, Хельсинки). 5′-UTR и вся кодирующая последовательность α-актина скелетных мышц были амплифицированы с помощью четырех пар олигонуклеотидов: 1F-GGTGGCGCGGAGGGAATG и 1R-TTCTGCCCCGGAGTCCTTC (ампликон 223 п.н.), 2F-TGAGTCTGCGGCTGATGP-2F-TGAGTCTGCGCGGTGP -CCCCCAGCCACTCACTCTC и 3R-GCGGGGAGCGTGAGCAGA (552), а также 4F-AGCTTCTGCTCACGCTCCC и 4R-GTCCTGAGAAGTCGCGTGCT (473 п.
Геномную ДНК из лимфоцитов периферической крови или клеточных линий, полученных из лимфоцитов, трансформированных вирусом Эпштейна-Барра, получали с использованием набора для выделения ДНК Puregene (Gentra Systems, Миннеаполис).Геномную ДНК из буккальных мазков получали с использованием набора QIAamp DNA Mini Kit (Qiagen, Valencia, CA). ПЦР-амплификацию образцов ДНК экзонов Ca V 1.2 и мутационные анализы проводили, как описано (4, 6). Экзоны 8 (первый) и 8A (второй) были обозначены в соответствии с их порядком в геномной ДНК. Олигонуклеотиды и условия ПЦР для амплификации экзонов небулина 145–148, 151–171, 173 и 175–182 были получены от K. Pelin (Университет Хельсинки, Хельсинки). 5′-UTR и вся кодирующая последовательность α-актина скелетных мышц были амплифицированы с помощью четырех пар олигонуклеотидов: 1F-GGTGGCGCGGAGGGAATG и 1R-TTCTGCCCCGGAGTCCTTC (ампликон 223 п.н.), 2F-TGAGTCTGCGGCTGATGP-2F-TGAGTCTGCGCGGTGP -CCCCCAGCCACTCACTCTC и 3R-GCGGGGAGCGTGAGCAGA (552), а также 4F-AGCTTCTGCTCACGCTCCC и 4R-GTCCTGAGAAGTCGCGTGCT (473 п. н.).Олигонуклеотиды α-актина были сконструированы для геномных последовательностей, найденных в базе данных Celera, с использованием oligo6.6 (Molecular Biology Insights, Cascade, CO). Фрагменты ПЦР очищали с использованием набора для очистки ПЦР QIAquick (Qiagen), а секвенирование выполняли с помощью автоматического секвенатора ДНК Applied Biosystems 3700.
н.).Олигонуклеотиды α-актина были сконструированы для геномных последовательностей, найденных в базе данных Celera, с использованием oligo6.6 (Molecular Biology Insights, Cascade, CO). Фрагменты ПЦР очищали с использованием набора для очистки ПЦР QIAquick (Qiagen), а секвенирование выполняли с помощью автоматического секвенатора ДНК Applied Biosystems 3700.
Экспрессия мРНК и анализ кДНК. Анализ Нозерн-блоттинг выполняли с использованием 12-полосных Нозерн-блоттингов I и III для множественных тканей человека (BD Biosciences Clontech).Дот-блот-анализ мРНК проводили с использованием Multiple Tissue Expression Human Array 3 (BD Biosciences Clontech). Фрагмент ПЦР длиной 117 п.н., амплифицированный из кДНК Ca V 1.2 с олигонуклеотидами прямого GATGCAGGACGCTATGGGC и обратного TGGAAAACTCTCCGCTCAACA, использовали в качестве зонда для мРНК, содержащих экзон 8. Фрагмент метили с помощью набора для мечения Prime-It II (Stratagene) с использованием обратного олигонуклеотида вместо предоставленных случайных 9-меров. Условия гибридизации и промывки соответствовали рекомендациям производителя.Кляксы экспонировали на пленке в течение 3 дней.
Условия гибридизации и промывки соответствовали рекомендациям производителя.Кляксы экспонировали на пленке в течение 3 дней.
Конструкции ДНК для функциональной экспрессии. Полноразмерная кДНК Ca V 1,2 человека WT (номер доступа в GenBank AJ224873), клонированная в векторной системе экспрессии Xenopus (pBluescript), была щедрым подарком от Н. Солдатова (Национальный институт старения, Бетезда). Мутации G402S и G406R были введены путем сайт-направленного мутагенеза с использованием Quikchange (Stratagene).
Ca V β 2b и Ca V α 2 δ 1 — вспомогательные субъединицы, связанные с Ca V 1.2 в сердце человека (7, 8). Клоны Ca V β 2b и Ca V α 2 δ 1 , использованные для экспрессии в ооцитах Xenopus , были любезным подарком от Н. Даскаля (Тель-Авивский университет, Рамат-Авив, Израиль) .
Полноразмерные клоны для всех четырех экспрессионных конструкций, описанных выше, секвенировали в прямом и обратном направлении и сравнивали с геномной ДНК, чтобы убедиться в отсутствии или введении непреднамеренных мутаций.
Инъекции и растворы для ооцитов. Выделение и инъекция ооцитов Xenopus laevis , а также синтез кэпированной поли (A) комплементарной РНК (кРНК) из линеаризованных матриц кДНК выполняли, как описано (9). Ооциты совместно инъецировали кРНК, кодирующей WT или мутантную субъединицу Ca V человека (11 нг) плюс Ca V β 2b (2,7 нг) и Ca V α 2 δ 1 (2 .7 нг) субъединиц. Внеклеточный раствор содержал 40 мМ Ba (OH) 2 , 50 мМ NaOH, 1 мМ КОН и 5 мМ Hepes (pH 7,4 с метансульфоновой кислотой, 22-25 ° C). К раствору добавляли нифлуминовую кислоту (300 мкМ) для блокирования эндогенных токов Cl — , активированных Ca 2+ (10).
Зажим напряжения и анализ данных. Ba 2+ токов через Ca V 1,2 каналов регистрировали из ооцитов с помощью стандартных двухмикроэлектродных методов фиксации напряжения через 2–10 дней после инъекции кРНК (11, 12).Микропипетки содержали 3 M KCl и имели сопротивление 0,5–1 МОм. Взаимосвязь между током и напряжением ( I — В ) определялась путем измерения пикового внутреннего тока, вызванного 2-секундными испытательными импульсами, приложенными с шагом 10 мВ до потенциалов в диапазоне от -70 до +40 мВ. Удерживающий потенциал составлял -80 мВ. Токи фильтровались на 2 кГц и оцифровывались на 10 кГц. Относительная зависимость активации от напряжения рассчитывалась по нормированным пиковым входящим токам ( I пик ) и экстраполированный реверсивный потенциал ( E rev ) для каждого ооцита.Зависимость тока инактивации Ba 2+ от напряжения определялась по двухимпульсному протоколу. Относительная величина входящего тока, возникающего во время второго импульса (до +10 мВ), была построена как функция переменного напряжения кондиционирующего 2-секундного предымпульса. Данные были подогнаны к функции Больцмана, чтобы получить полупункт ( V 1/2 ) и коэффициент наклона ( k ) для соотношений, описывающих зависимость напряжения Ca V 1.2 активация и деактивация. Сбор данных и анализ выполняли с использованием программного обеспечения pclamp8 (Axon Instruments, Юнион-Сити, Калифорния). Данные представлены в виде среднего значения ± стандартная ошибка ( n = количество ооцитов).
Относительная величина входящего тока, возникающего во время второго импульса (до +10 мВ), была построена как функция переменного напряжения кондиционирующего 2-секундного предымпульса. Данные были подогнаны к функции Больцмана, чтобы получить полупункт ( V 1/2 ) и коэффициент наклона ( k ) для соотношений, описывающих зависимость напряжения Ca V 1.2 активация и деактивация. Сбор данных и анализ выполняли с использованием программного обеспечения pclamp8 (Axon Instruments, Юнион-Сити, Калифорния). Данные представлены в виде среднего значения ± стандартная ошибка ( n = количество ооцитов).
Моделирование сердечных миоцитов. Модель миоцита левого желудочка человека (13) была использована для моделирования эффектов мутаций экзона 8 и экзона 8A G406R. Свойства каналов WT и мутантных кальциевых каналов L-типа моделировали путем регулирования функции относительной потенциал-зависимой инактивации y ∞ . Описания каналов были объединены в модели миоцитов для реконструкции гетерозиготного состояния, в котором экзон 8, содержащий белок Ca V 1.2, составляет 77% (38,5% WT, 38,5% G406R) от общего белка Ca V 1.2. Кроме того, была создана модель для гетерозиготного состояния, в котором экзон 8A, содержащий белок Ca V 1.2, составляет 23% (11,5% WT и 11,5% G406R) от общего белка Ca V 1.2 (4). Модель спонтанного высвобождения кальция из соединительного саркоплазматического ретикулума через кальциевые каналы рианодинового рецептора была включена в модель миоцитов (14).Порог спонтанного высвобождения внутриклеточного Ca 2+ соответствует 70% кальсеквестрин-связанного Ca 2+ .
Описания каналов были объединены в модели миоцитов для реконструкции гетерозиготного состояния, в котором экзон 8, содержащий белок Ca V 1.2, составляет 77% (38,5% WT, 38,5% G406R) от общего белка Ca V 1.2. Кроме того, была создана модель для гетерозиготного состояния, в котором экзон 8A, содержащий белок Ca V 1.2, составляет 23% (11,5% WT и 11,5% G406R) от общего белка Ca V 1.2 (4). Модель спонтанного высвобождения кальция из соединительного саркоплазматического ретикулума через кальциевые каналы рианодинового рецептора была включена в модель миоцитов (14).Порог спонтанного высвобождения внутриклеточного Ca 2+ соответствует 70% кальсеквестрин-связанного Ca 2+ .
Моделирование каналов и моделей миоцитов проводилось с использованием метода Эйлера для численного интегрирования обыкновенных дифференциальных уравнений (15). Для моделирования с помощью модели миоцитов временная дискретизация для решения уравнений была адаптирована для различных компонентов (например, описания Na-канала) модели.
Результаты
TS2. Человек европеоидной расы (индивидуум 1) обратился за медицинской помощью на 25 неделе беременности из-за брадикардии (частота сердечных сокращений 60 ударов в минуту) и атриовентрикулярной проводимости 2: 1 (рис. 1). Дополнительные результаты включали гипертрофию двух желудочков и умеренную дисфункцию желудочков. Девочка родилась путем кесарева сечения из-за тяжелой брадикардии на 38 неделе беременности. При рождении ребенок чередовал нормальную проводимость и атриовентрикулярную блокаду 2: 1 и имел заметное удлинение интервала QT (QTc 730 мс).Для улучшения сердечной проводимости был установлен имплантируемый кардиостимулятор. Однако желудочковая стимуляция была небезопасной, поскольку она постоянно приводила к развитию торсад. Вместо этого стимуляция предсердия проводилась со скоростью 140 ударов в минуту с допустимой желудочковой реакцией 70 ударов в минуту. Младенец выписан из больницы под круглосуточным уходом и наблюдением.
Дисморфические черты лица, выраженное удлинение интервала QT, аритмия и дефекты скелетных мышц у пораженных лиц. ( A — C ) Пациент 1 демонстрирует дисморфические черты лица, включая плоскую переносицу, тонкую верхнюю губу и выступающий язык. ( D ) Электрокардиограмма показывает резкое удлинение интервала QT, вызывающее предсердно-желудочковую блокаду 2: 1, проявляющуюся в виде двух предсердных сокращений (зубцов P) для каждого желудочкового сокращения (комплекс QRS). ( E ) Электрокардиограмма показывает полиморфную желудочковую тахикардию для индивидуума 1.( F ) Замороженный срез биопсии левой четырехглавой мышцы, окрашенный модифицированным трихромом Гомори, демонстрирующий редкие немалиновые стержни (указаны стрелками) в разбросанных миофибриллах (масштабная линейка, 20 мкм). ( G ) Электронная микрофотография субсарколеммальных собраний электронно-плотных стержней (× 17,800). ( H ) Электронная микрофотография, иллюстрирующая нормальную саркомерную архитектуру для сравнения с G (× 17,800).
( G ) Электронная микрофотография субсарколеммальных собраний электронно-плотных стержней (× 17,800). ( H ) Электронная микрофотография, иллюстрирующая нормальную саркомерную архитектуру для сравнения с G (× 17,800).
В 4-месячном возрасте у ребенка во время кормления случился эпизод цианоза и апноэ.Младенца доставили в больницу на машине скорой помощи. Ей шесть раз делали электрокардиоверсию по дороге и во время госпитализации. Один эпизод потребовал реанимации. Лекарства включали пропранолол, эналаприл и мексилитин. Были отмечены признаки бивентрикулярной гипертофии. Аресты не дали ответа на i.v. магний, в / в лидокаин, или кардиоверсия. Увеличение концентрации калия в сыворотке не повлияло на интервал QT. Две недели спустя были выполнены шейная симпатическая ганглионэктомия и установка желудочкового кардиостимулятора в попытке уменьшить аритмию.Ни одно из вмешательств не было эффективным.
Этот человек также страдал от двустороннего врожденного вывиха бедер и чрезмерной растяжимости суставов. Биопсия скелетных мышц через 5 месяцев показала умеренные колебания в размере волокон с минимальной атрофией волокон 1 типа и иногда более мелкими волокнами с скоплениями немалиновых палочек (рис. 1 F ).
). Патологический диагноз НМ подтвержден идентификацией немалиновых палочек с помощью электронной микроскопии (рис. 1 G и H ).
), который также выявил умеренное очаговое повышение содержания гликогена.Митохондрии морфологически нормальные. К 6 годам стало очевидно, что пациентка страдает несоответствием в развитии тела. Хотя верхняя часть ее тела выглядела нормальной для ее возраста, нижняя часть имела вид, типичный для двух- или трехлетнего ребенка. Известные черты лица включали выступающий лоб, вдавленную переносицу и выступающий язык. Зубная эмаль была плохо развита, и из-за тяжелого кариеса большинство зубов было удалено. Во время анестезии были задокументированы значительные альтернации и торсады зубца T.
Биопсия скелетных мышц через 5 месяцев показала умеренные колебания в размере волокон с минимальной атрофией волокон 1 типа и иногда более мелкими волокнами с скоплениями немалиновых палочек (рис. 1 F ).
). Патологический диагноз НМ подтвержден идентификацией немалиновых палочек с помощью электронной микроскопии (рис. 1 G и H ).
), который также выявил умеренное очаговое повышение содержания гликогена.Митохондрии морфологически нормальные. К 6 годам стало очевидно, что пациентка страдает несоответствием в развитии тела. Хотя верхняя часть ее тела выглядела нормальной для ее возраста, нижняя часть имела вид, типичный для двух- или трехлетнего ребенка. Известные черты лица включали выступающий лоб, вдавленную переносицу и выступающий язык. Зубная эмаль была плохо развита, и из-за тяжелого кариеса большинство зубов было удалено. Во время анестезии были задокументированы значительные альтернации и торсады зубца T.
У ребенка участились судороги. Другие неврологические наблюдения включали частые рефлексы испуга, статическую энцефалопатию и нерегулярный режим сна. При осмотре регресса в развитии замечено не было. В 6 лет ребенок не мог держать голову без поддержки, но мог перевернуться. Она не могла держать чашку или посуду. Ребенок иногда улыбался и издавал какие-то звуки, но слов было не узнать. В 6 лет она умерла от фибрилляции желудочков.Ни у одного члена семьи не было фенотипических признаков, идентифицированных у особи 1.
Другие неврологические наблюдения включали частые рефлексы испуга, статическую энцефалопатию и нерегулярный режим сна. При осмотре регресса в развитии замечено не было. В 6 лет ребенок не мог держать голову без поддержки, но мог перевернуться. Она не могла держать чашку или посуду. Ребенок иногда улыбался и издавал какие-то звуки, но слов было не узнать. В 6 лет она умерла от фибрилляции желудочков.Ни у одного члена семьи не было фенотипических признаков, идентифицированных у особи 1.
Белый мальчик (особь 2) родился путем кесарева сечения на 38 неделе беременности. При рождении или в младенчестве не было отмечено проблем с сердцем или здоровьем. Ребенок рос нормально, достигнув всех этапов развития в нормальные сроки. Однако у него случилась остановка сердца в возрасте 4 лет при восхождении на батуте. Воспитатель ребенка провела искусственное дыхание, и его доставили в больницу, где поставили диагноз: синдром удлиненного интервала QT.В течение следующих 6 лет у ребенка было по крайней мере три дополнительных эпизода остановки сердца, все из которых были вызваны слуховыми раздражителями. Был имплантирован кардиостимулятор. В 11 лет он перенес остановку сердца после терапии бактримом (сульфаметоксазолом и триметопримом) по поводу инфекции носа. Затем он находился в коме 2 недели. Хотя реабилитация помогла ребенку восстановить физические, умственные и социальные способности, серьезные повреждения мозга остались. В то время был установлен автоматический кардиодефибриллятор, который впоследствии сработал более 20 раз.В настоящее время он страдает аритмией сердца один раз в неделю, всегда по ночам и ассоциируется с ночными ужасами. Воспитатели также отметили признаки депрессии и обсессивно-компульсивного поведения.
Был имплантирован кардиостимулятор. В 11 лет он перенес остановку сердца после терапии бактримом (сульфаметоксазолом и триметопримом) по поводу инфекции носа. Затем он находился в коме 2 недели. Хотя реабилитация помогла ребенку восстановить физические, умственные и социальные способности, серьезные повреждения мозга остались. В то время был установлен автоматический кардиодефибриллятор, который впоследствии сработал более 20 раз.В настоящее время он страдает аритмией сердца один раз в неделю, всегда по ночам и ассоциируется с ночными ужасами. Воспитатели также отметили признаки депрессии и обсессивно-компульсивного поведения.
De Novo Миссенс-мутации в Ca V 1.2 Причина TS2. В предыдущем исследовании мы показали, что повторяющаяся миссенс-мутация de novo в Ca V 1.2 вызвала TS (4). Мы предположили, что мутации в этом гене могут быть связаны с другими формами этого заболевания.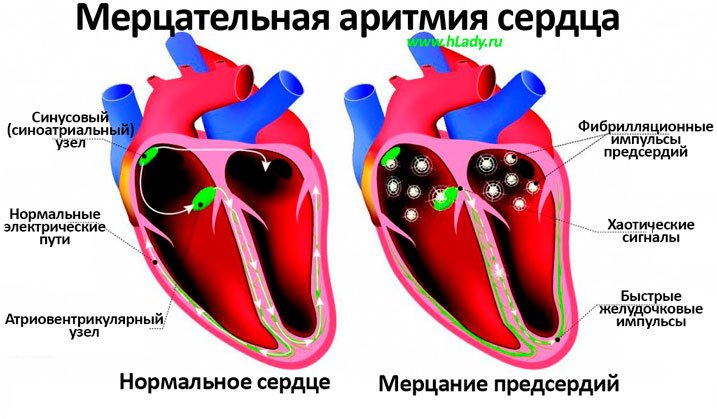 Мы проверили все 50 экзонов Ca V 1.2 у 324 человек с аритмией. Были идентифицированы две мутации, связанные с заболеванием. Анализ экзона 8 выявил переход G1216A в образцах ДНК от индивидуума 1 (рис. 2 A ). Этот переход привел к замене глицина на аргинин по остатку 406 (G406R). Переход G1204A в том же экзоне был идентифицирован у индивида 2, вызывая замену глицина на серин в положении 402 (G402S, рис. 2 B ).Обе аминокислоты (G406 и G402) полностью консервативны в других потенциалзависимых кальциевых каналах многих видов, от червей до человека (рис. 2 C ).
) и расположены на С-конце шестого трансмембранного сегмента домена I (DI / S6, рис. 2 D ). Ни одна из мутаций не была идентифицирована в 182 этнически сопоставимых контрольных образцах (364 хромосомы). Мутационный анализ дополнительных членов семьи, включая родителей, не выявил мутаций в Ca V 1.2.
Мы проверили все 50 экзонов Ca V 1.2 у 324 человек с аритмией. Были идентифицированы две мутации, связанные с заболеванием. Анализ экзона 8 выявил переход G1216A в образцах ДНК от индивидуума 1 (рис. 2 A ). Этот переход привел к замене глицина на аргинин по остатку 406 (G406R). Переход G1204A в том же экзоне был идентифицирован у индивида 2, вызывая замену глицина на серин в положении 402 (G402S, рис. 2 B ).Обе аминокислоты (G406 и G402) полностью консервативны в других потенциалзависимых кальциевых каналах многих видов, от червей до человека (рис. 2 C ).
) и расположены на С-конце шестого трансмембранного сегмента домена I (DI / S6, рис. 2 D ). Ни одна из мутаций не была идентифицирована в 182 этнически сопоставимых контрольных образцах (364 хромосомы). Мутационный анализ дополнительных членов семьи, включая родителей, не выявил мутаций в Ca V 1.2. Относительно более мягкий фенотип индивида 2 заставил нас предположить, что он мог быть мозаикой. Чтобы проверить гипотезу, мы получили ДНК из слизистой оболочки полости рта. Наблюдали мутантный пик миссенс-мутации. Однако этот мутантный пик был намного меньше по сравнению с мутантным пиком, обнаруженным в ДНК крови (рис. 2 B ). Это открытие указывает на то, что мутация возникла во время развития и присутствует только в подмножестве клеток. Таким образом, фенотип у этих двух пробандов возник в результате de novo мутаций в Ca V 1.2.
Относительно более мягкий фенотип индивида 2 заставил нас предположить, что он мог быть мозаикой. Чтобы проверить гипотезу, мы получили ДНК из слизистой оболочки полости рта. Наблюдали мутантный пик миссенс-мутации. Однако этот мутантный пик был намного меньше по сравнению с мутантным пиком, обнаруженным в ДНК крови (рис. 2 B ). Это открытие указывает на то, что мутация возникла во время развития и присутствует только в подмножестве клеток. Таким образом, фенотип у этих двух пробандов возник в результате de novo мутаций в Ca V 1.2.
De novo Ca v 1.2 мутации вызывают TS2. ( A ) Родословная показывает спорадическое возникновение фенотипа заболевания и миссенс-мутацию de novo G1216A у индивидуума 1. Эта мутация приводит к замене глицина 406 на аргинин (G406R) в экзоне 8.Кружки и квадраты обозначают женщин и мужчин соответственно. Закрашенные и пустые символы обозначают пострадавших и здоровых людей соответственно. Человек с косой чертой умер. Если не указано иное, трассировки последовательностей были получены из образцов ДНК крови. ( B ) Родословная показывает спорадическое возникновение фенотипа заболевания и миссенс-мутацию de novo G1204A у индивидуума 2. Эта мутация приводит к замене глицина 402 серином (G402S) в экзоне 8. Мутантный пик (зеленый, стрелка) ) присутствует в последовательности из ДНК крови, но только небольшой пик обнаруживается в ДНК слизистой оболочки полости рта, что указывает на мозаицизм.Мозаицизм может объяснить более мягкий фенотип у этого человека. ( C ) Выравнивание аминокислотной последовательности, показывающее консервативность глицина в положениях 402 и 406 от множества видов. Скобка указывает на конец шестого трансмембранного сегмента домена I (DI / S6).
Эта мутация приводит к замене глицина 406 на аргинин (G406R) в экзоне 8.Кружки и квадраты обозначают женщин и мужчин соответственно. Закрашенные и пустые символы обозначают пострадавших и здоровых людей соответственно. Человек с косой чертой умер. Если не указано иное, трассировки последовательностей были получены из образцов ДНК крови. ( B ) Родословная показывает спорадическое возникновение фенотипа заболевания и миссенс-мутацию de novo G1204A у индивидуума 2. Эта мутация приводит к замене глицина 402 серином (G402S) в экзоне 8. Мутантный пик (зеленый, стрелка) ) присутствует в последовательности из ДНК крови, но только небольшой пик обнаруживается в ДНК слизистой оболочки полости рта, что указывает на мозаицизм.Мозаицизм может объяснить более мягкий фенотип у этого человека. ( C ) Выравнивание аминокислотной последовательности, показывающее консервативность глицина в положениях 402 и 406 от множества видов. Скобка указывает на конец шестого трансмембранного сегмента домена I (DI / S6). ( D ) ( Верхний ) Прогнозируемая топология Ca V 1.2, показывающая расположение мутаций. ( Lower ) Гомология аминокислотной последовательности экзонов 8 и 8A. DI / S6 подчеркнут. G402 и G406, аминокислоты, мутировавшие в TS2, оба находятся в экзоне 8 и показаны красным.G406, мутировавший в TS, находится в экзоне 8A и показан синим цветом. Эти данные показывают, что de novo миссенс-мутаций в экзоне 8 Ca V 1,2 вызывают тяжелый синдром удлиненного интервала QT и другие фенотипические аномалии.
( D ) ( Верхний ) Прогнозируемая топология Ca V 1.2, показывающая расположение мутаций. ( Lower ) Гомология аминокислотной последовательности экзонов 8 и 8A. DI / S6 подчеркнут. G402 и G406, аминокислоты, мутировавшие в TS2, оба находятся в экзоне 8 и показаны красным.G406, мутировавший в TS, находится в экзоне 8A и показан синим цветом. Эти данные показывают, что de novo миссенс-мутаций в экзоне 8 Ca V 1,2 вызывают тяжелый синдром удлиненного интервала QT и другие фенотипические аномалии.
Чтобы проверить возможность того, что NM, присутствующий у индивидуума 1, мог быть вызван мутациями в генах, ранее участвовавших в этом заболевании, мы исследовали всю последовательность α-актина скелетных мышц ( ACTA1, ) и 35 экзонов небулина ( NEB ), которые содержат все ранее идентифицированные мутации, связанные с NM.Эти два гена, вероятно, ответственны за ≈75% случаев ЯМ (5). Анализ последовательности не обнаружил мутаций.
Анализ последовательности не обнаружил мутаций.
Ca V 1.2 Экзон 8 высоко экспрессируется в сердце и мозге. В Ca V 1.2 трансмембранный сегмент 6 домена I (D1 / S6) может кодироваться двумя взаимоисключающими экзонами, 8 и 8A. Ранее мы определили тканевое и клеточное распределение альтернативно сплайсированной формы, содержащей экзон 8A (4). Для определения характера экспрессии доминантной альтернативно сплайсированной формы Ca V 1.2, содержащий экзон 8, мы использовали этот экзон в качестве зонда для Нозерн- и дот-блоттинга. В образцах взрослых и плода экзон 8 экспрессировался во многих тканях. Экзон 8 очень сильно экспрессируется в сердце (рис. 3 A ). Этот экзон также экспрессируется на более низких уровнях в головном мозге и надпочечниках. В головном мозге дот-блот анализ показал, что экзон 8 экспрессируется в мозжечке, коре головного мозга, черной субстанции, прилежащем ядре, таламусе и гипофизе. Он также экспрессируется в желудке, тощей кишке, подвздошной кишке, мочевом пузыре, простате, яичках, периферических лейкоцитах, лимфатических узлах, печени и слюнных железах.К органам плода, которые проявляют экспрессию, относятся мозг, сердце, печень, селезенка, тимус и легкие. Для сравнения, экспрессия экзона 8A менее впечатляющая в сердце и мозге, надпочечниках, слюнных железах, периферических лейкоцитах и лимфатических узлах. С другой стороны, экспрессия экзона 8A была выше в органах с гладкими мышцами, включая аорту, мочевой пузырь и матку (4). Ранее мы определили, что экзон 8 составляет ≈80% мРНК в сердце и головном мозге (4). Таким образом, эти данные показывают, что экзон 8 Ca V 1.2 высоко экспрессируется в сердце и головном мозге, что согласуется с серьезными сердечными и когнитивными дефектами, связанными с двумя описанными выше мутациями.
Он также экспрессируется в желудке, тощей кишке, подвздошной кишке, мочевом пузыре, простате, яичках, периферических лейкоцитах, лимфатических узлах, печени и слюнных железах.К органам плода, которые проявляют экспрессию, относятся мозг, сердце, печень, селезенка, тимус и легкие. Для сравнения, экспрессия экзона 8A менее впечатляющая в сердце и мозге, надпочечниках, слюнных железах, периферических лейкоцитах и лимфатических узлах. С другой стороны, экспрессия экзона 8A была выше в органах с гладкими мышцами, включая аорту, мочевой пузырь и матку (4). Ранее мы определили, что экзон 8 составляет ≈80% мРНК в сердце и головном мозге (4). Таким образом, эти данные показывают, что экзон 8 Ca V 1.2 высоко экспрессируется в сердце и головном мозге, что согласуется с серьезными сердечными и когнитивными дефектами, связанными с двумя описанными выше мутациями.

Вариант сплайсинга 1,2 экзона 8 Ca V высоко экспрессируется в сердце и головном мозге. ( A ) Нозерн-блоттинг человека показывает экспрессию экзона 8 Ca V 1,2 экзона 8 в головном мозге, сердце и других тканях. ( B ) дот-блот мРНК демонстрирует экспрессию Ca V 1.2 экзон 8 во множестве тканей плода и взрослого, включая многие области мозга.
Мутации G402S и G406R ухудшают инактивацию канала. Чтобы определить молекулярные последствия мутаций G402S и G406R, мы гетерологично экспрессировали WT и мутантные формы канала Ca V 1.2 в ооцитах Xenopus . Ооциты инъецировали кРНК, кодирующей Ca V 1.2 и его вспомогательные субъединицы Ca V β 2b и Ca V α 2 δ 1 .Мы зарегистрировали активность WT и мутантного канала, используя Ba 2+ (40 мМ) в качестве носителя заряда. Токи Ba 2+ инактивируются намного медленнее, чем токи Ca 2+ , потому что в отсутствие внеклеточного Ca 2+ инактивация каналов почти полностью зависит от трансмембранного напряжения ( В м ) (16). По сравнению с каналами WT (рис.4 A ), зависящая от времени инактивация мутантных каналов резко снизилась за счет обеих мутаций (рис.4 B и C ). Каналы WT и G402S имели аналогичное соотношение I — V и зависимость тока активации от напряжения, тогда как отношения для каналов G406R были смещены на -9 мВ (рис. 4 D и E ). Затем мы определили зависимость инактивации от напряжения, используя 2-секундные кондиционирующие импульсы, как описано в Материалы и методы . В то время как каналы WT инактивировались на 90% после кондиционирующего импульса до +30 мВ, каналы G406R и G402S инактивировались на 12% и 9% соответственно при том же потенциале (рис.
Токи Ba 2+ инактивируются намного медленнее, чем токи Ca 2+ , потому что в отсутствие внеклеточного Ca 2+ инактивация каналов почти полностью зависит от трансмембранного напряжения ( В м ) (16). По сравнению с каналами WT (рис.4 A ), зависящая от времени инактивация мутантных каналов резко снизилась за счет обеих мутаций (рис.4 B и C ). Каналы WT и G402S имели аналогичное соотношение I — V и зависимость тока активации от напряжения, тогда как отношения для каналов G406R были смещены на -9 мВ (рис. 4 D и E ). Затем мы определили зависимость инактивации от напряжения, используя 2-секундные кондиционирующие импульсы, как описано в Материалы и методы . В то время как каналы WT инактивировались на 90% после кондиционирующего импульса до +30 мВ, каналы G406R и G402S инактивировались на 12% и 9% соответственно при том же потенциале (рис. 4 Ф ). Эти данные демонстрируют, что мутации G402S и G406R значительно снижают степень инактивации канала Ca V 1.2, зависящую от напряжения, и продуцируют поддерживаемые внутрь токи Ca 2+ . Таким образом, мутации G402S и G406R имеют эффект усиления функции на кальциевых каналах Ca V 1.2.
4 Ф ). Эти данные демонстрируют, что мутации G402S и G406R значительно снижают степень инактивации канала Ca V 1.2, зависящую от напряжения, и продуцируют поддерживаемые внутрь токи Ca 2+ . Таким образом, мутации G402S и G406R имеют эффект усиления функции на кальциевых каналах Ca V 1.2.
Мутации Ca V 1,2 экзона 8 вызывают почти полное отсутствие потенциал-зависимой инактивации каналов. ( A — C ) WT ( A ), G402S ( B ) и G406R ( C ) Ca V 1,2 канальные токи были зарегистрированы от ооцитов Xenopus в ответ на приложенные импульсы напряжения с шагом 10 мВ от -70 до +40 мВ, второй импульс до +10 мВ. Внешний раствор содержал 40 мМ BaCl 2 для устранения Ca 2+ -зависимой инактивации Ca V 1.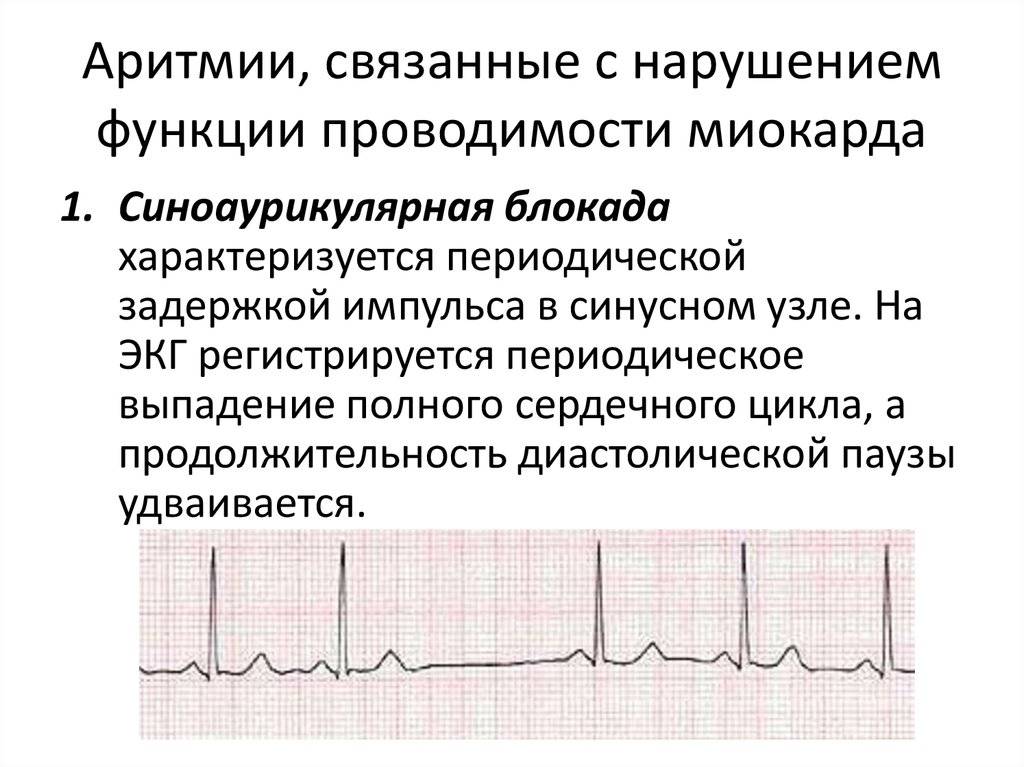 2 канала. Обратите внимание на отсутствие инактивации тока для мутантных каналов по сравнению с токами каналов WT. ( D ) Каналы G406R имеют аналогичное соотношение Ba 2+ вольт-напряжение ( I – V ) по сравнению с WT. ( E ) Зависимость напряжения Ba 2+ ток активации для WT ( В 1/2 = 4,5 ± 0,1 мВ; k = 5,5 ± 0,1 мВ; n = 7), G402S ( V 1/2 = 6.2 ± 0,1 мВ; k = 7,5 ± 0,1 мВ; n = 14) и G406R ( V 1/2 = -4,4 ± 0,3 мВ; k = 5,4 ± 0,2 мВ; n = 14). ( F ) Зависимость напряжения Ba 2+ ток инактивации для WT ( В 1/2 = -6,6 ± 0,4 мВ; k = 7,6 ± 0,4 мВ; n = 8) и мутантный Ca V 1,2 канала. Минимальное значение для относительной инактивации было 0.10 ± 0,01 для WT ( n = 8), но 0,88 ± 0,03 для G406R ( n = 15) и 0,91 ± 0,04 для G402S ( n = 6), что указывает на практически полное отсутствие зависимости инактивации от напряжения.
2 канала. Обратите внимание на отсутствие инактивации тока для мутантных каналов по сравнению с токами каналов WT. ( D ) Каналы G406R имеют аналогичное соотношение Ba 2+ вольт-напряжение ( I – V ) по сравнению с WT. ( E ) Зависимость напряжения Ba 2+ ток активации для WT ( В 1/2 = 4,5 ± 0,1 мВ; k = 5,5 ± 0,1 мВ; n = 7), G402S ( V 1/2 = 6.2 ± 0,1 мВ; k = 7,5 ± 0,1 мВ; n = 14) и G406R ( V 1/2 = -4,4 ± 0,3 мВ; k = 5,4 ± 0,2 мВ; n = 14). ( F ) Зависимость напряжения Ba 2+ ток инактивации для WT ( В 1/2 = -6,6 ± 0,4 мВ; k = 7,6 ± 0,4 мВ; n = 8) и мутантный Ca V 1,2 канала. Минимальное значение для относительной инактивации было 0.10 ± 0,01 для WT ( n = 8), но 0,88 ± 0,03 для G406R ( n = 15) и 0,91 ± 0,04 для G402S ( n = 6), что указывает на практически полное отсутствие зависимости инактивации от напряжения.
Индуцированное G406R ингибирование потенциал-зависимой инактивации канала предположительно было вызвано нарушенной функцией, обычно обеспечиваемой глицином в положении 406. Чтобы определить важность остатка глицина, мы мутировали G406 на несколько других остатков.Замены включали другой основной остаток (лизин), кислотный остаток (глутаминовая кислота), полярный, но незаряженный остаток (серин), небольшие гидрофобные остатки (аланин и валин) и другую отдельную аминокислоту (пролин). Несмотря на различия в физико-химической природе боковых цепей этих остатков, каждая из замен ингибировала потенциал-зависимую инактивацию (рис. 5). Эти данные показывают, что нормальная инактивация однозначно обеспечивается глицином в положении 406 в Ca V 1.2 канала.
Рис. 5.
5.Глицин является важной аминокислотой в положении 406 Ca V 1.2. Зависимость инактивации WT и мутантного экзона 8 Ca v от напряжения в ооцитах Xenopus от напряжения определяли путем измерения пиковой амплитуды тока, вызванного во время импульса до +10 мВ, после 2-секундного кондиционирующего импульса, приложенного к переменной. потенциал.Токи были нормализованы и нанесены на график как функция кондиционирующего потенциала. Внешний раствор содержал 40 мМ BaCl 2 для устранения инактивации, зависящей от Ca 2+ . WT, n = 6; G406R, n = 10; G406E, n = 11; G406K, n = 9; G406P, n = 8; G406S, n = 8; G406V, n = 6; G406A, n = 11.
Ca V 1.2 Мутации продлевают смоделированные возможности действия. У обоих пациентов с TS2 присутствуют две характерные особенности: резкое удлинение интервала QT и опасные для жизни аритмии. Снижение инактивации канала Ca V 1.2 должно продлить внутрь (деполяризация мембраны) ток Ca 2+ во время фазы плато и задержать реполяризацию кардиомиоцитов. Поскольку влияние мутаций G402S и G406R (экзон 8) на функцию канала было одинаковым, мы решили смоделировать эффект мутации G406R и сравнить его с эффектом мутации G406R, идентифицированной в экзоне 8A (4).
Снижение инактивации канала Ca V 1.2 должно продлить внутрь (деполяризация мембраны) ток Ca 2+ во время фазы плато и задержать реполяризацию кардиомиоцитов. Поскольку влияние мутаций G402S и G406R (экзон 8) на функцию канала было одинаковым, мы решили смоделировать эффект мутации G406R и сравнить его с эффектом мутации G406R, идентифицированной в экзоне 8A (4).
Ранее мы определили, что 77% каналов Ca V 1.2 в сердце содержали экзон 8 и 23% содержали экзон 8A (4). Таким образом, в гетерозиготном состоянии 38,5% каналов Ca V 1.2 несут мутацию экзона 8 в случаях TS2 и 11,5% несут мутацию экзона 8A в случаях TS. Мы предположили эти соотношения, чтобы моделировать измененную инактивацию кальциевых каналов L-типа (рис. 6 A ), вызванные мутациями в динамической модели миоцита желудочка человека (13).Мутации увеличивали пиковую концентрацию внутриклеточного Ca 2+ (фиг.6 B ) и увеличенной продолжительности потенциала действия (Рис. 6 C ) при стимуляции модельной клетки с частотой 1 Гц.
6 C ) при стимуляции модельной клетки с частотой 1 Гц.
Компьютерное моделирование выявило пролонгированные потенциалы действия, измененную обработку внутриклеточного кальция и DAD, индуцированные Ca V 1.2 мутации. ( A ) Смоделированная зависимость от напряжения инактивации тока кальциевых каналов L-типа для WT (черный), G406R (зеленый), WT / экзон 8 G406R гетерозигот (красный) и WT / экзон 8A G406R гетерозигот (синий). Относительная инактивация, зависящая от напряжения, была построена как функция В м . ( B ) Переходные процессы внутриклеточного кальция во время моделирования потенциала действия. Пик транзиента был увеличен на 29% у гетерозигот WT / экзон 8 G406R по сравнению с 7% у WT / экзон 8A G406R, поскольку предполагалось, что экспрессия варианта сплайсинга экзона 8 преобладает в сердце с соотношением ≈3. 5: 1. ( C ) Потенциалы сердечного действия были увеличены на 30% у WT / экзон 8 G406R по сравнению с 8% удлинением у гетерозигот WT / экзон 8A G406R. ( D — F ) Переходные процессы [Ca 2+ ] JSR ( D ), [Ca 2+ ] i ( E ) и V м ( F ) были рассчитаны для частоты стимула 3 Гц. За последними тремя потенциалами действия стимуляции 3 Гц следовала пауза.Во время этой паузы экзон WT / экзон 8A G406R приводил к DAD через 509 мс с пиковым напряжением -54 мВ; WT / экзон 8 G406R приводил к сработавшему потенциалу действия через 423 мс с пиковым напряжением 26 мВ. В этой модели DAD возникают в результате спонтанного высвобождения Ca 2+ из саркоплазматического ретикулума. Экспериментальные исследования сердечных миоцитов показали, что DAD являются результатом перегрузки Ca i и последующей активации Na / Ca-обменника и, в меньшей степени, катион-неселективной проводимости, активируемой Ca i и Ca i — активированный Cl — проводимость (23–25).
5: 1. ( C ) Потенциалы сердечного действия были увеличены на 30% у WT / экзон 8 G406R по сравнению с 8% удлинением у гетерозигот WT / экзон 8A G406R. ( D — F ) Переходные процессы [Ca 2+ ] JSR ( D ), [Ca 2+ ] i ( E ) и V м ( F ) были рассчитаны для частоты стимула 3 Гц. За последними тремя потенциалами действия стимуляции 3 Гц следовала пауза.Во время этой паузы экзон WT / экзон 8A G406R приводил к DAD через 509 мс с пиковым напряжением -54 мВ; WT / экзон 8 G406R приводил к сработавшему потенциалу действия через 423 мс с пиковым напряжением 26 мВ. В этой модели DAD возникают в результате спонтанного высвобождения Ca 2+ из саркоплазматического ретикулума. Экспериментальные исследования сердечных миоцитов показали, что DAD являются результатом перегрузки Ca i и последующей активации Na / Ca-обменника и, в меньшей степени, катион-неселективной проводимости, активируемой Ca i и Ca i — активированный Cl — проводимость (23–25).
Переходные процессы концентрации кальция в соединительном саркоплазматическом ретикулуме ([Ca 2+ ] JSR , рис. 6 D ), внутриклеточная концентрация кальция ([Ca 2+ ] i , рис. 6 E ) и V м (рис.6 F ) были рассчитаны для миоцита, несущего мутацию экзона 8 или экзона 8A, и стимулировали с частотой стимула 3 Гц.Прекращение действия стимулов приводило к отсроченной постдеполяризации (DAD) через ≈0,5 с для экзона 8A G406R и запускало потенциал действия для экзона 8 G406R (рис. 6 F ). ). Известно, что ДАД или триггерные возбуждения являются аритмогенными (17).
Нестабильность в [Ca 2+ ] JSR , [Ca 2+ ] i и V m могло быть вызвано резким изменением скорости стимуляции. На рис.7, при t = 0 с, частота стимула была переключена с 2,5 на 3 Гц, и миоциты электрически активировались с большей скоростью в течение 1–300 дополнительных циклов. Пиковые значения [Ca 2+ ] JSR , [Ca 2+ ] i и V м. после прекращения каждой серии электростимуляций были определены и нанесены на рис. 7 A – C . Переходная фаза показала значительные альтернативы с DAD, которые иногда могут запускать потенциал действия для миоцита экзона 8 G406R.Напротив, DAD для миоцита экзона 8A G406R были в основном подпороговыми для запуска потенциала действия. Эти симуляции предсказывают, что мутация экзона 8 G406R (такая же для G402S) вызывает заметное удлинение сердечных потенциалов действия и DAD, что согласуется с серьезным удлинением интервала QT и высоким риском аритмии у людей TS2. Предполагается, что мутация экзона 8A вызывает меньшее удлинение потенциала действия и электрических альтернатив, но также может вызывать аритмию.
На рис.7, при t = 0 с, частота стимула была переключена с 2,5 на 3 Гц, и миоциты электрически активировались с большей скоростью в течение 1–300 дополнительных циклов. Пиковые значения [Ca 2+ ] JSR , [Ca 2+ ] i и V м. после прекращения каждой серии электростимуляций были определены и нанесены на рис. 7 A – C . Переходная фаза показала значительные альтернативы с DAD, которые иногда могут запускать потенциал действия для миоцита экзона 8 G406R.Напротив, DAD для миоцита экзона 8A G406R были в основном подпороговыми для запуска потенциала действия. Эти симуляции предсказывают, что мутация экзона 8 G406R (такая же для G402S) вызывает заметное удлинение сердечных потенциалов действия и DAD, что согласуется с серьезным удлинением интервала QT и высоким риском аритмии у людей TS2. Предполагается, что мутация экзона 8A вызывает меньшее удлинение потенциала действия и электрических альтернатив, но также может вызывать аритмию.
Преходящие изменения частоты стимуляции приводят к электрофизиологической нестабильности в миоцитах, несущих мутации канала Ca V 1.2. В этом моделировании частота стимула была увеличена с 2,5 до 3 Гц в момент времени 0 с. Затем миоцит стимулировали с частотой 3 Гц в течение переменной продолжительности (–), после чего следовала пауза. Пиковые значения [Ca 2+ ] JSR ( A ), [Ca 2+ ] i ( B ) и V m ( C ), а также Время начала спонтанного высвобождения кальция ( D ) определяли во время паузы.Время начала указывается относительно времени последнего стимула. В переходной фазе миоциты с WT / экзоном 8A G406R Ca V 1.2 показали подпороговые значения DAD между t = 9 и 77 с. При более длительном времени ( t > 77 с) DAD запускал потенциал действия. Миоциты с WT / экзоном 8 G406R Ca V 1.2 также обнаруживали DAD, которые были спорадическими в течение t <82 с. Только некоторые из этих DAD запускают потенциалы действия (например, при t = 67 с).Миоциты WT никогда не показывали DAD. Вместе эти симуляции предсказывают, что мутации Ca V 1.2 способствуют электрофизиологической нестабильности, которая может вызвать летальную аритмию в ответ на относительно незначительные изменения частоты сердечных сокращений.
При более длительном времени ( t > 77 с) DAD запускал потенциал действия. Миоциты с WT / экзоном 8 G406R Ca V 1.2 также обнаруживали DAD, которые были спорадическими в течение t <82 с. Только некоторые из этих DAD запускают потенциалы действия (например, при t = 67 с).Миоциты WT никогда не показывали DAD. Вместе эти симуляции предсказывают, что мутации Ca V 1.2 способствуют электрофизиологической нестабильности, которая может вызвать летальную аритмию в ответ на относительно незначительные изменения частоты сердечных сокращений.
Обсуждение
Мы пришли к выводу, что дисфункция Ca V 1.2 вызывает тяжелый синдром аритмии, TS2. В этом исследовании de novo миссенс-мутаций G402S и G406R возникли в Ca V 1.2 экзон 8, доминантный вариант сплайсинга в сердце и головном мозге. Напротив, TS является результатом идентичной мутации G406R в экзоне 8A Ca V 1,2, варианте сплайсинга, который составляет ≈20% сердечных мРНК. В соответствии с этим выводом, у лиц с TS средний QTc составлял 580 мс, множественные аритмии были редкими, и большинство аритмий было связано с приемом лекарств и / или анестезией. Однако пациенты с TS2 имели средний QTc 640 мс и множественные эпизоды неспровоцированной аритмии. Как и при TS, механизм аритмии снижается Ca V 1.2 инактивация канала, приводящая к сохранению деполяризующих токов Ca 2+ во время фазы плато сердечного потенциала действия. Во время фазы плато наружный ток относительно невелик, поэтому даже незначительные изменения входящего кальциевого тока приводят к значительному удлинению интервала QT. Это удлинение, в свою очередь, приводит к повышенному риску спонтанной аномальной вторичной деполяризации (постдеполяризации), аритмии и внезапной смерти.
В соответствии с этим выводом, у лиц с TS средний QTc составлял 580 мс, множественные аритмии были редкими, и большинство аритмий было связано с приемом лекарств и / или анестезией. Однако пациенты с TS2 имели средний QTc 640 мс и множественные эпизоды неспровоцированной аритмии. Как и при TS, механизм аритмии снижается Ca V 1.2 инактивация канала, приводящая к сохранению деполяризующих токов Ca 2+ во время фазы плато сердечного потенциала действия. Во время фазы плато наружный ток относительно невелик, поэтому даже незначительные изменения входящего кальциевого тока приводят к значительному удлинению интервала QT. Это удлинение, в свою очередь, приводит к повышенному риску спонтанной аномальной вторичной деполяризации (постдеполяризации), аритмии и внезапной смерти.
Кардинальная черта TS — простая синдактилия; В 100% случаев проявлялась эта особенность.Ни в одном из представленных здесь случаев не было синдактилии. Вероятно, это различие является результатом дифференциальной экспрессии экзонов 8 и 8A. Другими основными фенотипическими различиями между TS и представленными здесь случаями являются серьезность дефектов ЦНС у индивидуума 1 (экзон 8 G406R). Предположительно эти дефекты происходят из-за того, что экзон 8 представляет ≈80% мРНК Ca V 1.2 в головном мозге. Тот факт, что случай 2 имел относительно легкие особенности ЦНС (до повреждения мозга, вызванного аритмией), может быть связан с тем, что этот человек представляет собой мозаику.Ранее мы идентифицировали мозаицизм у людей с мутациями экзона 8A, которые также имели более мягкий или нормальный фенотип.
Другими основными фенотипическими различиями между TS и представленными здесь случаями являются серьезность дефектов ЦНС у индивидуума 1 (экзон 8 G406R). Предположительно эти дефекты происходят из-за того, что экзон 8 представляет ≈80% мРНК Ca V 1.2 в головном мозге. Тот факт, что случай 2 имел относительно легкие особенности ЦНС (до повреждения мозга, вызванного аритмией), может быть связан с тем, что этот человек представляет собой мозаику.Ранее мы идентифицировали мозаицизм у людей с мутациями экзона 8A, которые также имели более мягкий или нормальный фенотип.
Скелетная миопатия у человека 1 не может быть прямым следствием мутации Ca V 1.2 G406R. Экспрессия Ca V 1.2 в скелетных мышцах низкая. Кроме того, экзон 8A, а не экзон 8, является экзоном доминантных скелетных мышц с соотношением ≈20: 1 как в скелетных мышцах плода, так и в скелетных мышцах взрослого человека (I.S., неопубликованные наблюдения). Скелетная миопатия не является основным признаком TS, который вызывается Ca V 1. 2 мутации экзона 8А. Одним из возможных объяснений этого очевидного парадокса может быть то, что человек 1 был иммобилизован из-за серьезных дефектов ЦНС. Известно, что иммобилизация может вызывать образование немалинового стержня (18).
2 мутации экзона 8А. Одним из возможных объяснений этого очевидного парадокса может быть то, что человек 1 был иммобилизован из-за серьезных дефектов ЦНС. Известно, что иммобилизация может вызывать образование немалинового стержня (18).
Описанные здесь мутации расположены в динуклеотидах CpG. Предполагая, что мутация произошла в некодирующей цепи, в обоих случаях мутация была от CpG к TpG. Изменение CpG на TpG вызывается дезаминированием метилированного цитозина и является наиболее частой спонтанной мутацией в биологии (19, 20).Переход от C к T приведет к наблюдаемому изменению G-на-A на кодирующей цепи в последующем цикле репликации ДНК.
Замена G406 на несколько различных остатков нарушила инактивацию канала Ca V 1.2, аналогичную той, которая индуцировалась G406R, вызвавшим TS2. Это открытие указывает на то, что глицин необходим в положении 406 и, вероятно, также необходим в положении 402. Глицин может действовать как точка шарнира в α-спиральной структуре белков. На основании рентгеновской кристаллографической структуры открытие бактериального канала MthK происходит, когда порообразующая внутренняя α-спираль изгибается у высококонсервативного остатка глицина (21).Остаток глицина в гомологичном положении расположен в трансмембранном домене S6 большинства калиевых каналов, где он также может действовать как шарнир для ворот активации (22). Мы предполагаем, что G406 (и, возможно, G402) действует как шарнир для внутриклеточного, зависимого от напряжения ворот инактивации Ca V 1.2, который закрывается в ответ на деполяризацию мембраны и отличается от механизма стробирования инактивации, который зависит от [Ca 2 + ] и (16).
Таким образом, мы обнаружили две дополнительные миссенс-мутации в сегменте S6 домена I Ca V 1.2, что вызывает TS2. Эти данные подтверждают важность потенциал-зависимой инактивации кальциевых каналов L-типа для поддержания нормального гомеостаза Ca 2+ во многих органах.
Благодарности
Мы благодарим всех участников исследования и их семьи за пожертвованное время и образцы; Л. Шарп, А. Черри, К. Пирсон, К. Пелин, М. Берк, Б. Дил, М. Гуджрати, К. Таллури, Центр общих клинических исследований Детской больницы и Фонд синдромов внезапной аритмии и смерти для технических специалистов. помощь или направление пациентов; Н.Солдатова и Н. Даскаля для экспрессионных конструкций; и С. Приори, Э. Энгл, Р. Касс и Д. Клэпхэм за критический обзор рукописи. Эта работа была поддержана Фондом Чарльза Х. Гуда (IS), Национальными институтами здравоохранения Гранты T32 HL07572 (для IS), HL46401 и HL52338 (для MTK и MCS), AR44345 (для AHB) и P30 HD18655 (для Mental Центр исследования умственной отсталости при детской больнице) и Фонд Дональда В. Рейнольдса (MTK и IS).
Сноски
↵ ¶ Кому должна быть адресована корреспонденция.Электронная почта: igor {at} enders.tch.harvard.edu.
Вклад авторов: I.S., F.B.S. и M.C.S. спланированное исследование; I.S., K.W.T., N.D., P.K. и F.B.S. проведенное исследование; A.H.B. внесены новые реагенты / аналитические инструменты; I.S., K.W.T., N.D., F.B.S., A.H.B., M.C.S. и M.T.K. проанализированные данные; и является. и M.T.K. написал газету.
Этот вклад является частью специальной серии вступительных статей членов Национальной академии наук, избранных 20 апреля 2004 г.
Сокращения: Ca V 1.2, сердечный кальциевый канал L-типа; QTc, интервал QT с поправкой на частоту сердечных сокращений; TS, синдром Тимоти; NM, немалиновая миопатия; torsades, torsades de pointes желудочковая тахикардия; [Ca 2+ ] JSR , концентрация кальция в соединительном саркоплазматическом ретикулуме; [Ca 2+ ] i , внутриклеточная концентрация кальция; В м , трансмембранное напряжение; ДАД — отсроченная деполяризация; кРНК, комплементарная РНК.
См. Сопроводительную биографию на странице 8086.
- Copyright © 2005, Национальная академия наук
Аритмия | Система Здравоохранения Мемориал
Ваше сердце имеет сложную электрическую систему, но иногда в этой системе случается короткое замыкание. Результатом может быть аритмия, то есть ненормальное или нерегулярное сердцебиение. Одна из наиболее частых аритмий — фибрилляция предсердий (AFib).
Memorial Cardiac and Vascular Institute предлагает разнообразные методы лечения сердечной аритмии для лечения ФП и связанных с ней состояний — от лекарств до высокотехнологичных вмешательств в электрофизиологической лаборатории. Наши специалисты по сердечному ритму проводят большинство процедур лечения аритмии в Южной Флориде с отличными результатами.
Что такое аритмия?
Аритмия — это ненормальная частота сердечных сокращений или ритм. Слишком быстрое (тахикардия), слишком медленное (брадикардия) или нерегулярное сердцебиение может повлиять на способность сердца перекачивать кровь.Нерегулярный кровоток имеет более высокую вероятность образования сгустков, как это может случиться при фибрилляции предсердий (когда учащенное сердцебиение позволяет крови скапливаться в сердце). Аритмия также может препятствовать попаданию крови в сердце или мозг. Вот почему аритмия увеличивает риск инсульта или сердечного приступа.
Не все сердечные аритмии являются симптоматическими, но если у вас есть симптомы, они могут включать:
- Ощущение «трепетания» в сердце или ощущение, что сердце «пропускает» удары
- Головокружение или дурноту
- Обморок или почти обморок
- Боль в груди
- Аномальное потоотделение
- Одышка
Как мы лечим сердечную аритмию в Мемориале
Диагноз аритмии может вызывать беспокойство.Мы понимаем это и ежегодно лечим сотни людей от нерегулярного сердцебиения. В Мемориале мы предлагаем:
- Экспертный диагноз: Мы диагностируем аритмию, используя как неинвазивные мониторинговые тесты, так и малоинвазивные тесты, которые анализируют электрическую активность вашего сердца. Перед заказом теста наши специалисты по сердечному ритму сотрудничают с группами кардиологической визуализации и катетеризации сердца, чтобы определить подходящий тест для каждого пациента.
- Центр абляции большого объема: Распространенным методом лечения аритмий является абляция сердца.Выполняем радиочастотную абляцию и криоабляцию. Радиочастотная абляция использует тепло для безопасного разрушения сердечной ткани, вызывающей нерегулярный ритм. Криоабляция выполняет ту же функцию, но использует холод вместо тепла. В рамках крупномасштабной программы мы проводим более 700 абляций сердца каждый год, что дает нам значительный опыт.
- Сложные кабинеты электрофизиологии: Электрофизиология — это раздел кардиологии, который фокусируется на электрической активности сердца. У нас есть три кабинета, посвященные электрофизиологическим процедурам, оснащенные новейшими инструментами для лечения пациентов с аритмией.Например, с помощью технологии трехмерного картирования мы можем точно определить местонахождение аритмии.
- Имплантируемые устройства: При опасной для жизни аритмии, которую нельзя вылечить с помощью лекарств или абляции, мы можем имплантировать кардиостимулятор для коррекции медленного сердцебиения или имплантируемый кардиовертер-дефибриллятор (ICD) для коррекции быстрого или нерегулярного сердцебиения.
- Командный подход к уходу: Наша команда готова помочь вам, независимо от того, страдаете ли вы аритмией или связанной с ней ишемической болезнью сердца, кардиомиопатией, сердечной недостаточностью или врожденным пороком сердца.Все наши сердечно-сосудистые специалисты работают вместе на благо пациента. Мы называем этот подход TotalHeart: единый центр с несколькими специалистами и вариантами лечения.
Типы сердечных аритмий, которые мы лечим
Мы лечим несколько типов нарушений сердечного ритма, в том числе:
- Фибрилляция предсердий (AFib): Самый распространенный тип серьезной аритмии. AFib заставляет верхние камеры сердца трястись или биться нерегулярно. Это увеличивает риск инсульта и сердечного приступа.Около 9 процентов американцев старше 65 лет страдают AFib.
- Наджелудочковая тахикардия (СВТ): При СВТ иногда сердце бьется слишком быстро. Не все случаи СВТ нуждаются в лечении. Тем, кто это делает, мы используем абляцию, чтобы безопасно разрушить сердечную ткань, вызывающую аритмию.
- Желудочковая тахикардия (ЖТ): ЖТ встречается реже, чем СВТ, и может быть опасной для жизни. Мы часто лечим ЖТ абляцией.
- Синдром Вольфа-Паркинсона-Уайта (WPW): Учащенное сердцебиение, вызванное дополнительным электрическим путем, WPW поддается лечению с помощью лекарств или абляции.
- Сердечные каналопатии: Эти наследственные аритмии включают синдром удлиненного интервала QT и синдром укороченного интервала QT. Мы проверяем их в семьях и лечим их лекарствами или другими способами.
- Синдром постуральной ортостатической тахикардии (POTS): POTS — это учащенное сердцебиение при стоянии. Обычно мы можем лечить это лекарствами.
Свяжитесь с нами для лечения аритмии
Чтобы записаться на прием или узнать больше о сердечно-сосудистой помощи в «Мемориале», позвоните по телефону 954-276-7800.
Познакомьтесь с нашей командой специалистов по сердечному ритму
Врачи родственных занятий
Пособие для пациентов: аритмия
US Pharm. 2017; 42 (2): 13-14.
Нерегулярное сердцебиение
Все органы и ткани зависят от правильной работы сердца по доставке богатой кислородом крови к остальным частям тела. Аритмия , состояние, при котором электрическая система сердца нарушена, является одной из причин, по которой сердце не может выполнять эту жизненно важную функцию. При аритмии сердце бьется слишком быстро, слишком медленно или беспорядочно. Аритмии могут быть опасными для жизни, например, в случае желудочковой тахикардии или фибрилляции желудочков. Боль в груди, головокружение, потливость и потеря сознания являются симптомами этих опасных для жизни аритмий и требуют немедленной медицинской помощи.
Хотя это может наблюдаться у здоровых людей, часто причиной является другое заболевание
Чтобы лучше понять аритмию, важно знать, как работает сердце.Сердце состоит из четырех камер: двух предсердий (верхних камер) и двух желудочков (нижних камер). Группа нервов, называемая узлом sinus (SA) , расположена в верхней части правого предсердия. Узел SA отвечает за запуск сердцебиения — это естественный кардиостимулятор организма. Во время сердцебиения электрический сигнал распространяется через верхнюю часть сердца, заставляя предсердия сокращаться. Затем сигнал распространяется через нижнюю часть сердца, и желудочки сокращаются.Чтобы сердце билось правильно, ток электричества через сердце должен происходить именно в таком порядке. В нормальных условиях человеческое сердце бьется от 50 до 100 раз в минуту. Когда сердце бьется быстрее, чем обычно, или более 100 ударов в минуту, это состояние называется тахикардией . Когда сердце сокращается менее 50 ударов в минуту, это состояние называется брадикардией . Обычно сердце бьется примерно с одинаковым промежутком времени между каждым сокращением (обычный ритм).Когда сердцебиение происходит с большим или меньшим промежутком времени между сокращениями, ритм считается нерегулярным.
Причины аритмииАритмия — обычное явление, от нее страдают более 4 миллионов человек в Соединенных Штатах. Аритмия также может возникать в здоровом сердце, но часто причиной этого являются другие состояния или заболевания. Распространенными причинами, связанными с сердцем, являются уплотнение (сужение) артерий, высокое кровяное давление, ошибки в электрической структуре («проводке») сердца, повреждение сердечной мышцы после сердечного приступа и восстановление после операции на сердце.Причинами, не связанными с сердцем, являются недостаточная или сверхактивная щитовидная железа, несбалансированный уровень натрия и калия, стресс, некоторые лекарства, диабет, апноэ во сне (затрудненное дыхание во сне) и генетика. Курение, употребление наркотиков и алкоголь также могут привести к аритмии. Риск развития аритмии увеличивается с возрастом.
ЛечениеЦели лечения аритмии — восстановить нормальную частоту сердечных сокращений и ритм и предотвратить сердечные приступы и инсульт. Кардиолог может назначить лекарства, контролирующие частоту и ритм сердца.Бета-адреноблокаторы (метопролол, пропранолол) и блокаторы кальциевых каналов (дилтиазем) — это классы препаратов, используемых для поддержания частоты сердечных сокращений от 60 до 100 ударов в минуту. Блокаторы натриевых каналов (пропафенон, флекаинид) и блокаторы калиевых каналов (дофетилид, соталол AF) — это классы, используемые для коррекции сердечного ритма. Хирургическая процедура (называемая аблацией ), которая использует радиочастоты для разрушения небольшого количества сердечных клеток, может быть выполнена для предотвращения того, чтобы клетки запускали случайные сердцебиения.В тяжелых случаях можно использовать кардиостимулятор или имплантируемый кардиовертер-дефибриллятор для контроля электрической системы сердца и обеспечения автоматической коррекции при возникновении аритмии.
Наиболее распространена фибрилляция предсердийСамым распространенным типом аритмии является фибрилляция предсердий (ФП), при которой предсердия сердца сокращаются нерегулярно. Самый большой риск, связанный с ФП, — это инсульт. Если ФП длится достаточно долго, кровь может начать образовывать сгусток в предсердии.Этот сгусток может перемещаться из сердца в мозг. В результате врачи прописывают людям с ФП препараты для разжижения крови. Разжижители крови (антикоагулянты) предотвращают образование сгустка и снижают риск инсульта. Наиболее распространенными антикоагулянтами на рынке являются кумадин (варфарин), прадакса (дабигатран), ксарелто (ривароксабан), Eliquis (апиксабан) и савайса (эдоксабан).
Ваш местный фармацевт всегда готов помочь. Если у вас, вашего друга или члена семьи есть вопросы о лекарствах, используемых при аритмии, обратитесь к проверенному фармацевту или другому поставщику медицинских услуг.
Кардиология | Аритмия (нерегулярное сердцебиение)
Аритмия, обычно известная как нерегулярное сердцебиение, представляет собой проблему, связанную с частотой биений сердца, его ритмом или и тем, и другим.
Большинство аритмий не опасны, и беспокоиться о них не о чем. Они могут раздражать и могут застать вас врасплох, но они не должны причинять вам вреда или вызывать какие-либо долгосрочные последствия для здоровья. Но некоторые из них могут быть очень серьезными и даже могут привести к тому, что ваше сердце перестанет эффективно перекачивать кровь или полностью перестанет биться.
Если ваше сердце не перекачивает кровь по всему телу эффективно, вы можете пострадать от повреждения мозга и других органов. Узнайте о различных типах аритмий.
Почему возникают аритмии?
Сердце бьется, потому что нервные клетки в организме посылают электрические сигналы в камеры сердца, заставляя их сокращаться. Если электрические сигналы не работают должным образом или не могут добраться до нужного места, может возникнуть аритмия.
Когда возникают аритмии?
Аритмия может случиться с кем угодно, но есть некоторые вещи, которые могут ее вызвать.Например:
- Сердечный приступ
- Медицинские состояния, в том числе:
- Высокое кровяное давление
- Ишемическая болезнь сердца (болезнь сердца)
- Сердечная недостаточность
- Заболевание щитовидной железы (как гипотиреоз, так и гипертиреоз)
- Ревматическая лихорадка
- Генетические пороки сердца, такие как:
- Синдром Вольфа-Паркинсона-Уайта (также известный как WPW)
- Стресс
- Выбор образа жизни, например:
- Курение
- Чрезмерное употребление алкоголя
- Некоторые виды наркотиков , например, амфетамины или кокаин
- Чрезмерное употребление кофеина или других стимуляторов
- Лекарства, отпускаемые по рецепту и без рецепта
Причины некоторых аритмий неизвестны.
Как узнать, что у вас аритмия?
Не все аритмии вызывают заметные симптомы. Те, которые действительно часто вызывают у людей переживания:
- Чувство, будто ваше сердце не бьется нормально; может казаться:
- Слишком быстро
- Слишком медленно
- Слишком сильно
- Как будто ритм нерегулярный
- Как трепет в груди
- Как пропущенный ритм
- Некоторые люди также испытывают:
- Головокружение, головокружение или обморок
- Одышка
- Усталость или недостаток энергии
- Потоотделение
- Приливы жара
- Боль в груди, давление, стеснение или дискомфорт в груди
- Беспокойство
- Проблемы с повседневными делами или упражнениями
- Учащенное мочеиспускание (чаще пользоваться туалетом)
Что делать, если вы считаете, что у вас аритмии
Многие аритмии не опасны, но вам все равно следует обратиться к врачу, который сможет диагностировать ваши аритмии и лечить их если необходимо.Поговорите со своим врачом и попросите направление к электрофизиологу (врачу, который специализируется на нарушениях сердечного ритма). Он или она расскажет вам о ваших симптомах, изучит медицинский анамнез, расскажет о сердечных заболеваниях и аритмии в вашей семье, а также проведет медицинский осмотр. Ваш врач также может сделать ЭКГ и назначить другие тесты или кардиомониторы.
Если у вас есть признаки или симптомы сердечного приступа, немедленно звоните 911 или обратитесь за медицинской помощью. Не у всех, кто страдает сердечным приступом, есть эти симптомы, и у большинства людей они не все, поэтому, если вы когда-либо сомневаетесь, немедленно обратитесь за медицинской помощью.Некоторые из признаков и симптомов сердечного приступа:
- Боль в груди, давление или дискомфорт, обычно в центре груди
- Боль или дискомфорт в одной или обеих руках, спине, шее, челюсти, или в области живота
- Одышка (даже без боли в груди)
- Тошнота
- Холодный пот
- Головокружение
Тесты для диагностики аритмий
Аритмии сложно диагностировать, потому что они часто проходят быстро, поэтому некоторые тесты и физические экзамены могут не поймать их.
Вот некоторые из тестов, используемых для диагностики аритмий:
- Электрокардиограмма (ЭКГ или ЭКГ): снимок электрической активности вашего сердца. Электроды прикрепляются к груди, рукам и ногам. Эти электроды измеряют частоту и ритм вашего сердца.
- Портативные мониторы:
- Монитор Холтера: портативный монитор ЭКГ, который крепится к груди и может носить в течение дня или до двух недель одновременно
- Монитор событий: портативные мониторы ритма для пациентов с нерегулярным сердечным ритмом менее часто.Вы можете носить монитор всегда и активировать его, когда чувствуете симптомы, или можете подключиться к монитору, когда чувствуете симптомы.
- Мобильный кардиомонитор: носится до 30 дней, регистрирует сердцебиение как в нормальном, так и в ненормальном ритме; результаты автоматически отправляются вашему врачу.
- Вставной петлевой регистратор: вводится под кожу и может автоматически записывать паттерны аномального ритма в течение трех лет
- Рентген грудной клетки: делает снимки грудной клетки, чтобы определить, увеличено ли ваше сердце
- Эхокардиограмма: использует звуковые волны для создания изображений вашего сердца.Этот тест позволяет вашему врачу увидеть, как ваша сердечная мышца движется и качает кровь. У вас может быть один из нескольких типов эхокардиограммы:
- Трансторакальная эхокардиограмма, TTE: неинвазивная эхокардиограмма, которая дает вашему врачу изображение вашего сердцебиения; техник использует устройство для визуализации звуковых волн вашего сердца
- Чреспищеводная эхокардиограмма, TEE: неинвазивная эхокардиограмма, которая помогает получить хорошее изображение задней части сердца; Техник использует устройство для визуализации и помещает его в пищевод, потому что пищевод проходит за вашим сердцем.
- Компьютерная томография сердца (КТ) или магнитно-резонансная томография (МРТ) : позволяет техническим специалистам получить трехмерное изображение сердца и грудной клетки, когда они бьются
- Электрофизиологические исследования (EPS): измеряет электрическая активность в сердце. Они используются для диагностики основной причины аритмий. Во время теста крошечные катетеры вводятся в вену или артерию. Эти катетеры представляют собой электроды, которые могут стимулировать сердце и регистрировать электрическую активность.Если врач обнаружит дополнительный путь, вызывающий аритмию, он или она может одновременно выполнить абляцию сердца.
- Проверка наклона стола : тест, используемый для определения причин обморока (падение артериального давления или временная потеря сознания)
Вы можете помочь своему врачу, отслеживая свою диету и режим упражнений, а также когда у вас есть аритмия. Если у вас перемежающиеся аритмии, анализ этой информации поможет вам и вашему врачу понять, что может вызвать вашу аритмию.
Аритмия (нарушение сердечного ритма) | Temple Health
Что означает аритмия?
Аритмия означает ненормальное сердцебиение. Сюда входит сердцебиение:
- Слишком быстро (тахикардия)
- Слишком медленно (брадикардия)
- Неправильно или если электрические сигналы приходят не в том месте
Нормальный электрический паттерн сердца называется «синусовым ритмом», когда каждое сердцебиение начинается с его естественной точки кардиостимулятора, расположенной в правом верхнем отделе сердца (правое предсердие).Затем этот электрический сигнал проходит от верхней половины сердца (правого и левого предсердия) до нижней половины сердца (правого и левого желудочка) с помощью специальной электрической системы.
Если есть проблема с нормальными частями электрической системы сердца, сердце может биться слишком медленно.
Когда могут возникать аритмии?
Аритмия (также называемая ненормальным сердечным ритмом) может возникать, когда одна или несколько точек «просыпаются» и начинают испускать электрические сигналы.Или когда сердце застревает в результате короткого замыкания по разным причинам.
Эти быстрые ритмы могут исходить из верхних камер сердца (наджелудочковые или предсердные аритмии) или нижних камер (желудочковые аритмии).
Опасны ли аритмии?
Аритмии могут варьироваться от единичных дополнительных ударов сердца до более продолжительных эпизодов, которые приходят и уходят, и до аномальных ритмов, которые являются постоянными. Многие аритмии не опасны и лечатся из-за симптомов, которые они вызывают.

 223.2273, добавочный номер 4-6697 или запишитесь на прием онлайн.
223.2273, добавочный номер 4-6697 или запишитесь на прием онлайн. Импульсы задерживаются. Это самый легкий тип сердечной блокады.
Импульсы задерживаются. Это самый легкий тип сердечной блокады. Блок третьей степени серьезно влияет на способность сердца перекачивать кровь к вашему телу.
Блок третьей степени серьезно влияет на способность сердца перекачивать кровь к вашему телу.
 Если вам нужен монитор, вы получите подробную информацию о том, как им пользоваться.
Если вам нужен монитор, вы получите подробную информацию о том, как им пользоваться.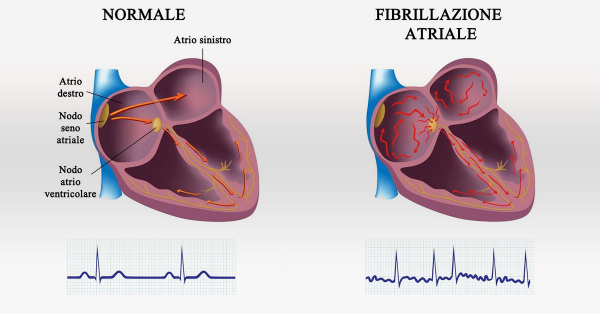 При необходимости ваш поставщик медицинских услуг может изменить ваше лекарство на лекарство другого класса.
При необходимости ваш поставщик медицинских услуг может изменить ваше лекарство на лекарство другого класса.